
Dr. Lyle Newball Henry Colombia
Dra. Laura Romero De León Colombia
En la actualidad la cirugía de catarata ha dejado de considerarse simplemente una necesidad por el proceso natural del envejecimiento y se ha convertido en casi que una cirugía refractiva, dados los avances tanto en la técnica quirúrgica, con el paso de la cirugía extracapsular a la facoemulsi cación, como por la tecnología de las lentes intraoculares. Las típicas han sido monofocales y esféricas, pero ahora con- tamos con las llamadas “premium” en las que se encuentran las multifocales, asféricas, acomodativas y tóricas.
Las LIO multifocales y acomodativas se suelen usar principalmente en pacientes con presbicia y catarata sin otras comorbilidades oculares. Las lentes tóricas se encuentran diseñadas para compensar el astigmatismo corneal y las asféricas, para compensar la aberración esférica positiva corneal.
 En la evaluación del paciente con glauco- ma y catarata encontramos que la agudeza visual, el campo visual, la percepción del color y la sensibilidad al contraste pueden estar alteradas, siendo reversibles sólo los defectos asociados a la catarata, por lo que el compromiso en el campo visual y en la sensibilidad al contraste permanecerán afectados aún después de una cirugía de catarata exitosa, y el resultado refractivo puede no ser el deseado en los pacientes que desean menor dependencia de gafas. Por tal motivo, el oftalmólogo debe ser muy claro con las expectativas del paciente y debe conocer los benecios
En la evaluación del paciente con glauco- ma y catarata encontramos que la agudeza visual, el campo visual, la percepción del color y la sensibilidad al contraste pueden estar alteradas, siendo reversibles sólo los defectos asociados a la catarata, por lo que el compromiso en el campo visual y en la sensibilidad al contraste permanecerán afectados aún después de una cirugía de catarata exitosa, y el resultado refractivo puede no ser el deseado en los pacientes que desean menor dependencia de gafas. Por tal motivo, el oftalmólogo debe ser muy claro con las expectativas del paciente y debe conocer los benecios
lentes intraoculares.
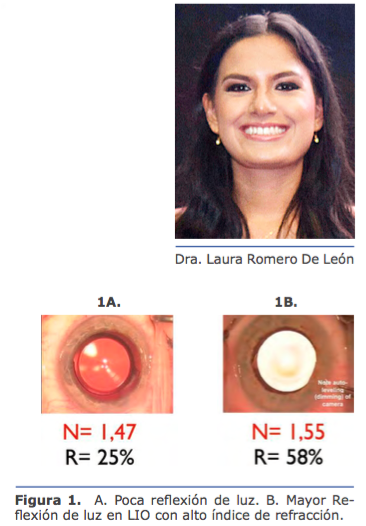
El uso de lentes premium en pacientes con glaucoma es un tema muy controversial, por tanto, para una selección correcta de la lente se de- ben considerar varios factores, y uno de ellos es el diseño y el material de éste. Es importante conocer el índice de refracción de la lente, la re ec- tancia, la capacidad de corrección de aberraciones esférica y cromática y que no genere mucho impacto sobre la transmisión de luz y sobre la sensibilidad al contraste. Figura 1.
Re exión de luz en 2 lentes acrílicos hidrofóbicos del mismo poder con la misma intensidad de luz y con diferente índice de refracción.
Los pacientes con hipertensión ocular o con un estadio incipiente de glaucoma se pueden bene ciar de cualquiera de las lentes que hay en el mercado, de la misma manera que un paciente con catarata y sin glaucoma. Para aquellos interesados en corrección de visión cercana, es menester explicarles la posibilidad de progresión en el futuro y cómo se podría afectar el resultado refractivo, pero esto no les debería negar la posibilidad de po- der corregir en el mismo acto quirúrgico su visión cercana.
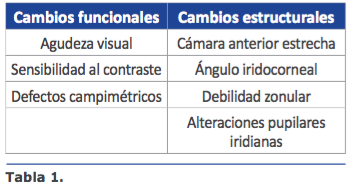
Los pacientes con catarata y glaucoma, además de los cambios morfológicos y funcionales en el nervio óptico y en el campo visual, presentan diferencias anatómicas, estructurales y funcionales que pueden afectar la evaluación preoperatoria (AV, campo visual y sensibilidad al contraste), la intervención quirúrgica (profundidad de cámara anterior, ángulo iridocorneal, dilatación pupilar, inestabilidad zonular) y el seguimiento posoperatorio (hipertensión ocular). Estos son aspectos que se deben tener en cuenta para la selección e indicación del tipo de lente intraocular, y con mayor razón si se trata de una lente intraocular premium.
 CAMBIOS FUNCIONALES
CAMBIOS FUNCIONALES
Agudeza visual y sensibilidad al contraste
La agudeza visual es el mínimo tamaño de una gura de alto contraste que un paciente puede reconocer, mientras que la sensibilidad al contraste (SC) es la capacidad que tiene el sistema visual para percibir un objeto de su fondo.
La agudeza visual por sí sola es un mal indicador de evaluación funcional de glaucoma. Pacientes con glaucomas avanza- dos pueden presentar excelentes agudezas visuales; en cambio, la disminución de la sensibilidad al contraste ha mostrado correlación con la pérdida de campo visual en pacientes con glaucoma.
CAMBIOS ESTRUCTURALES
Cámara anterior estrecha:
Es frecuente en los glaucomas de ángulo cerrado y su presencia di culta técnicamente el procedimiento quirúrgico de catarata, pero no es un factor que debe condicionar nuestra de- cisión sobre qué lente implantar.
Ante una asimetría de la profundidad de la cámara anterior entre ambos ojos se debe des- cartar desinserción zonular y, en tal caso, no sería recomendable implantar una LIO para corrección de visión cercana por el riesgo de descentramiento.
Debilidad zonular:
Frecuente en los pacientes con glaucoma y pseudoexfoliación. Estos no son pacientes óp- timos para el implante de una lente premium, ya que el comportamiento del saco capsular a futuro es impredecible, con un gran riesgo de subluxación o luxación a largo plazo.
 Pupila e iris:
Pupila e iris:
La pupila del paciente con glaucoma presenta en muchas ocasiones una mala dilatación debido al uso de mióticos, la presencia de sinequias y patologías asociadas, como la pseudoexfoliación y disgenesias del segmento anterior, o puede existir una alteración en la funcionalidad del iris y atro a del esfínter pupilar en pacientes con episodios previos de cierre angular. La escasa dilatación di culta técnicamente la cirugía y puede condicionar el rendimiento funcional de una lente intraocular para corrección de visión cercana, ya que hay lentes pupilo-dependientes, como las multifocales refractivas, que no deberíamos implantar en caso de pupilas pequeñas.
Otro aspecto importante a considerar es en lo que el implante de la lente pueda in uir en el seguimiento del paciente glaucomatoso en cuanto a las pruebas de evaluación del nervio óptico y campo visual.
En lo que al campo visual se re ere, debido al posible cambio en la sensibilidad al contraste, es recomendable realizar uno nuevo tras el implante de las lentes para así disponer de un nuevo nivel de referencia para el seguimiento del paciente. Existe un estudio donde se demuestra el efecto de disminución de la sensibilidad en el campo visual de hasta 2 dB con perimetría estándar en pacientes con LIO multi- focal comparado con pacientes fáquicos18, y de 0.8 dB comparado con el grupo de lente intraocular monofocal.
En cuanto a las técnicas de imagen que evalúan el nervio óptico y la capa de – bras nerviosas, no se conoce muy bien la in uencia de las LIO multifocales sobre las mediciones, pero igualmente se recomienda un nuevo estudio tras la cirugía para obtener un nuevo nivel de comparación para el seguimiento del paciente.
Entonces, el candidato ideal para una lente multifocal sería aquel altamente motivado y con catarata que desee menor dependencia del uso de ante- ojos para visión cercana. Desafortunadamente hay poca publicación xfoliación debido al potencial riesgo de subsobre el uso de estas lentes en pacientes con glaucoma11,12, siendo la mayor experiencia anecdótica. Por lo tanto, la decisión de implantar o no una lente multifocal en un paciente glaucomatoso debe tomarse de forma individualizada. La clave en esta decisión está en encontrar el equilibrio entre la disminución de la sensibilidad al contraste debido al glaucoma y a la lente y la mejora de la calidad de vida que esperamos generar en el paciente.
Como se mencionó previamente, las llamadas lentes premium incluyen diferentes tipos, cada una con sus respectivas ventajas y desventajas. En este artículo mencionaremos algunas de ellas, en especial las tóricas, las asféricas y las multifocales, refractivas y difractivas. De estas últimas, prestaremos especial atención a las de rango de visión extendida.
Las lentes intraoculares tóricas nacen en 1992 para la corrección del astigmatismo, cuentan con una superficie más curva en un eje que en otro y sus meridianos principales forman entre sí un eje de 90 grados. Este tipo de LIO puede ser usado en pacientes con glaucoma, incluso en glaucomas severos en los cuales no hay compromiso de la visión central, pero no debe ser utilizado cuando se va a hacer una cirugía combinada de catarata con cirugía ltrante convencional de glaucoma, ya que el astigmatismo corneal posoperatorio es impredecible en estos casos, aunque sí podría usarse en combinación con MIGS (cirugía mínimamente inva- siva de glaucoma), ya que no tendrían ningún efecto sobre el astigmatismo. Es discutible si debe ser utilizado en los casos de pseudoeluxación y descentramiento.
Las lentes intraoculares asféricas se diseña- ron con la idea de compensar la aberración esférica positiva de la córnea y así conseguir una mejoría de la sensibilidad al contraste. Según estudios, se estima que la aberración corneal media de la población normal es de +0.27 μm para una pupila de 6 mm. Esta no varía signi cativamente con la edad y es compensada en las personas jóvenes por la aberración esférica negativa del cristalino, pero a medida que avanza la edad, el cristalino experimenta una disminución de su aberración esférica negativa, alcanzando valores cercanos a cero hacia los 40 años. De ahí en adelante tiende a tornarse positiva, con lo cual tiende a disminuir la sensibilidad al contraste.
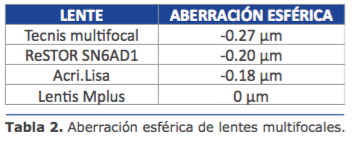 La primera LIO asférica fue comercializada en el año 2002. En la actualidad las hay con per l de asfericidad nulo y con per l asférico negativo, en aras de lograr mejoría signi cativa en la sensibilidad al contraste y disminuir los fenómenos disfotópsicos, como glare y halos. Adicionalmente se les han añadido cualidades de multifocalidad y/o toricidad.
La primera LIO asférica fue comercializada en el año 2002. En la actualidad las hay con per l de asfericidad nulo y con per l asférico negativo, en aras de lograr mejoría signi cativa en la sensibilidad al contraste y disminuir los fenómenos disfotópsicos, como glare y halos. Adicionalmente se les han añadido cualidades de multifocalidad y/o toricidad.
Las lentes multifocales se introdujeron por primera vez en la década de 1980. Tienen dos o más puntos focales y se basan en el principio de visión simultánea. Esto signi ca queunaimagenesproyectadasobrelaretina de forma nítida y la otra, borrosa simultáneamente, siendo el paciente capaz de suprimir la imagen borrosa y ver solo la nítida. Actualmente las hay de tipo refractivo, que proporcionan una muy buena agudeza lejana e intermedia, pero son dependientes del diámetro pupilar y de tipo difractivas,
que son independientes del diámetro de la pupila y proveen excelente agudeza visual cercana y lejana. Ambos tipos de lentes multifocales tienen el inconveniente que disminuyen la sensibilidad al contraste y pueden causar halos alrededor de las luces por la noche. La disminución del contraste puede ser considerable y llegar a ser hasta de un 50 %, reduciendo de manera importante la calidad de la imagen que se forma en la retina3,4.
Dentro de las lentes difractivas encontramos a las lentes de rango de visión ex- tendida, que proporcionan un patrón de difracción de la luz que alarga el foco en el ojo, dando lugar al llamado rango de visión extendida por su diseño echelette y poseen tecnología acromática que corrige la aberración cromática para mejorar la sensibilidad al contraste.
La aberración cromática ocurre cuando la luz blanca se separa en sus componentes espectrales (diferentes colores) y la longitud de onda de cada uno de los colores hace que éstos se refracten de manera diferente, creando varios puntos focales que generan dispersión y desenfoque. Cuanto más alto sea el número ABBE del LIO, hay menos dispersión y se genera menos desenfoque, lo que va a dar como resultado una imagen de mejor calidad.
El ojo fáquico tiene aproximadamente 1.38 D de aberración cromática entre longitudes de onda de 450 y 700 nm1. Los ojos pseudofáquicos tienen entre 1.45 y 2 D de aberración cromática, según la dispersión del material de la LIO17.
Las lentes de rango de visión extendida actúan invirtiendo los puntos de enfoque del color rojo y el azul, y de esta manera es que logran disminuir la aberración cromática y mejorar el contraste en la visión de los pacientes.
Teniendo en cuenta lo descrito anterior- mente, los pacientes con glaucoma sí podrían optar por el beneficio de usar lentes intraoculares premium, en especial aquellos que corrijan la aberración esférica y activamente la aberración cromática y que así mismo disminuyan los fenómenos disfotópsicos, halos alrededor de las luces y glare, como lo hacen las lentes de rango de visión extendida. Por último, nuestra recomendación en aquellos que quieren mejor visión cercana, sería dejar el ojo no dominante en -0.50 dioptrías y en el ojo dominante buscar el target a plano. En el caso del lente con rango de visión extendida, el paciente ideal para este tipo de LIO es aquel con catarata y glaucoma que se conforme con una visión cercana útil y que esté altamente “MOTIVADO” en co- rregir las diferentes distancias de visión.
Bibliografía
- Calladine D, Evans JR, Shah S, Leyland M. Multifocal versus monofocal intraocular lenses after cataract ex- traction. Cochrane Database Syst Rev 2012; (9).
- Anton A, Böhringer D, Bach M, Reinhard T, Birnbaum F. Contrast sensitivity with bifocal intraocular lenses is halved, as measured with the Freiburg Vision Test (FrACT), yet patients are happy. Graefes Arch Clin Exp Ophthalmol 2014; 252:539–544.
- Owsley C, Stalvey BT, Wells J, Sloane ME, McGwinG Jr. Visual risk factors for crash involvement in ol- der drivers with cataract. Arch Ophthalmol 2001; 119:881–887.
- McGwin G Jr, Chapman V, Owsley C. Visual risk factors for driving dif culty among older drivers. Accid Anal Prev 2000; 32:735–744.
- Libro Catarata y Glaucoma de la Secoir 2012; Cap 48:314-325.
- Hawkins AS, Szlyk JP, Ardickas Z, et al. Comparison of Contrast sensitivity, visual acuity and Humphrey visual eld testing in patients with glaucoma. L Glau- coma 2003; 12: 134-8.
- Stamper RL. Psycophysical changes in glaucoma. Surv Ophthalmol 1989; 33: 309-18.
- Stifter E, Sacu S, Thaler A, Weghaut S. Con- trast acuity in cataract of different morphology and association to self-reported visual function. Invest Ophthalmol Vis Sci 2006; 47:5412-22.
- McKendrick AM, Sampson GP, Walland MJ, Badcock DR. Contrast sensitivity changes due to glaucoma and normal aging: low-spatial- frequency losses in both magnocellular and parvocellular pathways. Invest Ophthalmol Vis Sci. 2007; 48(5):2115-2122.
- Aychoua N, Montolio FGJ, Jansonius NM. In- uence of multifocal intraocular lenses on stan- dard automated perimetry test results. JAMA Ophthalmol. 2013; 131(4):481-485.
- Kumar BV, Phillips RP, Prasad S. Multifocal in- traocular lenses in the setting of glaucoma. Curr Opin Ophthalmol. 2007; 18:62-68.
- Teichman JC, Ahmed IIK. Intraocular lens choices for patients with glaucoma. Curr Opin Ophthalmol. 2010; 21:135-143.
- Souza CE, Mucciolli C, Soriano ES, et al. Vi- sual performance of AcrySof apodized diffrac- tive IOL: a prospective comparative trial. Am J Ophthalmol. 2006; 141: 827-832.
- Vingolo EM, Grenga P, Iacobelli L, Grenga R. Visual acuity and contrast sensitivity: AcrySof Restor apodized diffractive versus AcrySof SA- 60AT monofocal intraocular lenses. J Cataract Refract Surg. 2007;33(7):1244-1247.
- Artal P, Manzanera S, Piers P, Weeber H. Visual effect of the combined correction of spherical and longitudinal chromatic aberrations. Optics Express 1637 18 January 2010 / Vol. 18, No. 2.
- H. Zhao, M. Mainster. The effect of cromatic dispersión on pseudofakic optical performance. Br J Ophthalmology 2007; 91: 1225-1229
- Weber et al. Differences in Chromatic Aberra- tions of IOLs, ESCRS 2016.
- Mathai A, Thomas R, Braganza A, et al. Vistech contrast sensitivity testing in prymary open angle glaucoma. Indian J Ophthalmol 1997; 45:99-103.
- Ruiz R. Óptica para el cirujano faco-refractivo. Elsevier España. Ed 1ra. 2015
- Iancu R, Corbu C. Premium intraocular lenses use in patients with cataract and concurrent glaucoma: a review. Maedica (Buchar). 2013; 8(3):290-296.
- Ichhpujani P, Bhartiya S, Sharma A. Premium IOLs in Glaucoma. Journal of Current Glauco- ma Practice 2013; 7(2):54-57.
-




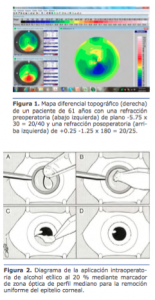 3. La ablación guiada por topografía no solo tiene la ventaja de contar
3. La ablación guiada por topografía no solo tiene la ventaja de contar
 En SMILE hacemos un procedimiento realmente intraestromal, mínimamente invasivo, no hay duda de que se res- peta de una mejor manera la biomecánica corneal2, comparada con los otros procedimientos y haciendo tratamientos por debajo de 140 micras, respetamos mucho más el plexo nervioso de la córnea. Se logra el menor daño posible utilizando un solo equipo alta- mente preciso, que requiere mucho me- nos mantenimiento o condiciones ambientales menos estrictas de sala que el láser excimer. Con SMILE, además, podemos corregir miopía y astigmatismo muy por arriba del rango que frecuentemente vemos, con la posibilidad de corregir hasta 10 dioptrías de miopía y 5 dioptrías de astigmatismo.
En SMILE hacemos un procedimiento realmente intraestromal, mínimamente invasivo, no hay duda de que se res- peta de una mejor manera la biomecánica corneal2, comparada con los otros procedimientos y haciendo tratamientos por debajo de 140 micras, respetamos mucho más el plexo nervioso de la córnea. Se logra el menor daño posible utilizando un solo equipo alta- mente preciso, que requiere mucho me- nos mantenimiento o condiciones ambientales menos estrictas de sala que el láser excimer. Con SMILE, además, podemos corregir miopía y astigmatismo muy por arriba del rango que frecuentemente vemos, con la posibilidad de corregir hasta 10 dioptrías de miopía y 5 dioptrías de astigmatismo.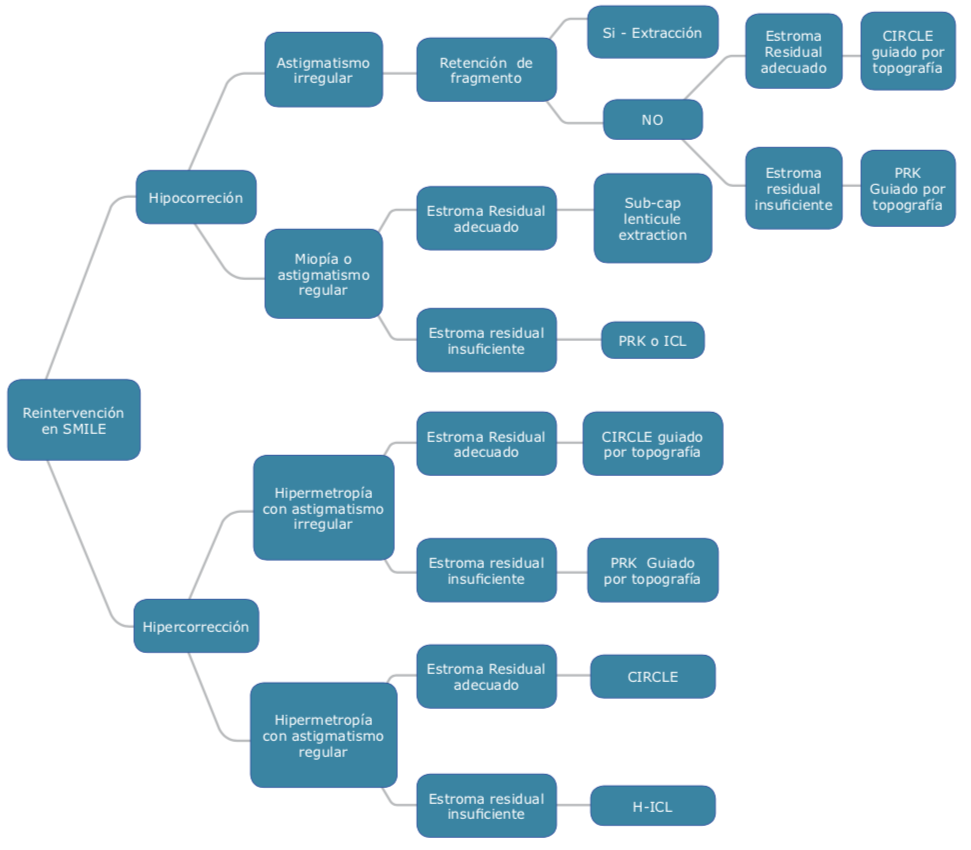 Dr. Claudio Orlich: Existe una tendencia a hipocorregir el cilindro en la mayoría de los estudios9, esto asociado a varios factores. Para mí, el más importante es la ciclo- torsión. A todos los casos con astigmatismo de 0.75 D o más los marco en la lámpara de hendidura con una aguja con tinta a las III y IX, y una vez realizada la succión, roto la interfase para que la retícula del equipo coincida con las marcas de la córnea. Esta compensación me ha permitido mejorar mucho la corrección del cilindro y alcanzar resultados similares al LASIK. En general los mejores resultados los obtengo en miopías con astigmatismos menores que la esfera. En cilindros irregulares, astigmatismos mixtos o cilindros muy altos con poca miopía, prefiero realizar un LASIK guiado por topografía.
Dr. Claudio Orlich: Existe una tendencia a hipocorregir el cilindro en la mayoría de los estudios9, esto asociado a varios factores. Para mí, el más importante es la ciclo- torsión. A todos los casos con astigmatismo de 0.75 D o más los marco en la lámpara de hendidura con una aguja con tinta a las III y IX, y una vez realizada la succión, roto la interfase para que la retícula del equipo coincida con las marcas de la córnea. Esta compensación me ha permitido mejorar mucho la corrección del cilindro y alcanzar resultados similares al LASIK. En general los mejores resultados los obtengo en miopías con astigmatismos menores que la esfera. En cilindros irregulares, astigmatismos mixtos o cilindros muy altos con poca miopía, prefiero realizar un LASIK guiado por topografía.
 Los parámetros de seguridad son los mismos que para LASIK, en cuanto a regularidad topográfica y limitaciones paquimétricas.
Los parámetros de seguridad son los mismos que para LASIK, en cuanto a regularidad topográfica y limitaciones paquimétricas.
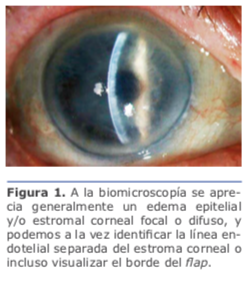 Hay factores previos que aumentan las probabilidades de producir iatrogénicamente un desprendimiento de la MD, como las cámaras planas, córneas edematosas e hipotonía.5
Hay factores previos que aumentan las probabilidades de producir iatrogénicamente un desprendimiento de la MD, como las cámaras planas, córneas edematosas e hipotonía.5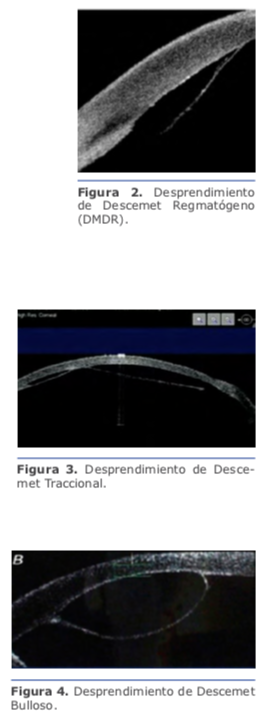 Clasificación
Clasificación Manejo del desprendimiento de MD
Manejo del desprendimiento de MD
 Dr. Alfonso Arias Puente: La mejor solución para evitar o, en su caso, romper el síndrome de retropulsión iri- diana es asegurar fluido debajo del iris que iguale la presión en ambas cámaras. Esto se consigue evitando presiones bruscas e inten- sas sobre el cristalino en el momento de intro- ducir irrigación en la cámara anterior.
Dr. Alfonso Arias Puente: La mejor solución para evitar o, en su caso, romper el síndrome de retropulsión iri- diana es asegurar fluido debajo del iris que iguale la presión en ambas cámaras. Esto se consigue evitando presiones bruscas e inten- sas sobre el cristalino en el momento de intro- ducir irrigación en la cámara anterior.
 Caso clínico
Caso clínico Dr. Nicolás Fernández Meijide: La tomografía muestra un encurvamiento inferior símil «pelúcida» (sin serlo) con astigmatismo central en contra de la regla que coincide con su refracción. Para poder dar más objetividad al análisis refractivo, sería bueno contar con dos topografías separadas en el tiempo, lo que descartaría o confirmaría la participación corneal en el cambio refractivo (recordar que a veces el cambio refractivo se relaciona con cambios cristalinianos, de tipo esclerosis o catarata nuclear, aunque esto más frecuentemente vira hacia la miopía pura que hacia al astigmatismo).
Dr. Nicolás Fernández Meijide: La tomografía muestra un encurvamiento inferior símil «pelúcida» (sin serlo) con astigmatismo central en contra de la regla que coincide con su refracción. Para poder dar más objetividad al análisis refractivo, sería bueno contar con dos topografías separadas en el tiempo, lo que descartaría o confirmaría la participación corneal en el cambio refractivo (recordar que a veces el cambio refractivo se relaciona con cambios cristalinianos, de tipo esclerosis o catarata nuclear, aunque esto más frecuentemente vira hacia la miopía pura que hacia al astigmatismo).

 Preguntas del caso:
Preguntas del caso: 2.¿Tomando en cuenta que la mejor agudeza visual corregida no mejora más de 20⁄100 OD y 20⁄150 OI, tomaría una conducta quirúrgica?
2.¿Tomando en cuenta que la mejor agudeza visual corregida no mejora más de 20⁄100 OD y 20⁄150 OI, tomaría una conducta quirúrgica? 3.¿Qué abordaje quirúrgico realizaría en cada ojo y por qué? Describir técnica quirúrgica.
3.¿Qué abordaje quirúrgico realizaría en cada ojo y por qué? Describir técnica quirúrgica. En mi caso, y dado que soy cirujano de segmento anterior, optaría por este abordaje, aunque sometería el caso también a la con- sideración del retinólogo ante una eventual complicación intraoperatoria.
En mi caso, y dado que soy cirujano de segmento anterior, optaría por este abordaje, aunque sometería el caso también a la con- sideración del retinólogo ante una eventual complicación intraoperatoria.
 Parece muy posible que la mejor opción en profilaxis de endoftalmitis sea la combinación de agentes que eliminen gérmenes de la superficie ocular, antibióticos (quinolonas de cuarta generación) sumada al uso de antisépticos (cloruro de benzalconio, yodopovidona) más inyección de antibióticos en la cámara anterior.8-11
Parece muy posible que la mejor opción en profilaxis de endoftalmitis sea la combinación de agentes que eliminen gérmenes de la superficie ocular, antibióticos (quinolonas de cuarta generación) sumada al uso de antisépticos (cloruro de benzalconio, yodopovidona) más inyección de antibióticos en la cámara anterior.8-11
 2. Indicaciones para la fijación escleral de lentes intraoculares
2. Indicaciones para la fijación escleral de lentes intraoculares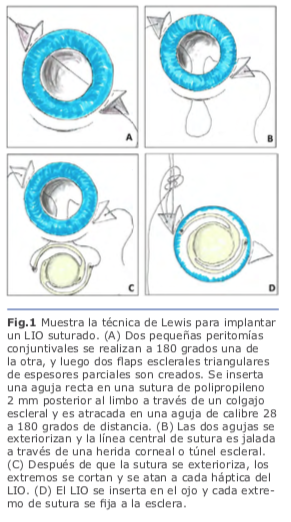 3. Técnicas de fijación escleral
3. Técnicas de fijación escleral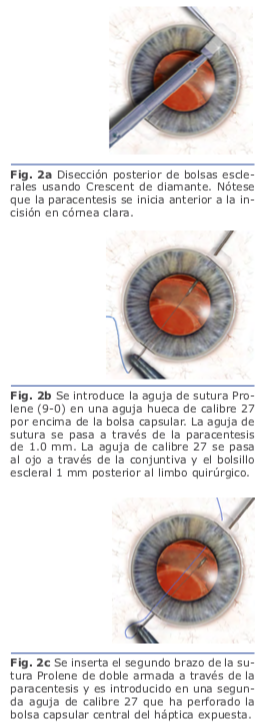 En 1991, Lewis popularizó el concepto de pases de sutura ab externo con el uso de flaps esclerales para cubrir los nudos de sutura. Presentó el concepto de introducir la aguja de la sutura de polipropileno 10-0 dentro del lumen de una aguja calibre 28g que penetra el globo ocular a 180 grados de distancia de la entrada de la aguja de la sutura. Los puntos de entrada para ambas agujas son medidas a 2 mm por detrás del limbo, lo que, da una posición final de LIO más reproducible en el surco ciliar en comparación con enfoques ab internos. La sutura atraviesa el ojo de surco a surco, y después de que fue externalizado con el uso de un segundo instrumento (gancho de Sinsky) insertado a través de una herida corneal, se corta la sutura a la mitad de ésta, y se fijan a las hápticas del LIO; posteriormente se introduce el lente al interior del globo ocular posicionándolo detrás del iris con las hápticas descansando en el surco ciliar2. Fig. 1
En 1991, Lewis popularizó el concepto de pases de sutura ab externo con el uso de flaps esclerales para cubrir los nudos de sutura. Presentó el concepto de introducir la aguja de la sutura de polipropileno 10-0 dentro del lumen de una aguja calibre 28g que penetra el globo ocular a 180 grados de distancia de la entrada de la aguja de la sutura. Los puntos de entrada para ambas agujas son medidas a 2 mm por detrás del limbo, lo que, da una posición final de LIO más reproducible en el surco ciliar en comparación con enfoques ab internos. La sutura atraviesa el ojo de surco a surco, y después de que fue externalizado con el uso de un segundo instrumento (gancho de Sinsky) insertado a través de una herida corneal, se corta la sutura a la mitad de ésta, y se fijan a las hápticas del LIO; posteriormente se introduce el lente al interior del globo ocular posicionándolo detrás del iris con las hápticas descansando en el surco ciliar2. Fig. 1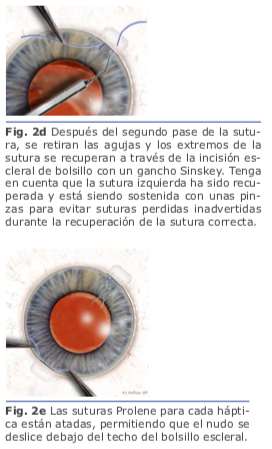 En la fijación escleral sin suturas, las hápticas del LIO se exteriorizan y se fijan dentro de la esclera mediante el uso de flaps o túneles esclerales paralelos al limbo. Una de las ventajas es que se usan lentes de tres piezas sin diseño especial.
En la fijación escleral sin suturas, las hápticas del LIO se exteriorizan y se fijan dentro de la esclera mediante el uso de flaps o túneles esclerales paralelos al limbo. Una de las ventajas es que se usan lentes de tres piezas sin diseño especial.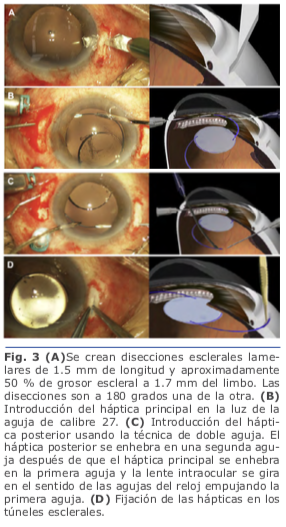 Se realizan los túneles paralelos al limbo de 2 mm de longitud con la aguja de calibre 27 en el final de la disección escleral lame- lar frente a las esclerotomías. Se insertan las hápticas en los túneles de 1.5 mm, y se centra la posición del LIO. Se realiza una iri- dotomía periférica utilizando el cortador de vitrectomía para evitar la captura por el iris del LIO. Se extrae la cánula de infusión, y todos los sitios de esclerotomía se inspeccionan por fugas de heridas3.
Se realizan los túneles paralelos al limbo de 2 mm de longitud con la aguja de calibre 27 en el final de la disección escleral lame- lar frente a las esclerotomías. Se insertan las hápticas en los túneles de 1.5 mm, y se centra la posición del LIO. Se realiza una iri- dotomía periférica utilizando el cortador de vitrectomía para evitar la captura por el iris del LIO. Se extrae la cánula de infusión, y todos los sitios de esclerotomía se inspeccionan por fugas de heridas3.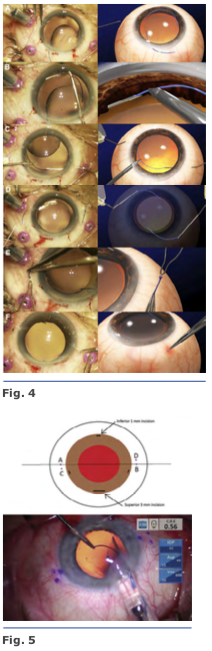 Se realizan una incisión limbal inferior de 1.0mm en el meridianode las VI, III, IX y una superior de 3.0 mm. El LIO se inserta a través de la incisión superior usando un inyector. El ayudante avanza el émbolo, mientras que el cirujano sostiene el eje del inyec- tor. Al ir emergiendo el háptica del inyector, el cirujano coloca un microfórceps calibre 23 a través de la incisión inferior (meridiano VI) para tomar la punta del háptica principal4. Fig. 5
Se realizan una incisión limbal inferior de 1.0mm en el meridianode las VI, III, IX y una superior de 3.0 mm. El LIO se inserta a través de la incisión superior usando un inyector. El ayudante avanza el émbolo, mientras que el cirujano sostiene el eje del inyec- tor. Al ir emergiendo el háptica del inyector, el cirujano coloca un microfórceps calibre 23 a través de la incisión inferior (meridiano VI) para tomar la punta del háptica principal4. Fig. 5