Editorial Catarata: Trabajo comparativo entre las técnicas ablativas de superficie, PRK y TransPRK

Dr. Ándres Giobellina
Las ablaciones de superficie se realizan para tratar ametropías leves a moderadas en pacientes con córneas delgadas. El dolor postoperatorio es uno de los principales efectos adversos de ambas técnicas.
Objetivo: Comparar las técnicas PRK y TransPRK en un mismo paciente, valorando resultados refractivos, dolor postoperatorio y efectos adversos.
Material y métodos: Estudio comparativo, prospectivo de una serie de casos donde se estudiaron 15 individuos (30 ojos) y se les realizó en OD PRK y TransPRK en ojo contralateral.
Resultados: En AV postquirúrgica no se observó diferencias entre ambos procedimientos. En cuanto al dolor postquirúrgico inmediato, hubo un aumento significativo en pacientes intervenidos con TransPRK.
Conclusión: Este estudio refleja que ambas técnicas quirúrgicas, PRK y TransPRK, han demostrado excelentes resultados tanto en estabilidad refractiva como tolerancia al dolor a largo plazo. La PRK convencional ofrece mayor ventaja al paciente en cuanto a menor dolor en el postoperatorio inmediato.
Introducción
La queratectomía fotorrefractiva (PRK) fue descrita por primera vez en 1983 por Trokel y colaboradores en ojos de vacas (1). Pero fue en el año 1987 cuando pudo realizarse de forma segura en humanos con una recuperación relativamente normal. La queratectomía fotorrefractiva transepitelial (transPRK) apareció en los años 90 como alternativa a la PRK convencional.
Las ablaciones de superficie (PRK y transPRK) se mantienen vigentes como prácticas frecuentes del cirujano refractivo, ya que permiten tratar con seguridad córneas delgadas o irregulares y preservan su integridad.
Material y métodos
Se realizó un estudio comparativo, prospectivo de una serie de casos. Los pacientes intervenidos de PRK convencional (ojo derecho) así como de trans PRK (ojo izquierdo) fueron 15 individuos sin antecedentes patológicos (30 ojos), adultos jóvenes ( entre 19 y 42 años) , sin cirugía previa, con ametropías leves a moderadas, anisometropías menores a 1,75D y paquimetrias mayores a 480 micras. Los mismos fueron evaluados en el Servicio Cirugía Refractiva de la Clínica de Ojos Reyes- Giobellina de la provincia de Córdoba – Argentina, durante los meses de marzo de 2024 a enero de 2025.
En OD se realiza la técnica de PRK, para la remoción del epitelio se utiliza alcohol etílico al 50% durante 20 segundos.
En OI se realiza la técnica de Trans PRK, el láser remueve el epitelio en un primer paso y luego la ablación refractiva.
En ambos grupos la zona óptica es de 6,5 mm. Se utilizó mitomicina C al 0.02% durante 10 segundos por dioptría ablacionada. Se instilo esteroides y antibiótico tópico y LC terapéutico.
El tiempo quirúrgico fue registrado y se utilizó la escala de dolor para graduarlo desde 0 (ausencia de dolor) a 10 (dolor insoportable).
El seguimiento se realizó a las 24 horas, 72 horas y a los 15 días post cirugía. primer día postoperatorio, tercero y finalmente a los quince días. La medicación utilizada fue 48 horas previas a la cirugía dexametasona fosfato sódico inyectable, 24 horas previas comenzaron con moxifloxacina y dexametasona tópica cada 4 horas por 15 días más diclofenaco una gota cada 4 horas por 3 días.
Resultados:
Agudeza visual
No se presentaron diferencias estadísticamente significativas en la agudeza visual postoperatorias entre ambos grupos (p=0.19)
Dolor
Se observó a las 24 horas postoperatorias, una diferencia significativa (p=0.02), donde hubo mayor dolor con el grupo de la TransPRK en relación con PRK. No obstante, no se observaron diferencias significativas entre ambos grupos a las 72 horas postoperatorias (p=0.07) y a día 15 (p=0.2) lo que indica que ambas técnicas tendrían efectos equivalentes sobre el dolor a largo plazo.
Complicaciones
No se encontraron efectos adversos hasta el momento tanto en PRK como en TransPRK, como haze, infecciones o retraso en la reepitelizacion.
Discusion
En el caso de la PRK convencional, la ablación láser se realiza en el estroma corneal, una vez que se ha removido mecánicamente el epitelio corneal, en la trans-PRK se realiza la remoción con el láser. La figura 1 y 2 ilustran ambas técnicas.
En la trans-PRK, el perfil de remoción se obtiene a partir de un valor de grosor epitelial de referencia. En el actual estudio tomamos 55 μm de grosor.
Diferentes autores se han pronunciado respecto a las diferencias de grosor epitelial a lo largo de la superficie corneal. Reinstein, et al.1 obtienen que la ubicación del epitelio más delgado se encuentra algo desplazado temporalmente (0.33 mm) y hacia la córnea superior (0.90 mm), muestran un grosor epitelial medio de 53.4 ± 4.6 μm en el vértice corneal utilizando ecografía digital de muy alta frecuencia..
Kanellopoulos, et al.2 y Sin, et al 3 han seguido esta línea de investigación con el empleo de tomografía de coherencia óptica del segmento anterior de dominio espectral y concluyen que no se puede aseverar que el mapa de grosor del epitelio sea simétrico.
Luger, et al.4 realizaron un estudio donde en el mismo paciente se operaba un ojo con trans-PRK y el ojo contralateral con PRK convencional, con el láser Amaris (Schwind), en 33 pacientes con 1 año de seguimiento. No se obtuvieron diferencias significativas entre ambas técnicas en términos de agudeza visual sin corrección. Igualmente, con la plataforma Amaris, Fadlallah, et al.5 obtuvieron parámetros de agudeza visual similares en ambas técnicas quirúrgicas. Aslanides, et al.6 realizaron un estudio en 30 pacientes utilizando una técnica en cada ojo, y obtuvieron valores similares de agudeza visual en ambos procedimientos..
Ortueta, et al.13, en un estudio más actual, concluyeron que la trans-PRK tiene resultados refractivos similares a las técnicas estromales, con menor posibilidad de complicaciones.
Constituye una ventaja de la trans-PRK la reducción del tiempo de cirugía. Kaluzny, et al.8 obtienen una reducción (35%) del tiempo quirúrgico en la trans-PRK comparado con PRK convencional.
Conclusión
Este estudio refleja que ambas técnicas quirúrgicas, PRK y TransPRK, realizadas en pacientes candidatos a cirugía refractiva han demostrado excelentes resultados tanto en estabilidad refractiva como tolerancia al dolor a largo plazo. La PRK convencional ofrece mayor ventaja al paciente en cuanto a menor dolor en el postoperatorio inmediato.

Figura 1: Procedimiento de PRK
Figura 2: Procediemiento de TransPRK
Referencias
Reinstein DZ, Archer TJ, Gobbe M, Silverman RH, Coleman DJ. Epithelial thickness in the normal cornea:three-dimensional display with Artemis very high-frequency digital ultrasound. J Refract Surg. 2008;24:571-81.
Kanellopoulos AJ, Asimellis G. In vivo three-dimensional corneal epithelium imaging in normal eyes by anterior-segment optical coherence tomography:a clinical reference study. Cornea. 2013;32:1493-8.
Sin S, Simpson TL. The repeatability of corneal and corneal epithelial thickness measurements using optical coherence tomography. Optom Vis Sci. 2006;83:360-5.
Luger MH, Ewering T, Arba-Mosquera S. Consecutive myopia correction with transepithelial versus alcohol-assisted photorefractive keratectomy in contralateral eyes:one-year results. J Cataract Refract Surg. 2012;38:1414-23.
Fadlallah A et al. Transepithelial photorefractive keratectomy: clinical results. J Cataract Refract Surg 2011; 37: 1852-7.
Aslanides IM, Padroni S, Arba Mosquera S, Ioannides A, Mukherjee A. Comparison of single-step reverse transepithelial all-surface laser ablation (ASLA) to alcohol-assisted photorefractive keratectomy. Clin Ophthalmol. 2012;6:973-80.
Ortueta D, von Rüden D. Transepithelial photorefractive keratectomy:Results and clinical experiences. Ophthalmologe. 2019;116(6):534-
Kaluzny BJ, Szkulmowski M, Bukowska DM, Wojtkowski M. Spectral OCT with speckle contrast reduction for evaluation of the healing process after PRK and transepithelial PRK. Biomed Opt Express. 2014;5:1089-98.












 Dr. César Carriazo
Dr. César Carriazo Dr. Juan Manuel Paulín – México
Dr. Juan Manuel Paulín – México Dra. Bruna Ventura – Brasil
Dra. Bruna Ventura – Brasil


 Dr. Virgilio Centurion
Dr. Virgilio Centurion Dr. Claudio Orlich – Costa Rica
Dr. Claudio Orlich – Costa Rica Dr. Pablo Bonnano – Argentina
Dr. Pablo Bonnano – Argentina


 Dra. Bruna V. Ventura
Dra. Bruna V. Ventura Dr. Juan José Mura – Chile
Dr. Juan José Mura – Chile Dra. Marcela Pérez – Chile
Dra. Marcela Pérez – Chile


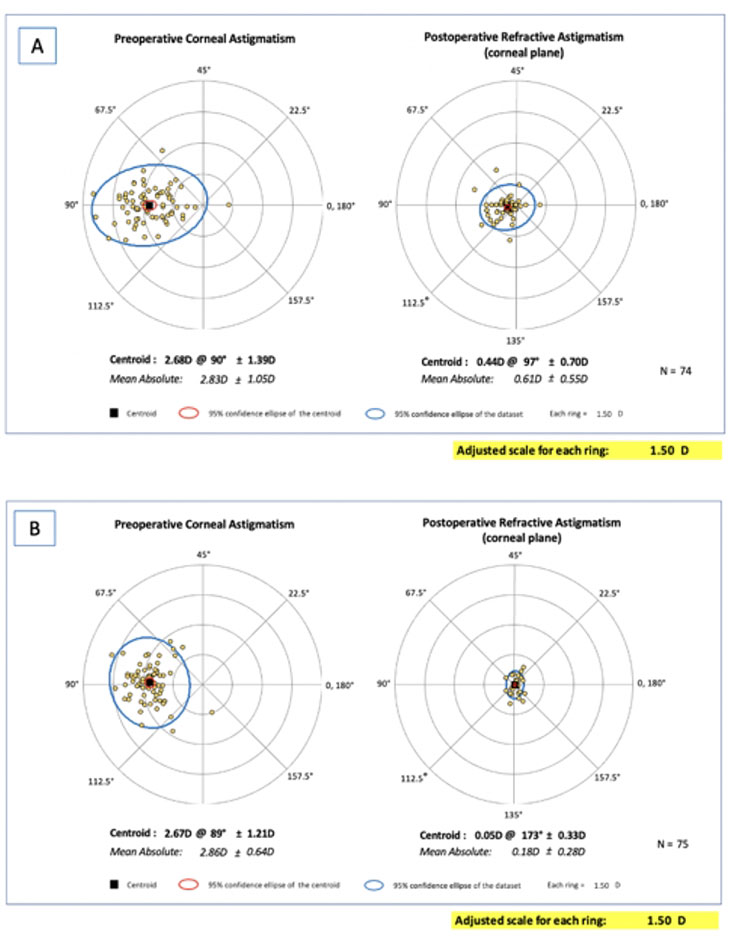 Fig 1. A) Double angle plot que muestra la distribución pre y post operatoria del astigmatismo refractivo, posterior a implante de ICL. B) Double angle plot que muestra la distribución pre y post operatoria del astigmatismo refractivo, posterior a la corrección con LASIK.
Fig 1. A) Double angle plot que muestra la distribución pre y post operatoria del astigmatismo refractivo, posterior a implante de ICL. B) Double angle plot que muestra la distribución pre y post operatoria del astigmatismo refractivo, posterior a la corrección con LASIK.