Novedades del
Congreso ESCRS 2021
Congreso ESCRS 2021: una apuesta inequívoca del Board de
la ESCRS para convertirse en el Congreso más influyente a
nivel global dirigido a cirujanos de polo anterior.
Joaquín Fernández España
joaquinfernandezoft@Qvision.es
Sidi Mohamed Hamida Abdelkader España
smha.ard@gmail.com
Manuel Rodríguez-Vallejo España
manuelrodriguezid@Qvision.es
El primer congreso presencial de la and Refractive Surgeons do recientemente en Amster dam (Países Bajos) ha supuesto una apuesta inequívoca por par European Society of Cataract celebrate del Board de la ESCRS para convertirse en el
Congreso más influyente a nivel global dirigido a cirujanos de polo anterior. El difícil equilibrio que siempre supone albergar espacios para la innovación de la industria junto con unos main simposium lo menos influenciados posibles por conflictos de interés en el que estén representados los autores de artículos científicos publicados más significados en el año, han sido aval suficiente para que este congreso se convierta en lo sucesivo, en cita obligada para cirujanos de polo anterior de todo el mundo, por ser probablemente el más confiable de los que se dan cita en la agenda congresista de las sub-especialidades tratadas.
Del 8 al 11 de octubre del 2021 tuvo lugar el 39º congreso de la European Society of Cataract and Refractive Surgeons en Amsterdam (Países Bajos), que debía haberse celebrado el año pasado pero fue suspendido por la pandemia COVID-19.
Recién aterrizados en Almería (España) os elaboramos este resumen exprés intentando analizar las innovaciones más destacadas que nos permitan identificar las tendencias de los departamentos de I+D de la industria, junto con la evidencia más sólida que pueda ayudarnos a la toma de decisiones en las diferentes áreas de nuestra práctica diaria.
CATARATAS/PRESBICIA:
INNOVACIÓN:
En la industria se puede identificar una tendencia al lanzamiento al mercado de LIOs de tipo EDOF y Mono-EDOF, de las que muchas de ellas solamente podemos contar, en algunos casos, con publicaciones de resultados en banco óptico y series de casos presentados por algunos colegas en el congreso. Os adjunto tabla actualizada a octubre 2021 de LIOs Premium (Figura 1).
No es infrecuente volver a encontrarnos estrategias de implante en algunos free papers en mix&match con LIOs EDOF o Mono-EDOF en el ojo dominante y Trifocales en el no dominante. El tiempo y la evidencia nos reportará si esta estrategia nos aporta mayor satisfacción percibida por parte de los pacientes.
EVIDENCIA:
La ESCRS Binkhorst Medal Lecture impartida por Gerd Auffarth, con el sugerente título de “There is no free lunch in optics” vino a desmitificar ciertos mensajes marketinianos detallando el compromiso en términos de MTF y PSF en banco óptico, que tendría traducción en clínica en sensibilidad al contraste y disfotopsias, que supone cualquier tratamiento que intente incrementar la profundidad de campo en nuestros pacientes. Cada profilometría puede intentar balancear este delicado equilibrio entre profundidad de campo, sensibilidad al contraste y disfotopsias, pero debemos ser conscientes de las limitaciones de cada tecnología y sus criterios de inclusión y exclusión. En esa línea tuvimos el honor de ser invitados por el Board para presentar en el main simposium sobre LIOs Multifocales la ponencia “From optical bench to clinical reality”.
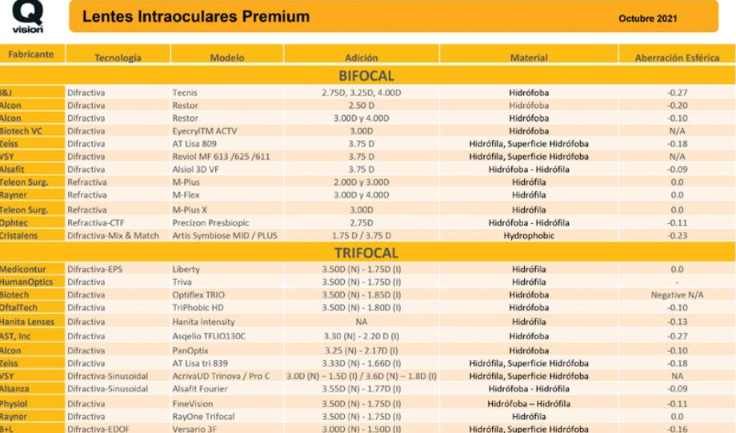
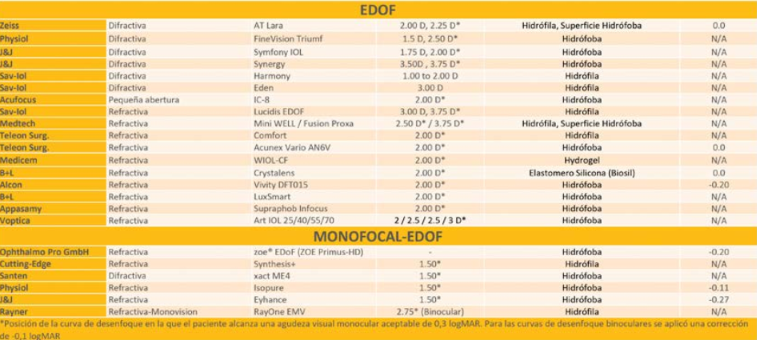 Figura 1. Actualización Lentes Intraoculares Premium (Octubre 2021)
Figura 1. Actualización Lentes Intraoculares Premium (Octubre 2021)
En cuanto a cálculo de LIOs tuvimos un espectacular simposium realizado por el “IOL Power Club” en el que participaron Filomena Ribeiro, Jaime Aramberri, Giacomo Savini y Thomas Olsen en el que nos actualizaron el estado del arte del
cálculo de LIOs basado en la evidencia publicada en el último año. *No hemos vuelto a tener noticias destacables de
la técnica FLACS (Femtosecond Laser Assisted Cataract Surgery) ni en Innovación ni en Evidencia.
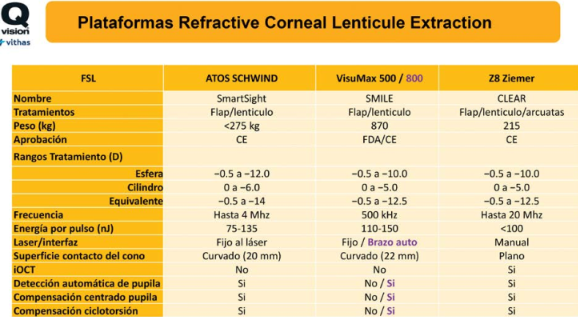
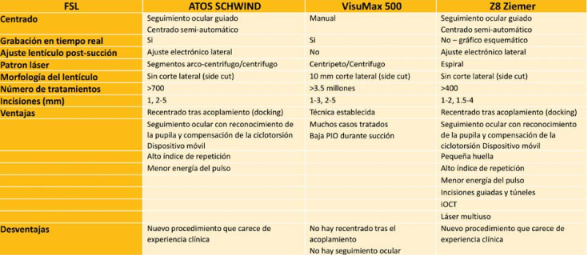
Figura 2. Nuevas Plataformas de Refractive Corneal Lenticule Extraction
CIRUGÍA REFRACTIVA:
INNOVACIÓN:
Nuevas plataformas de Refractive Corneal Lenticule Extraction han sido presentadas en el congreso por parte de Zeiss con el nuevo Visumax 800 con su técnica ReLex SMILE, el Z8 de Ziemer con la técnica CLEAR y el Atos de Schwind con la técnica SmartSight. En la Figura 2 resumimos las características, ventajas e inconvenientes de las 3 plataformas.
GLAUCOMA:
EVIDENCIA:
El main simposium sobre glaucoma de este año estuvo dedicado en exclusiva a una aproximación basada en evidencia a los implantes de MIGS (Minimally Invasive Glaucoma Surgery). Los ponentes del simposium seguirán recomendando las guías clínicas de la Sociedad Europea de Glaucoma en su 5º edición del 2020, que aconseja la trabeculectomía como 1ª opción quirúrgica para el GPAA (Glaucoma Primario Ángulo Abierto). La evidencia publicada recientemente reportaría mejores resultados de seguridad pero peores de eficacia a largo plazo de las técnicas MIGS frente a las bleb forming, por
lo tanto la indicación de MIGS quedaría restringida a etapas más precoces, intolerancia o mal seguimiento de la medicación tópica y combinación con cirugía de cataratas (en la que la cirugía combinada con trabeculectomía no daría tan buenos resultados). Es de destacar que las técnicas MIGS no comprometería los resultados de futuros procedimientos quirúrgicos.
En el simposium de JCRS (Journal of Cataract & Refractive Surgery), Guss Gazzard del Moorfields Eye Hospital nos presentó su protocolo de manejo que oferta como 1ª opción de tratamiento del GPAA la SLT (Trabeculoplastia Láser Selectiva) por los resultados de coste/efectividad de su estudio LiGHT (1); nos comentó que según 2 ensayos clínicos (2 y 3) los resultados de eficacia de la facoemulsificación aislada vs la facoemulsificación combinada con MIGS no difieren en exceso en términos de eficacia de control de PIO sin tratamiento médico adyuvante (50% vs 61% y 50% vs 72%) y resaltó el estudio COMPARE (4) que reporta mejores resultados de eficacia con Hydrus que con i-Stent (diferencia = 22.6% p =
0.0057) y similares de seguridad.
CÓRNEA:
INNOVACIÓN:
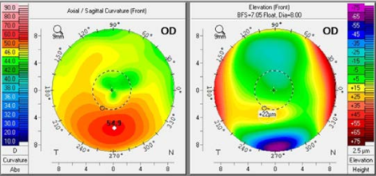
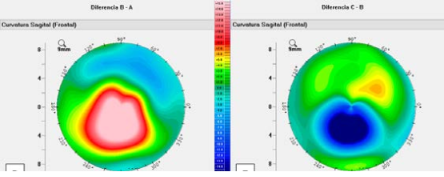
La sesión específica que el Board programó sobre biomecánica corneal y el lanzamiento de un nuevo software que combina Corvis y Pentacam para el seguimiento de la progresión del queratocono y de pacientes operados de cirugía refractiva láser corneal señala la probable tendencia como innovación en este área del conocimiento.
EVIDENCIA:
Las preguntas más controvertidas en cuanto al tratamiento con crosslinking del queratocono, ¿qué técnica presenta mejor balance de eficacia/ seguridad y cuándo debe tratarse el queratocono en la infancia, al diagnóstico o tras reporte de progresión (tal y como aconseja el estudio KERALINK (5) fueron tratadas en las sesiones de free papers, si bien se nos antoja que necesitamos mejores diseños de ensayos clínicos controlados aleatorizados que generen revisiones sistemáticas al respecto con menos sesgos y menor heterogeneidad.
MISCELÁNEA:
El Board quiso programar dos simposium específicos para ponencias sobre Valor-Salud y PROs (Patients Reported Outcomes) con una clara toma de posición sobre la importancia que le atribuye a estas dos áreas en el futuro de la atención asistencial. La impresión general que deja el congreso basado en cada uno de sus tipos de sesiones del programa como en la selección de presentaciones y ponentes es el de una apuesta inequívoca por parte del Board de la ESCRS para convertirse en el Congreso más influyente a nivel global dirigido a cirujanos de polo anterior. El difícil equilibrio que siempre supone albergar espacios para la innovación de la industria junto con unos main simposium lo menos influenciados posibles por conflictos de interés en el que estén representados los autores de artículos científicos publicados más significados en el año, han sido aval suficiente para que este congreso se convierta en lo sucesivo, en cita obligada para cirujanos de polo anterior de todo el mundo, por ser probablemente el más confiable de los que se dan cita en la agenda congresista de las sub-especialidades tratadas
REFERENCIAS
4. Iqbal Ike K. Ahmed, Antonio Fea, Leon Au, Robert E. Ang, Paul Harasymowycz, Henry D. Jampel, Thomas W. Samuelson, David F. Chang, Douglas J. Rhee, A Prospective Randomized Trial Comparing Hydrus and iStent Microinvasive Glaucoma Surgery Implants for Standalone Treatment of Open-Angle Glaucoma: The COMPARE Study, Ophthalmology, Volume 127, Issue 1, 2020, Pages 52-61, ISSN 0161-6420, https://doi. org/10.1016/j.ophtha.2019.04.034.
5. Larkin DFP, Chowdhury K, Burr JM, Raynor M, Edwards M, Tuft SJ, Bunce C, Caverly E, Doré C; KERALINK Trial Study Group. Effect of Corneal Cross-linking versus Standard Care on Keratoconus Progression in Young Patients: The KERALINK Randomized Controlled Trial. Ophthalmology. 2021 Apr 21:S0161- 6420(21)00297-9. doi: 10.1016/j.ophtha.2021.04.019. Epub ahead of print. PMID: 33892046.