Top Ten: Manejo de la Sorpresa Refractiva en Cirugía Implanto Refractiva

Dr. Ramón Ruíz
INTRODUCCIÓN
La cirugía de cristalino, dado los últimos avances contraídos tanto en diagnóstico y ejecución (avances en imagen ocular tanto en biómetros como en topógrafos y aberrómetros, diseños de lentes intraoculares, así como el perfeccionamiento de la técnica quirúrgica)(1)(2) va encaminada a la consecución, ya no sólo de la rehabilitación de la agudeza visual, sino de conseguirla sin apenas uso de ninguna prótesis tras la misma.
PREVENCIÓN
Aunque sean poco frecuentes, debemos obligarnos a explicar al paciente tal posibilidad y dejarlo constar en el consentimiento informado previo a la primera intervención, sobre todo en aquellos casos más susceptibles tales como ojos con longitud axial extrema, tras cirugía corneal (excimer o queratotomía radial), post vitrectomizados, etc).
Así mismo es importante el análisis de superficie así como de la tomografía para tener previsión de tener la posibilidad segura y abierta de un segundo procedimiento con láser excimer.
EXPLORACION BASICA
Lo primero será analizar la fecha de cuando fue realizada dicha cirugía así
como analizar si fuera posible los métodos y medios utilizados para el cálculo de la lente implantada y la refracción previa del paciente. Será de vital importancia investigar si se trata de una complicación pre o bien intra o postoperatoria.
Obviamente , debemos realizar una exhaustiva batería de pruebas que incluyan un estudio de su refracción y agudeza visual tanto espontánea como con su mejor corrección, así como toma de la presión intraocular en orden a descartar restos de viscoelástico aún en cámara anterior.
DIAGNÓSTICO DIFERENCIAL
Deberemos completar nuestra exploración con un examen minucioso en lámpara de hendidura, donde deberemos detallar y examinar con seguridad la presencia de las diferentes opciones:
Descartar ninguna complicación que fuera responsable del defecto visual refractivo: edema incisional, edema corneal, estabilidad de cámara con incisiones en buen estado, estado de la superficie corneal (en algunas ocasiones puede pasar desapercibido en el estudio preoperatorio la presencia de anomalías en la superficie corneal tal como la distrofia epitelial de la membrana basal (EBMD)(3), que nos puede llevar a la confusión de la etiología de tal sorpresa refractiva).
Evaluar bajo dilatación pupilar la situación de la lente intraocular implantada, si se encuentra en toda la totalidad su óptica dentro del saco capsular y centrada o no, si la capsulorrexis está completa, regular y centrada, en ausencia de contracción o fibrosis capsular, todos estos detalles son de suma importancia especialmente si hablamos de lentes multifocales y/o tóricas.
Realizar una OCT de segmento anterior con evaluación de la posición efectiva de la lente y descartando restos de viscoelástico retrolental lo cual nos puede inducir a un error de la refracción postoperatoria.
Revisar todo el estudio preoperatorio para que la causa que el error haya sido previo a la cirugía: los cálculos biométricos realizados y contrastar si: se eligió adecuadamente la fórmula a emplear, la lente a implantar y si coincide la elección con el implante (4).
OPCIONES DE TRATAMIENTO
Lo primero que debemos es evitar reincidir en posibles errores cometidos con anterioridad, para ellos debemos hacer un exhaustivo estudio de la superficie corneal en pos de si fuera necesaria abordar dicho estroma para solucionar el defecto residual remanente.
ALGORITMO
Dependiendo de la refracción resultante a tratar , podríamos seguir este algoritmo (1):
Equivalente esférico < 0.5 dioptrías ——-��� No cirugía
Equivalente esférico > 0.5 dioptrías a 3 dioptrías —-��� Cirugía ablacional excimer (superficie o Lasik)
Equivalente esférico > 3 dioptrías —-��� Cirugía lenticular endocular (intercambio o piggy back)
OPCIÓN CON LÁSER EXCIMER
Los procedimientos ablativos con láser excimer estarían más recomendado tal como hemos comentado en remanentes refractivos de baja corrección:
Se ha demostrado que los resultados de la cirugía refractiva en este tipo de pacientes no son tan exactos como los realizados en gente joven, esto se ha relacionado con la edad del paciente, reportando que, a mayor edad, decrece la eficacia de la ablación esférica y aumentan las posibles alteraciones o complicaciones, como pueden ser las abrasiones corneales. (7)(8)
La cirugía ablacional de superficie se puede realizar en un tiempo postoperatorio más temprano dado que no necesita de succión o aplanamiento corneal, además de ser el más adecuado para aquellos pacientes que tuvieran cierto grado de ojo seco.
Para la ablación con técnica femtolasik, lo ideal sería esperar a 3 meses tras el primer procedimiento con idea de no producir dehiscencia de la incisión principal, además tiene la ventaja de un menos molesto postoperatorio y poder abordar graduaciones más altas amén de ofrecer mejores resultados y más predecibles en astigmatismos e hipermetropía.
OPCIÓN BASADA EN LENTES INTRAOCULARES
Los procedimientos basados en lentes: intercambio de lente o implante adicional–piggy back- (especialmente útil en aquellos casos que desconocemos la potencia de la lente implantada en la primera cirugía) , son preferibles en algunas situaciones y tienen ciertas ventajas (8).
Si se desea la corrección del error de refracción residual poco después de la cirugía de cataratas, se puede volver a abrir la incisión original de la catarata y se puede implantar la LIO poco después de la cirugía inicial (cambio de LIO), minimizando el trauma quirúrgico . (5) Tabla 1
Si hay una gran sorpresa refractiva posoperatoria, los procedimientos basados en lentes son efectivos para reducir los altos grados de error esférico. Siempre contemplando hacerlo preferentemente de haber realizado limpieza de la cápsula posterior con láser Nd-Yag.
- Los procedimientos basados en lentes no alteran la superficie anterior de la córnea y no cambian significativamente el poder refractivo de esta, pero hay que contemplar el riesgo en pacientes añosos de un contaje y estructura endotelial adecuada dado que se pueden ver perjudicados en una segunda intervención intraocular.
Tabla 1. Cálculo de la potencia de la lente intraocular para un implante secundario según Gayton
| Error refractivo post qca faco | Potencia de la lente a implantar |
| Miópico | Rx residual |
| Hipermetrópico | Rx residual x 1.5 |
| Error refractivo | |
| Potencia de la implantar | |
| Qca: cirugía | |
| Faco: facoemulsificación | |
| Rx : refracción | |
Referencias
Cirugía de lente intraocular. Selección, complicaciones y casos complejos. J.Bradley Randleman, Iqbal Ike K Ahmed. Capítulo 10: Sorpresas de IOL refractivo. Sonia H. Yoo, Sotiria Palioura y Vasilos F. Diakonis p 80-82, 2019
Alio JL, Grzybowski A, El Aswad A, Romaniuk D: Refractive lens exchange. Surv Ophthalmol 2014. [Epub ahead of print].
Refractive surgery after routine cataract surgery with multifocal IOLs attributable to corneal ephitelial basement membrane dystrophy. Vivian W.M. Ho, FRCOphth, Nick Stanojcic, FRCOphth, Naomi A.L. O’Brart, BSc, MCOptom, David P.S. O’Brart, MD, FRCS, FRCOphth, DO, RefCert(RCOphth). J Cataract Refract Surg 2019; 2019 ASCRS and ESCRS
Surgical options for correction of refractive error following cataract surgery Ahmed A Abdelghany1,2 and Jorge L Alio. Eye and Vision 2014 1:2
Complicaciones en la cirugía de cristalino. Francisco Poyales Galán . Elsevier . Monografía Sociedad Española de Cirugía Implanto Refractiva (SECOIR) 2016. Capítulo 51 : La sorpresa refractiva . Nuria Garzón Jiménez y Francisco Poyales Galán p 427-433
Hersh PS, Fry KL, Bishop DS. Incidence and associations of retreatment after LASIK. Ophthalmology. 2003;110:748-54.
Hu DJ, Feder RS, Basti S, Fung BB, Rademaker AW, Stewart P, et al. Predictive formula for calculating the probability of LASIK enhancement. J Cataract Refract Surg. 2004;30:363-8.
El Awady HE, Ghanem AA: Secondary piggyback implantation versus IOL exchange for symptomatic pseudophakic residual ametropia. Graefes Arch Clin Exp Ophthalmol 2013, 251(7):1861–1866.



 Dra. Ana Silvia Serrano – Colombia
Dra. Ana Silvia Serrano – Colombia Dra. Luisa Anaya – México
Dra. Luisa Anaya – México Figura 1. Lente intraocular Juvene
Figura 1. Lente intraocular Juvene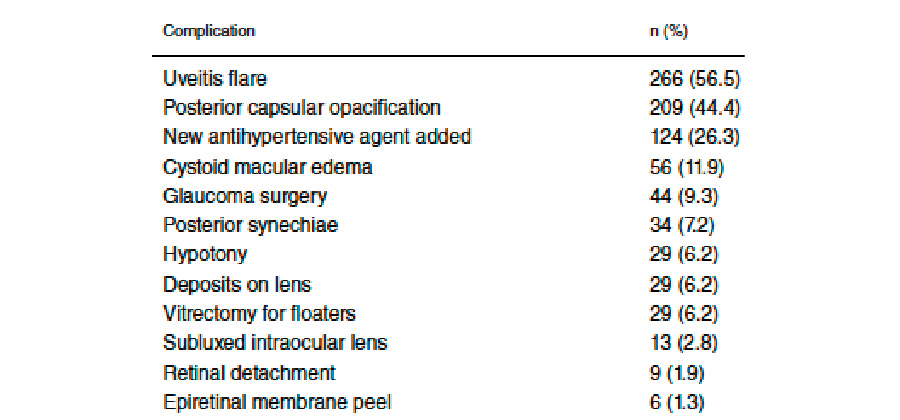 Tabla 1. Complicaciones postoperatorias presentadas en 471 pacientes con previo diagnóstico de uveítis que fueron operados de cirugía de catarata.
Tabla 1. Complicaciones postoperatorias presentadas en 471 pacientes con previo diagnóstico de uveítis que fueron operados de cirugía de catarata.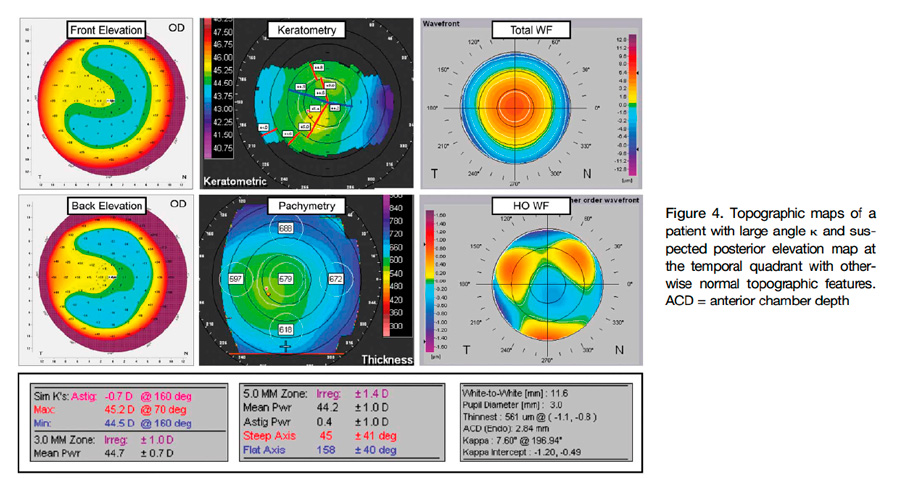 Un ángulo kappa elevado puede resultar en una ablación descentrada y aún más relevante es la correlación encontrada entre un ángulo kappa elevado y queratometrías más altas en elevación anterior y posterior en los 4 mm centrales en los cuadrantes temporales todo esto por el descentramiento en la lectura del estudio en córneas sanas usando la esfera de mejor ajuste. Este efecto se contrarresta si se usa la elipsoide tórica de mejor ajuste, ya que de esta forma se elimina el efecto que tiene el astigmatismo corneal sobre los mapas de elevación.
Un ángulo kappa elevado puede resultar en una ablación descentrada y aún más relevante es la correlación encontrada entre un ángulo kappa elevado y queratometrías más altas en elevación anterior y posterior en los 4 mm centrales en los cuadrantes temporales todo esto por el descentramiento en la lectura del estudio en córneas sanas usando la esfera de mejor ajuste. Este efecto se contrarresta si se usa la elipsoide tórica de mejor ajuste, ya que de esta forma se elimina el efecto que tiene el astigmatismo corneal sobre los mapas de elevación.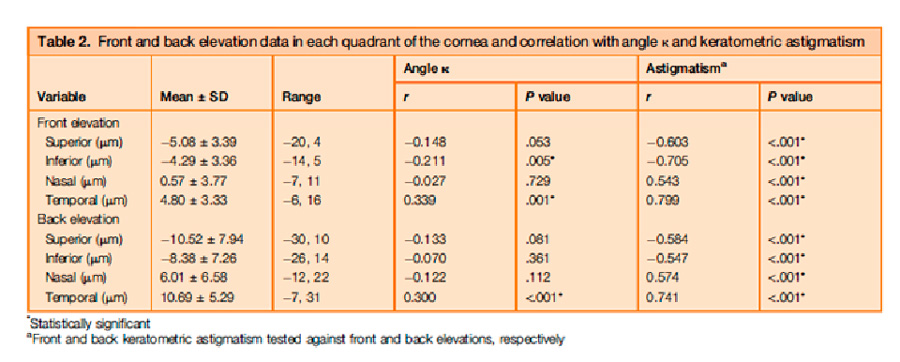 En conclusión, lo que los autores nos recomiendan es que sí estamos frente a una elevación anterior o posterior (temporales) dudosas, con ángulos kappa elevados y con topografías en su mayoría dentro de parámetros normales, se debe cambiar la esfera de mejor ajuste (BFS) por la elipsoide tórica de mejor ajuste (BFTE) y volver a verificar datos; si después de correlacionar datos, seguimos encontrando alteraciones, se debe hacer un mejor estudio de esa córnea para verificar la viabilidad de un procedimiento quirúrgico como: mapas epiteliales/estromales, histéresis corneal, entre otros.
En conclusión, lo que los autores nos recomiendan es que sí estamos frente a una elevación anterior o posterior (temporales) dudosas, con ángulos kappa elevados y con topografías en su mayoría dentro de parámetros normales, se debe cambiar la esfera de mejor ajuste (BFS) por la elipsoide tórica de mejor ajuste (BFTE) y volver a verificar datos; si después de correlacionar datos, seguimos encontrando alteraciones, se debe hacer un mejor estudio de esa córnea para verificar la viabilidad de un procedimiento quirúrgico como: mapas epiteliales/estromales, histéresis corneal, entre otros.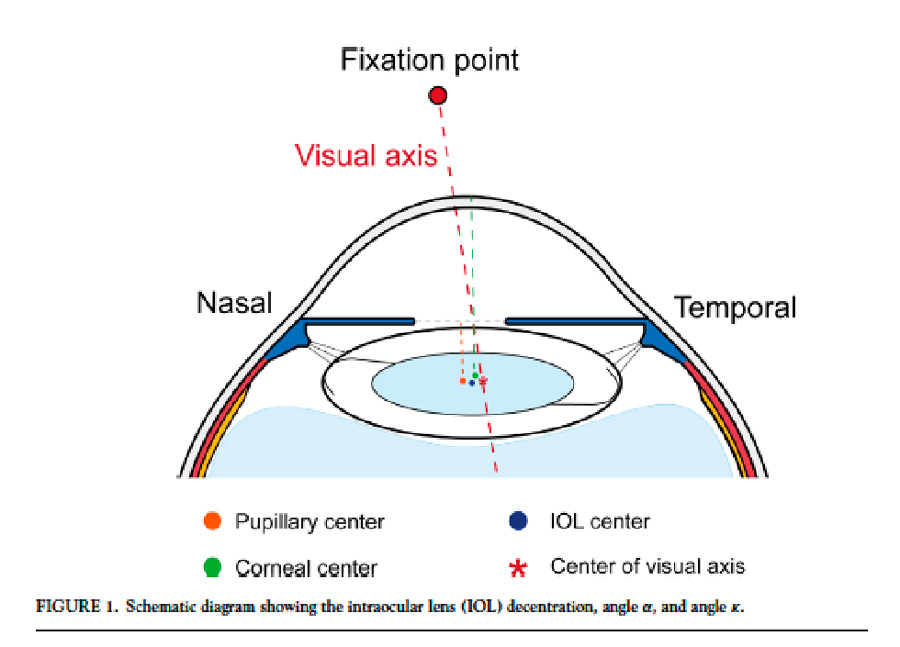 Si bien es cierto que la medida del ángulo kappa es importante en cirugía refractiva corneal, hoy día se ha vuelto un dato de gran relevancia a la hora de planear una facoemulsificación de catarata, en especial si se colocará un lente premium. Jie Xu et al5 realiza una cohorte prospectiva con 143 ojos y publica en octubre 2022 en el American Journal of Ophthalmology; una serie de variables estadísticamente significativas y determinantes como factores de riesgo para el descentramiento del lente, el cual, cuando supera los 0.4 mm genera cambios importantes en el confort visual.
Si bien es cierto que la medida del ángulo kappa es importante en cirugía refractiva corneal, hoy día se ha vuelto un dato de gran relevancia a la hora de planear una facoemulsificación de catarata, en especial si se colocará un lente premium. Jie Xu et al5 realiza una cohorte prospectiva con 143 ojos y publica en octubre 2022 en el American Journal of Ophthalmology; una serie de variables estadísticamente significativas y determinantes como factores de riesgo para el descentramiento del lente, el cual, cuando supera los 0.4 mm genera cambios importantes en el confort visual.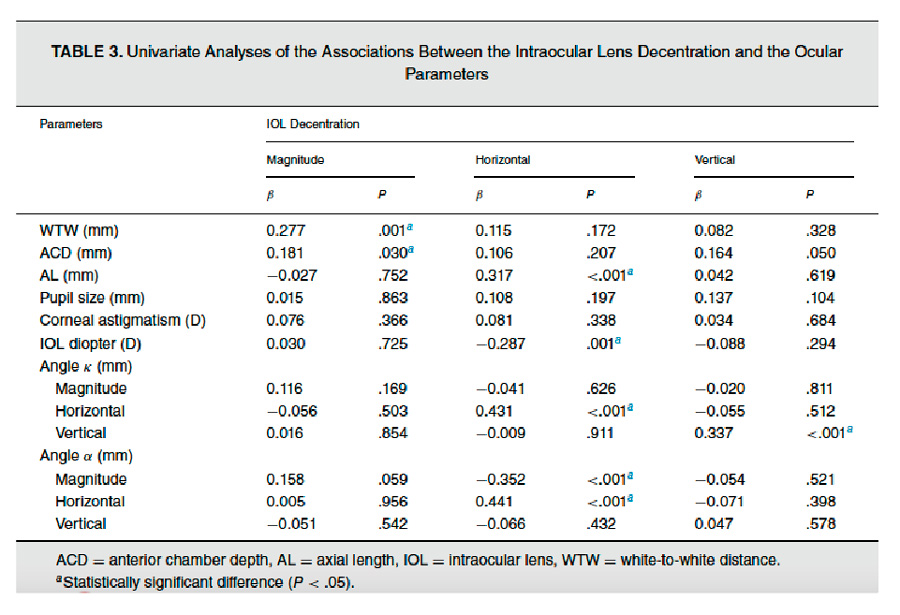 Este grupo define variables de predicción para descentramiento horizontal y vertical, siendo los más relevantes el White-to-White > a 12 mm y ángulo alpha > 0.50 mm; adicionalmente, ángulos kappa y alpha elevados horizontal y verticalmente también tienen importancia y favorecen el descentramiento, lo cual se puede explicar por la simetría rotacional del globo ocular, en el cual, el centro de la pupila es cercano al centro del saco capsular. Por el contrario de otros estudios, no se encontró la longitud axial elevada como factor de riesgo, aunque una cámara anterior amplia y un ángulo kappa vertical elevado favorecen el descentramiento vertical.
Este grupo define variables de predicción para descentramiento horizontal y vertical, siendo los más relevantes el White-to-White > a 12 mm y ángulo alpha > 0.50 mm; adicionalmente, ángulos kappa y alpha elevados horizontal y verticalmente también tienen importancia y favorecen el descentramiento, lo cual se puede explicar por la simetría rotacional del globo ocular, en el cual, el centro de la pupila es cercano al centro del saco capsular. Por el contrario de otros estudios, no se encontró la longitud axial elevada como factor de riesgo, aunque una cámara anterior amplia y un ángulo kappa vertical elevado favorecen el descentramiento vertical.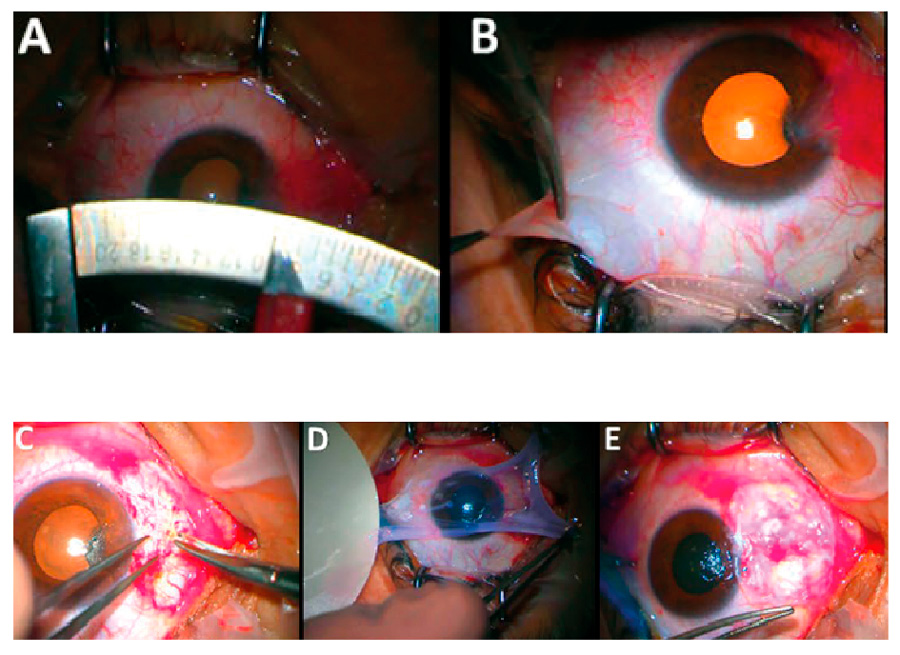 Figura 2. Imágenes intraoperatorias de SCET (simple conjunctival epithelial transplantation): A) Medición del área escleral comprometida por el pterigion. B) Toma de biopsia del tejido conjuntival del área superotemporal. C) Excisión de pterigion y exceso de tenon para dejar lecho escleral desnudo. D) El injerto de SCET (previamente procesado por técnico quien divide el tejido entre 8-10 fragmentos y los fija con adhesivo tisular a la membrana amniótica criopreservada) se coloca con adhesivo tisular sobre el lecho escleral. E) Se pueden notar los fragmentos de conjuntiva sobre el lecho escleral.
Figura 2. Imágenes intraoperatorias de SCET (simple conjunctival epithelial transplantation): A) Medición del área escleral comprometida por el pterigion. B) Toma de biopsia del tejido conjuntival del área superotemporal. C) Excisión de pterigion y exceso de tenon para dejar lecho escleral desnudo. D) El injerto de SCET (previamente procesado por técnico quien divide el tejido entre 8-10 fragmentos y los fija con adhesivo tisular a la membrana amniótica criopreservada) se coloca con adhesivo tisular sobre el lecho escleral. E) Se pueden notar los fragmentos de conjuntiva sobre el lecho escleral.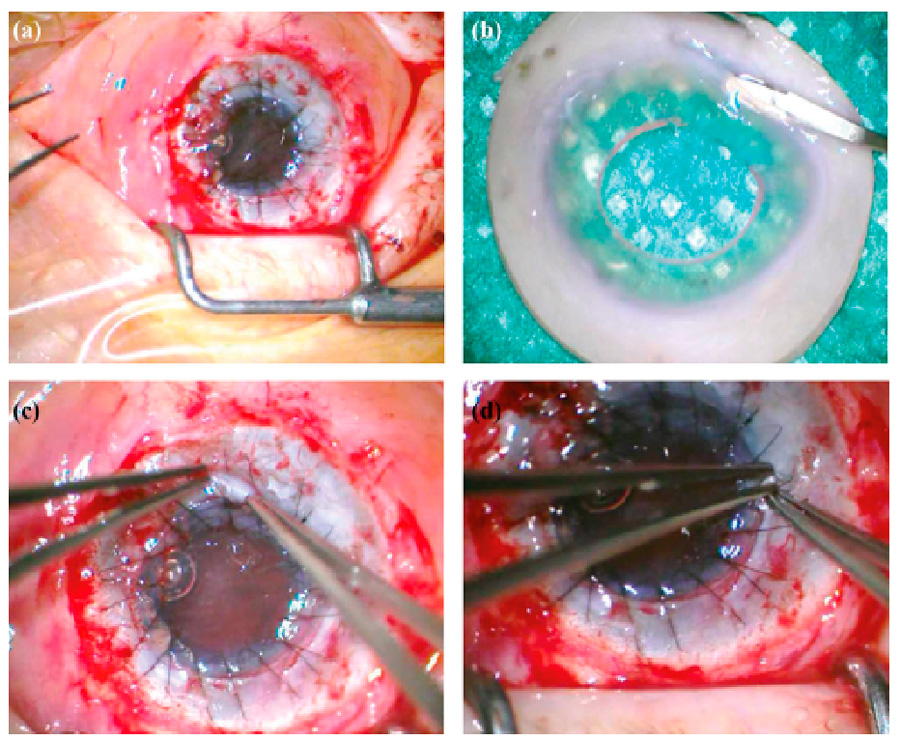 Figura 3. Fotografías intraoperatorias de cirugía ALT. A) Finalización de queratoplastia penetrante. B) Preparación de fragmentos de ALT. C y D) Colocación de los fragmentos de ALT debajo de las suturas.
Figura 3. Fotografías intraoperatorias de cirugía ALT. A) Finalización de queratoplastia penetrante. B) Preparación de fragmentos de ALT. C y D) Colocación de los fragmentos de ALT debajo de las suturas.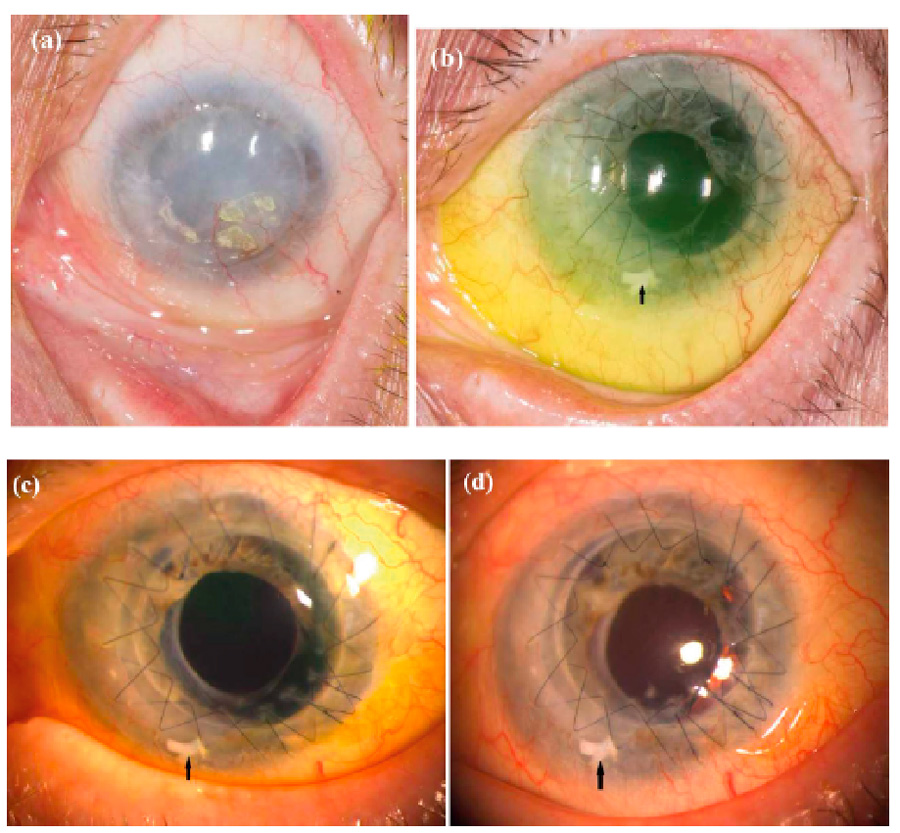 Figura 4. Fotografías clínicas de uno de los casos presentados con antecedente de quemadura química. A) Foto prequirúrgica. B) Postoperatorio a los 2 meses. C) Postoperatorio a los 12 meses. D) Postoperatorio a los 18 meses. La flecha indica un fragmento de ALT.
Figura 4. Fotografías clínicas de uno de los casos presentados con antecedente de quemadura química. A) Foto prequirúrgica. B) Postoperatorio a los 2 meses. C) Postoperatorio a los 12 meses. D) Postoperatorio a los 18 meses. La flecha indica un fragmento de ALT.


 Figura 1. Captura de pantalla del ChatGPT con la respuesta más aceptada sobre la formación de cataratas secundarias al cambio climático y los contaminantes del aire.
Figura 1. Captura de pantalla del ChatGPT con la respuesta más aceptada sobre la formación de cataratas secundarias al cambio climático y los contaminantes del aire.
 Por Dr. Omar López Mato
Por Dr. Omar López Mato El Juicio final • Miguel Ángel • 1541 – Capilla Sixtina, Vaticano, Italia.
El Juicio final • Miguel Ángel • 1541 – Capilla Sixtina, Vaticano, Italia. Paulo III con Alejandro y Octavio Farnesio • Tiziano • 1545 – Museo di Capodimonte, Nápoles, Italia.
Paulo III con Alejandro y Octavio Farnesio • Tiziano • 1545 – Museo di Capodimonte, Nápoles, Italia.


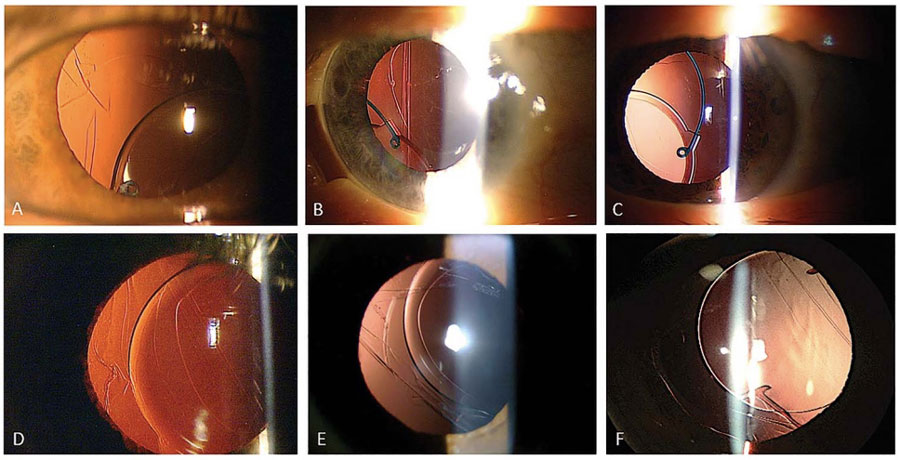 Figura 1. Fotografías de lámpara de hendidura de casos con sospecha de “dead bag syndrome” mostrando sacos capsulares particularmente limpios o transparentes. En algunos casos, el LIO se encuentra descentrado dentro del saco (A, B, C y F), y en algunos otros el saco capsular parece estar descentrado junto con el LIO (D, E).
Figura 1. Fotografías de lámpara de hendidura de casos con sospecha de “dead bag syndrome” mostrando sacos capsulares particularmente limpios o transparentes. En algunos casos, el LIO se encuentra descentrado dentro del saco (A, B, C y F), y en algunos otros el saco capsular parece estar descentrado junto con el LIO (D, E).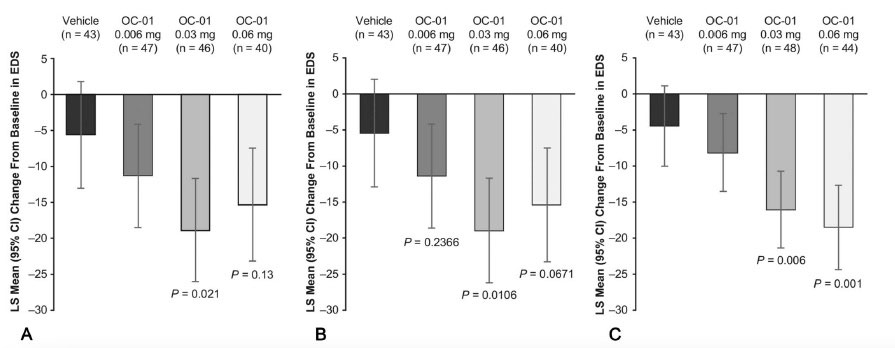 Tabla 1. A) Reducción de la escala EDS desde el punto de basal hasta el día 28. B) Reducción promedio de los mínimos cuadrados a los 28 días con los datos faltantes. C) Reducción promedio de los mínimos cuadrados a los 21 días en un ambiente controlado. Todas las comparaciones se hicieron con el grupo control (vehículo), con una diferencia estadísticamente significativa con la concentración 0.03 y 0.06 mg.
Tabla 1. A) Reducción de la escala EDS desde el punto de basal hasta el día 28. B) Reducción promedio de los mínimos cuadrados a los 28 días con los datos faltantes. C) Reducción promedio de los mínimos cuadrados a los 21 días en un ambiente controlado. Todas las comparaciones se hicieron con el grupo control (vehículo), con una diferencia estadísticamente significativa con la concentración 0.03 y 0.06 mg.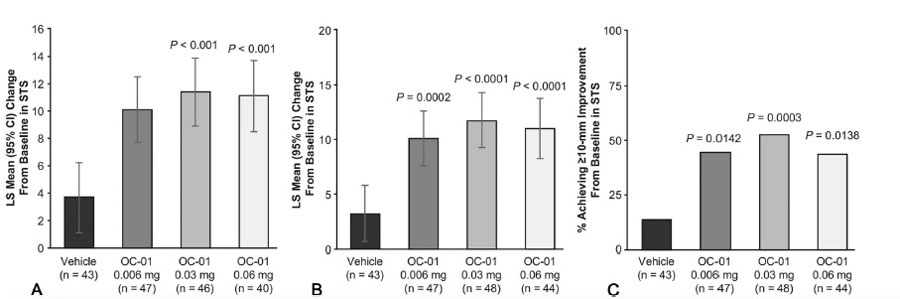 Tabla 2. A) Cambio promedio de mínimos cuadrados del basal hasta el día 28. B) Reducción promedio de los mínimos cuadrados a los 28 años con los datos faltantes. C) El porcentaje de pacientes que tuvieron al menos 10 mm de cambio en el test de Schirmer comparado con el grupo control. Estas tablas muestran una mejoría estadísticamente significativa en la producción de lágrima con OC-01 0.03 y 0.06, aumentando de ~5 mm a ~11 mm después de 28 días.
Tabla 2. A) Cambio promedio de mínimos cuadrados del basal hasta el día 28. B) Reducción promedio de los mínimos cuadrados a los 28 años con los datos faltantes. C) El porcentaje de pacientes que tuvieron al menos 10 mm de cambio en el test de Schirmer comparado con el grupo control. Estas tablas muestran una mejoría estadísticamente significativa en la producción de lágrima con OC-01 0.03 y 0.06, aumentando de ~5 mm a ~11 mm después de 28 días.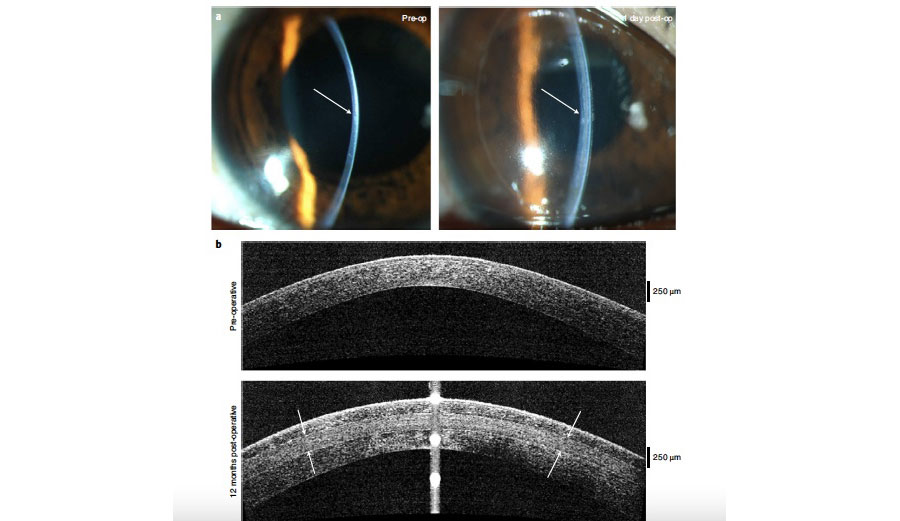 Figura 2. Datos clínicos de uno de los pacientes de india que recibieron BPCDX. A) Imágenes en lámpara de hendidura pre y postoperatorias. B) OCT pre y postquirúrgico donde se observa el BPCDX de 280 um de grosor, que muestra un engrosamiento y regularización de la superficie ocular. C) Mapas topográficos, de elevación anterior y paquimétricos que muestran un aplanamiento queratométrico central y un aumento en la paquimetría a los 12 meses.
Figura 2. Datos clínicos de uno de los pacientes de india que recibieron BPCDX. A) Imágenes en lámpara de hendidura pre y postoperatorias. B) OCT pre y postquirúrgico donde se observa el BPCDX de 280 um de grosor, que muestra un engrosamiento y regularización de la superficie ocular. C) Mapas topográficos, de elevación anterior y paquimétricos que muestran un aplanamiento queratométrico central y un aumento en la paquimetría a los 12 meses.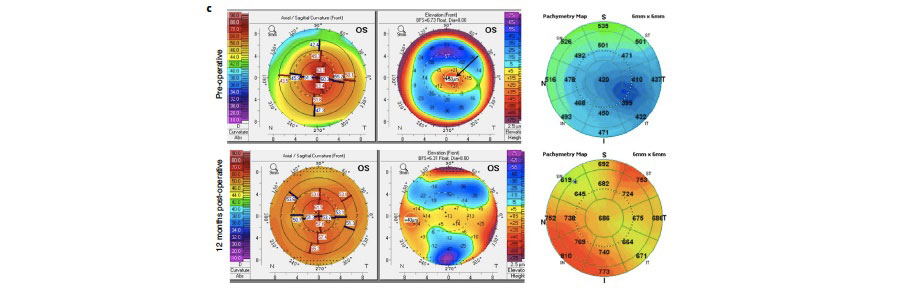
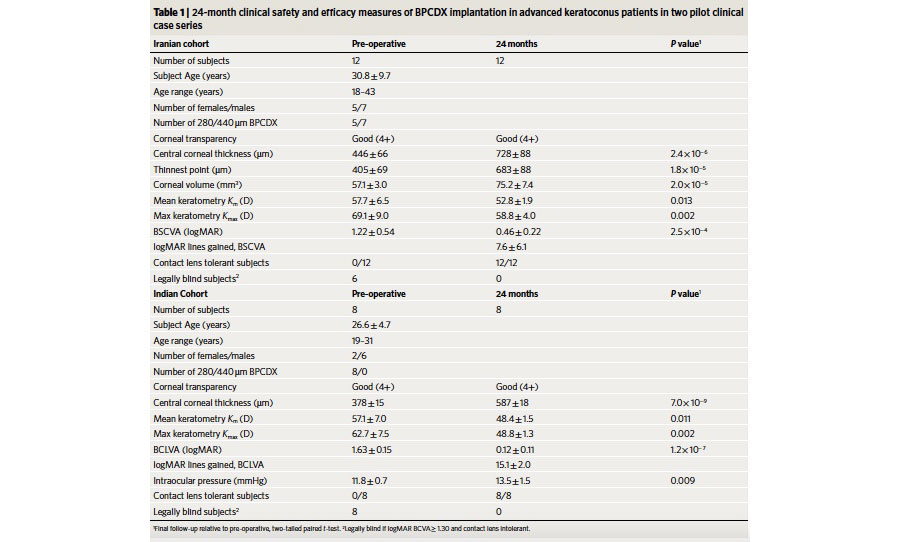 Tabla 3. Resultados de las variables medidas en la serie de casos del implante BPCDX.
Tabla 3. Resultados de las variables medidas en la serie de casos del implante BPCDX.



 La Virgen del canciller Rolin
La Virgen del canciller Rolin Izquierda:
Izquierda:  Izquierda:
Izquierda: 

 Zapata María Florencia, Córdoba, Argentina
Zapata María Florencia, Córdoba, Argentina

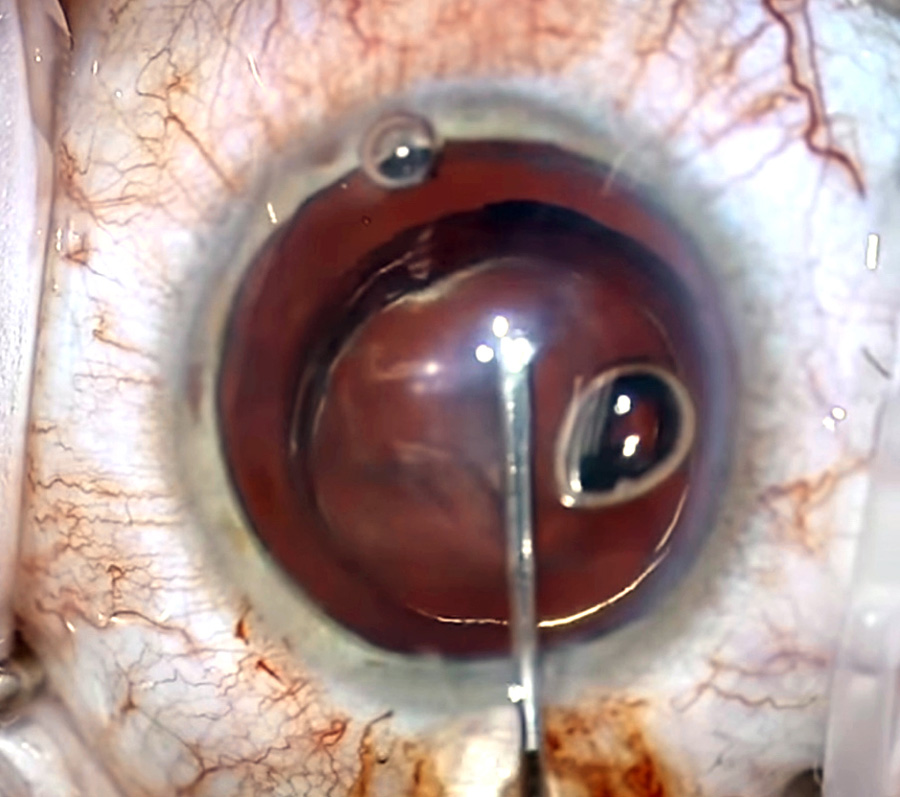 Imagen 1:
Imagen 1: 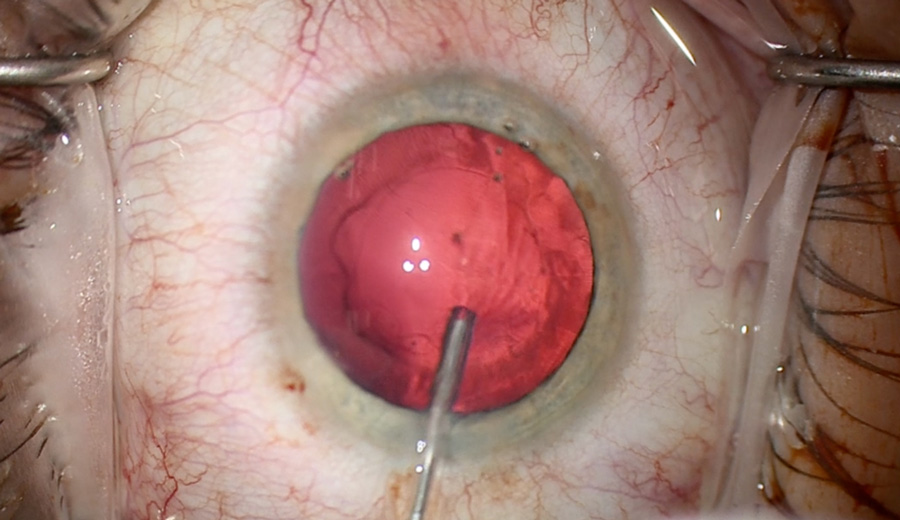 Imagen 2:
Imagen 2: