Foro catarata: Tecnología moderna para el cálculo de LIO
Coordinador
Dr. Julio Fernández Mendy – jofemendy@gmail.com
Invitados
Dr. Fernando Aguilera – drfaguilera@gmail.com
Dr. Daniel Badoza – dabadoza@gmail.com
Paciente de 73 años, en tratamiento por glaucoma desde hace 10 años con latanoprost, con daño mínimo. Miope desde los 12 años. Refracción histórica, según refiere, de -5 D aproximadamente y consulta para operarse de catarata.
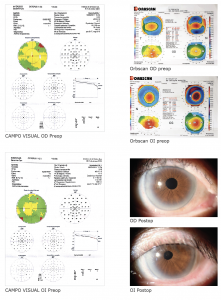
¿Cómo calcularía el LIO en este caso? Es un paciente que se va a operar de catarata y «se descubre» que tiene queratocono.
Dr. Fernando Aguilera: En este interesante caso hay varios aspectos a mencionar. En casos de ectasia corneal (y en pos cx refractiva corneal), el verdadero poder corneal es difícil de obtener porque la relación cara anterior/posterior corneal está alterada. La queratometría y la topografía anterior asumen una relación normal entre ambas caras corneales y miden el radio anterior de curvatura, lo que no es útil para el cálculo de córneas alteradas.
En este caso en particular, la tecnología con la que se evaluó este paciente no es la más avanzada para hacer cálculo con fórmulas de última generación. Por un lado el Orbscan no permite obtener todos los datos necesarios para utilizar en fórmulas avanzadas y el IOLMaster que se usó (IOLMaster 500, no Swept Source OCT-IOLM 700) no mide el espesor del cristalino, lo que es un factor esencial para calcular la posición efectiva del lente (ELPo). Por otro lado, el número de queratometrías del biómetro en este modelo es insuficiente.
Hubiera preferido contar con un tomógrafo corneal que ofreciera el True Corneal Power (TCP) como Pentacam, Galilei o Sirius para poder utilizar fórmulas que tomen en cuenta la relación cara anterior/posterior de córnea (Panacea/Olsen) para un cálculo más eficaz.
Cabe mencionar que un ojo tiene astigmatismo con la regla y el otro contra la regla, asimétrico e irregular por la ectasia corneal. Utilizando los datos que tenemos, utilizaría las fórmulas de Barret Universal II y Holladay 2 (en modo keratoconus), así tenemos que Barret y Holladay coinciden +/-1 dioptría en ambos ojos. En Holladay 2, el cálculo estándar vs. modo keratoconus pide 0,5 dioptrías menos en modo keratoconus.
Dicho lo anterior debemos siempre advertir al paciente sobre la inexactitud del cálculo, aun con la mejor tecnología, abriendo la posibilidad para el uso de anteojos y, en casos extremos, el recambio de lente.
Dr. Daniel Badoza: Nosotros realizamos el cálculo en casos de queratocono considerando los valores de queratometría que nos brinda los 3 mm centrales de la córnea. Para ello, realizamos un promedio de las mediciones que nos brinda la topografía de Plácido, la tomografía y la biometría por interferometría.
Es importante ser cuidadoso en la obtención de estos valores cuando existen grandes asimetrías o valores muy dispares entre uno y otro hemimeridiano. Lo más importante es calcular cuidadosamente los valores presentes en el área del eje visual y, sobre todo, descartar las mediciones que presenten artefactos, que son por cierto muy frecuentes en este tipo de pacientes. En particular en este caso, ya que el uso de latanoprost debe estar afectando la superficie ocular. Las fórmulas de cálculo preferidas son Haigis, Barret Universal II y SRK/T.
En cuanto a la selección de la LIO, en casos con intolerancia a los lentes de contacto y muy baja visión por la catarata, hemos obtenido resultados muy buenos con gran satisfacción de los pacientes implantando LIO tóricos. En casos donde la potencia esférica y cilíndrica requerida puede ser cubierta con un LIO convencional, usaremos AcrySof (como ocurre en el OD de este caso). En casos donde la potencia cilíndrica y/o la esférica necesarias están por fuera del rango convencional (mayor que 6 D de esfera y cilindro), encargaremos una Centerflex Premium de la firma Rayner, utilizando el calculador online provisto por la misma.1
En queratoconos que presenten agudeza visual no muy disminuida por la catarata y excelente tolerancia a la lente de contacto, la calidad visual posoperatoria con un LIO tórico podría ser inferior a la preoperatoria. En estos casos, preferimos apuntar a un equivalente esférico cercano a la emetropía, que en queratoconos como éste, con astigmatismo corneal no superior a 3 D, generalmente la AVSC obtenida ronda los 20/40, quedando a elección de los pacientes corregir el defecto residual con anteojos o lentes de contacto. Para nuestra sorpresa, en la mayoría de estos casos la AVSC obtenida fue suficiente para su vida cotidiana y los pacientes optaron por manejarse con anteojos para conducir o ver con más detalle la televisión.
Resolución del caso por el Dr. Julio Fernández Mendy
Es un caso desafiante desde el punto de vista del cálculo del LIO, pues calcular el LIO en el queratocono es un problema. En este caso, se suma que el paciente desconocía la verdadera problemática de su patología corneal. Siempre se consideró miope exclusivamente y se manejaba desde hace 10 años con anteojos que consideraba intermedios, con el que hacía todo: manejar automóvil y leer.
El primer tema fue explicarle el queratocono y la inexactitud en el cálculo. El segundo punto, tratar de consensuar las expectativas refractivas. Finalmente, llegamos a la conclusión de que NO podía quedar hipermétrope.
Faco OD 23 MAY 2016
LIO Acrysoft SA60AT de 11D
Análisis del cálculo: IOLMaster; multifórmula varía entre 7 D y 9,27 D.
Las K del Orbscan con el IOLMaster eran coincidentes en magnitud y bastantes cercanas en cuanto al eje.
Como la diferencia entre las fórmulas de Haigis y SRKT era de 2 D aproximadamente, decidí colocar 11 D que podría resultar con un error refractivo de -1 D con la SRKT
y -2,50 D con la Haigis (basado en casuística personal más exacta en mis casos).
Resultado al mes
AVSC: 20/25(-2); MAVCC: +0,25 -075 a 10° AV de 20/20(-2). AVSC cerca J2
PIO 10 mm Hg sin medicación.
Faco OI 25 JUL 2016
LIO Acrysoft SA60AT de 7 D
Análisis del cálculo: IOLMaster; multifórmula varía entre 1,5 D y 3 D.
Las K del Orbscan con el IOLMaster eran coincidentes en magnitud y bastantes cercanas en cuanto al eje. La fórmula de Haigis no la calculó, pues no pudo calcular el ACD. Dado el resultado del OD, en el cual resultó exacta la SRKT, el lente elegido fue 7 D para una refracción intentada de -2,25 D.
Resultado al mes
AVSC: 20/30(-2); MAVCC: -0,75 -0,75 a 95° AV de 20/20(-2). AVSC cerca J1
PIO 11 mm Hg sin medicación.

















