CC: ¿Cuál es la cirugía que más realizas?
DF: La faco es la más frecuente y la que más disfruto, por varias razones. Es más desafiante, con diferentes niveles de dificultad y permite la recuperación para el paciente de la agudeza visual perdida. Grandes satisfacciones para el médico y el paciente.
CC: ¿Tienes alguna actividad fuera de la profesión que te permite “desconectarte”, o tienes hobbies?
DF: La escultura. Me permite relajarme y reducir el estrés.
CC: Si pudieras solo hacer cirugía, ¿dejarías de hacer consulta oftalmológica?
DF: Me gustaría dedicarme a hacer solo cirugía y ver en consulta casos complejos o complicados, donde el día y la semana alcanzará para poder ver con detenimiento estos casos y realizar con paciencia y tiempo las cirugías.
CC: ¿Cómo sobrellevas el ritmo diario?
DF: Me tomo 5 tazas de café al día.
CC: ¿Haces cirugía bilateral simultánea?
DF: No realizó cirugía bilateral de rutina.
CC: Cuéntame brevemente tus preferencias de lentes intraoculares frente a diferentes situaciones.
DF: Pacientes con daño moderado de nervio óptico o mácula coloco LIO monofocal. Daño incipiente con posibilidad baja de progresión coloco LIO Edof. Pacientes con cirugía refractiva previa, miópica baja (bien centrada, Q<0.5) mono vs. Edof, miópica alta, hipermetrópica, QR, Monofocal.
CC: ¿Cuál es tu LIO preferido?
FS: Monofocal: Tecnis Monofocal 1piece asferico ZCB00
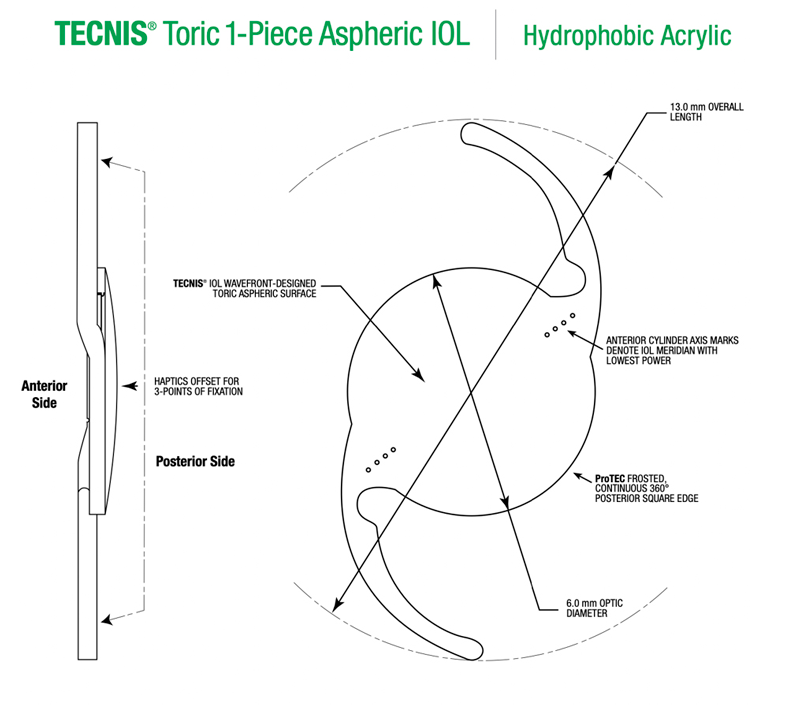
Monofocal Tórico < 6.00 Dt : Tecnis Toric II, 1 piece IOL ZCT

Monofocal Tórico > 6.00 Dt a 12.00 AT Torbi 709 M
Trifocal Torico >12.00 Astigmatismo: AT LISA Tri Toric 939 M, No recomiendo un lente de plato Zeiss LISA cuando se requiera un poder mayor a +24.00 por inestabilidad refractiva, ya que el lente es más grande que la bolsa.
CC: ¿Desde qué edad promedio haces facorefractiva?
FS: Los pacientes hipermétropes cuentan con un riesgo bajo de Desprendimiento de Retina, por lo tanto empiezo a considerar facorefractiva desde los 35 años de edad, no obstante, en hipermetropía elevada mayor a + 6.00 Dt aún en pacientes más jóvenes es una buena alternativa.
Para el paciente emétrope desde los 45 años. En pacientes miopes también desde esta edad considero multifocalidad ya que el LASIK monovisión proporcionará visión cercana por un periodo corto de tiempo.
CC: ¿Si pudieras solo hacer cirugía dejarías de hacer consulta oftalmológica?
FS: No la dejaría, disfruto los días de consulta. Hoy en día nos hemos convertido en educadores del paciente, y empleando distintas herramientas digitales como animaciones o videos, debemos dar a conocer el diagnóstico, alternativas de tratamiento, y describir procedimientos quirúrgicos, así como riesgos y beneficios.
CC: ¿Tú lectura preferida por fuera de la oftalmología?
FS: Novela histórica, o costumbrista mexicana, recomiendo Pedro Angel Palao: su libro sobre Pancho Villa “No me dejen morir así”, es una novela histórica muy apegada a la realidad sobre la vida de uno de los personajes históricos de la Revolución Mexicana sobre quien más se ha escrito
CC: ¿Cuáles son tus Hobbies?
FS: Jugar Tennis, cocinar parrilladas o paella.
CC: ¿Cuáles son tus alternativas quirúrgicas frente a un paciente con hipermetropía?
FS:
- ICL hipmetropico, desde que Roberto Zaldivar de Mendoza, Argentina me comentó hace algunos años sobre seguimientos a largo plazo con resultados favorables, empecé a considerarlo en pacientes jóvenes.
- Facorefractiva indudablemente proporciona excelente predictibilidad y estabilidad refractiva, aún en pacientes jóvenes.
- He estado pendiente del desarrollo futuro del tratamiento con Inlay de Aloinjerto Hipermetrópico (Allotex), inlay fabricado a base de colágeno humana que puede implantarse debajo de un flap de LASIK o por vía intraestromal a través de un bolsillo (pocket) creado con láser de Femtosegundo
 Trifocal: Physiol Micro F
Trifocal: Physiol Micro F

Trifocal Tórico < 6.00 Astigmatismo: Physiol Pod F

EDOF: J&J Eyehance y Eyehnce Tórico

CC: ¿Cómo es tu abordaje cuando tienes catarata y queratocono al mismo tiempo?
FS: Cuando me encuentro ante un caso de Queratocono razonablemente estable, córnea discretamente irregular y con poder corneal < 53.00 Dt realizo cálculo con fórmula de SRK-T.
En córneas francamente irregulares y poder > 53.00, con astigmatismo asimétrico e irregular considero realizar primero algún tipo de corneoplastia con TG-PRK o WFG PRK y cross-linking simultáneo o en casos aún más irregulares empleo primero implante de un segmento intracorneal que permita regularizar la córnea. Tres meses más tarde, realizo calculo de lente intraocular con fórmulas especiales como calcular post refractiva ASCRS, Shammas, Barret, Wang OCT, Hagis con reporte de EK Holladay a 3.5 mm (elimino poderes extremos y promedio los poderes centrales).
CC: ¿Qué LIO prefieres en pacientes con Glaucoma?
FS: Dependerá de la magnitud del Glaucoma, en un paciente estable Campo y OCT con cambios moderados, según el comité de Glaucoma de ESCRS sugieren que puede emplearse un lente intraocular trifocal o de foco extendido sin problema y lo considero
En casos moderados a avanzados de Glaucoma y catarata considero un lente monofocal asférico o pudiera emplear un lente de foco extendido.
Realizo frecuentemente procedimientos combinados como Facoemulsificación y Trabeculectomía, Facoemulsificación y Esclerectomía Profunda no Penetrante, Facoemulsificación y Válvula de Ahmed, y más recientemente Facoemulsificación asociada a MIGS (iSten) o en casos más avanzados ciclofotocoagulación transescleral laser.
CC: ¿En pacientes con ojo seco?
FS: Pienso que el ojo seco es una patología muy importante que debe ser tratada antes de cualquier procedimiento de Facoemulsificación. En nuestra clínica, procuramos realizar una evaluación preoperatoria de la calidad de la superficie ocular con el equipo diagnóstico Lacrydiag de Quantel que mide variables de la película lagrimal como tiempo de ruptura de película lagrimal, menisco lagrimal y meibografía; además también efectuamos HD Analizer para analizar estabilidad de la película lagrimal mediante Objective Scatterign Index (OSI).
En base a la magnitud de ojo seco, primero iniciamos manejo conservador a base de compresas húmedo calientes, aseo palpebral, colirios mixtos de antibiótico y esteroide, así como lubricante que además restaura la capa lipídica de la lágrima como Systante Complete o Balance. Dependiendo de la respuesta, y magnitud del ojo seco evaporativo relacionado meibomitis recalcitrante también podemos considerar 3 a 4 sesiones de Thermospa, luz pulsada intensa (IPL Thermaye) o expresión mecánica del meibo con pinzas palpebrales. Una vez que se observa una mejora en la calidad y estabilidad de la lágrima, reducción de lo síntomas, mejora en variables de la superficie ocular (menisco lagrimal, ruptura de película lagrimal y meibografía), podemos considerar proceder a la facoemulsificación de catarata con implante de lente intraocular. También buscamos consistencia en la calidad en calidad de la topografía corneal así como del poder corneal (queratometrias) con múltiples equipos (Topografia Topcon, Orbscan, Pentacam, IOL Master) que nos permita confiar en una mejor predictibilidad refractiva posterior.
CC: ¿Qué LIO prefieres en pacientes con personalidad tipo A?
FS: Pienso que debemos ser más críticos en este tipo de pacientes perfeccionistas, y explicar de manera formal y detenida los riesgos, beneficios y eventos adversos. Si queremos dormir en paz, es mejor emplear un lente Monofocal Asferico con una monovisión o un lente EDOF para evitar problemas de insatisfacción relacionada a los fenómenos fotopicos nocturnos como halos o deslumbramiento nocturno.
CC: ¿En pacientes con diabetes?
FS: La decisión de elegir qué tipo de lente emplear en un paciente con Diabetes, también depende del estado y estabilidad de la Retinopatía Diabética. En un paciente con excelente control y sin RTD o RTD de fondo no veo porqué no emplear un lente intraocular trifocal o EDOF.
Aquellos pacientes diabéticos con Retinopatías Diabéticas más avanzadas considerado un Lente Monofocal Asférico Tecnis 1 piece.
CC: ¿Y en pacientes post cirugía refractiva?
FS: Aunque es controversial, si implanto lentes intraoculares Trifocales y EDOF en casos de cirugía refractiva previa. Es obvio que debemos descartar casos con fotografías simétricas y demasiado irregulares, córneas altamente aberradas, y ojo seco significativo.
En casos post refractiva es importante realizar cálculos especiales como Shamas, ASCRS post refractiva, Barret, Wang OCT, Hagis con reporte Holladay EK a 3.5 mm, Panacea. Mi conducta personal es eliminar los extremos y promediar los cálculos centrales. No hay fórmula perfecta, así que hay que advertir al paciente sobre la tasa de retoque con cirugía láser corneal, PRK en alrededor del 10 al 15% de los casos, siempre y cuando la córnea lo permita.
En casos muy irregulares y con aberraciones ópticas elevadas, he tenido la experiencia de emplear el lente Xtrafocus pinhole IOL de Morcher, este dispositivo estenopeico se implanta algunos meses después del implante intraocular inicial para reducir aberraciones y mejorar la AVMC postoperatoria con resultados favorables.
CC: ¿Operarás Prelex con EDOF?
FS: Algunos pacientes lo requieran por necesidades profesionales evitar fenómenos fotopicos halos, y deslumbramientos nocturnos como en pilotos aviadores o personal que requiera conducir de noche es una buena alternativa. Mi experiencia se ha limitado al lente EDOF Eyehance de J&J, aunque recientemente ha llegado el lente Vivity a nuestro país. Y mi experiencia ha sido favorable.
CC: ¿Qué lentes te implementarías en tus ojos si tuvieras que operarte?
FS: Predicando con el ejemplo. Después de ver los resultados positivos logrados por nuestros pacientes, recientemente elegí
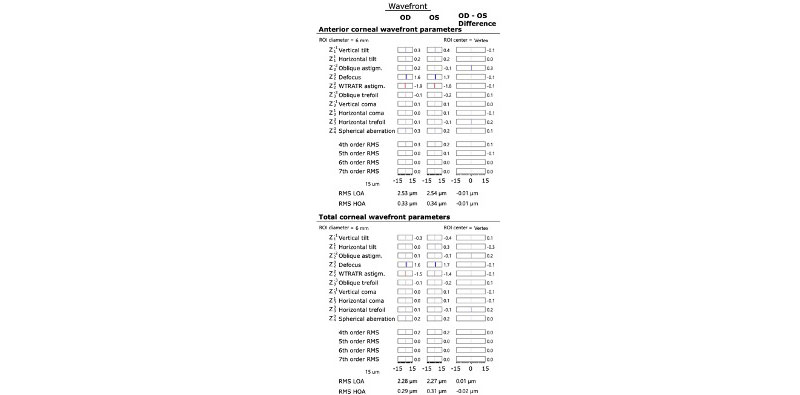
RELEX para mí. Fui sometido a cirugía RELEX en la ciudad de Guadalajara (en noviembre de 2020), por mi colega y amigo Ricardo Acosta. *Decidí considerar LIO FineVision Tri Toric POD F bilateralmente. Esta es una LIO hidrófila y difractiva, tiene un diseño de hápticas de doble asa en C y 5º de angulación para un excelente centrado y estabilidad. Elegí una LIO hidrofílica ya que ofrece menor aberración longitudinal cromática en comparación con los materiales hidrofóbicos (mejor calidad de percepción del color y contraste en alta iluminación) 1-3. La lente cuenta con filtro UV y un bloqueador de luz azul. El diámetro del cuerpo óptico es de 6 mm y el diámetro total es de 11,4 mm. Además de su poder para de refracción lejana, FineVision POD F proporciona dos focos para la agudeza visual intermedia y de cerca, con potencias adicionales de 1,75 y 3,50 D, respectivamente.4 Importante resaltar, que se ha demostrado que la combinación de cirugía de catarata con láser de femtosegundos y aberrometría intraoperatoria optimiza el posicionamiento y mejora el astigmatismo residual postoperatorio de una LIO tórica.5 En mi caso, presentaba astigmatismo queratometrico de 1,50 D en mi ojo derecho y 1,25 D en el izquierdo, por lo que pensé que el procedimiento de cirugía con FLACS y aberrometría intraoperatoria eran la mejores opciones para mis ojos. También, se ha demostrado que los ojos sometidos a extracción de cataratas e implantación de una LIO tórica asistida por aberrometría intraoperatoria tienen 2,4 veces más probabilidades de tener menos de 0,50 D de astigmatismo residual en comparación con los métodos de facoemulsificación estándar de corrección del astigmatismo. 6
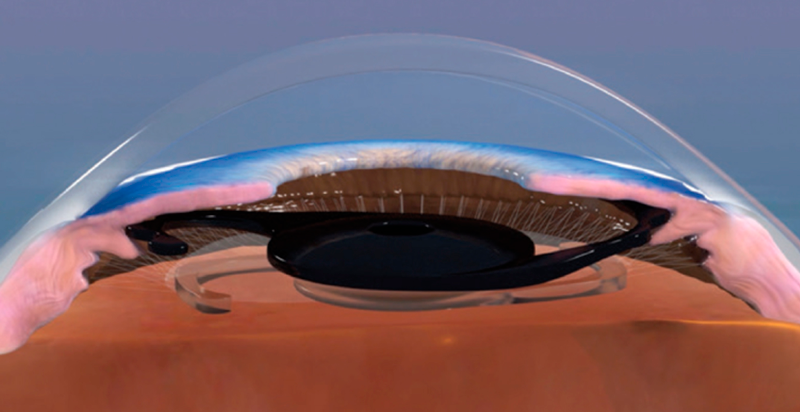
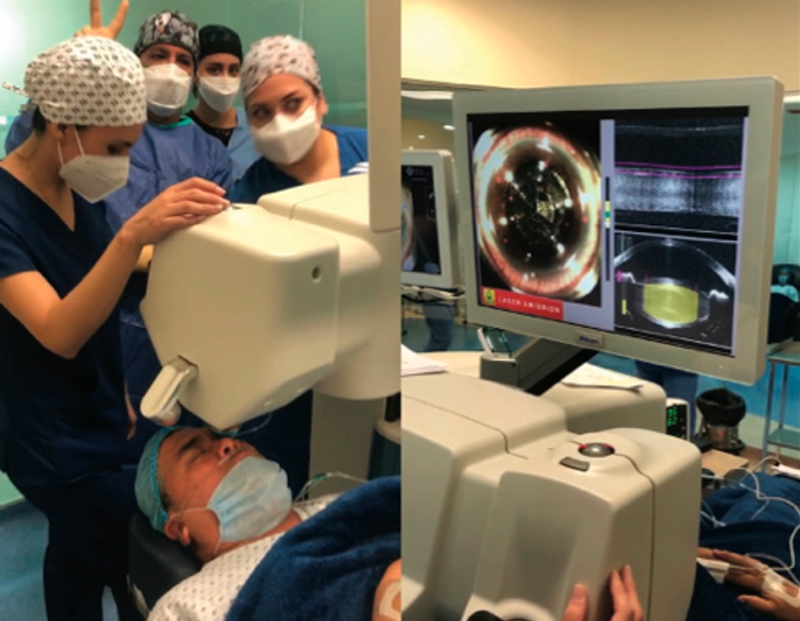
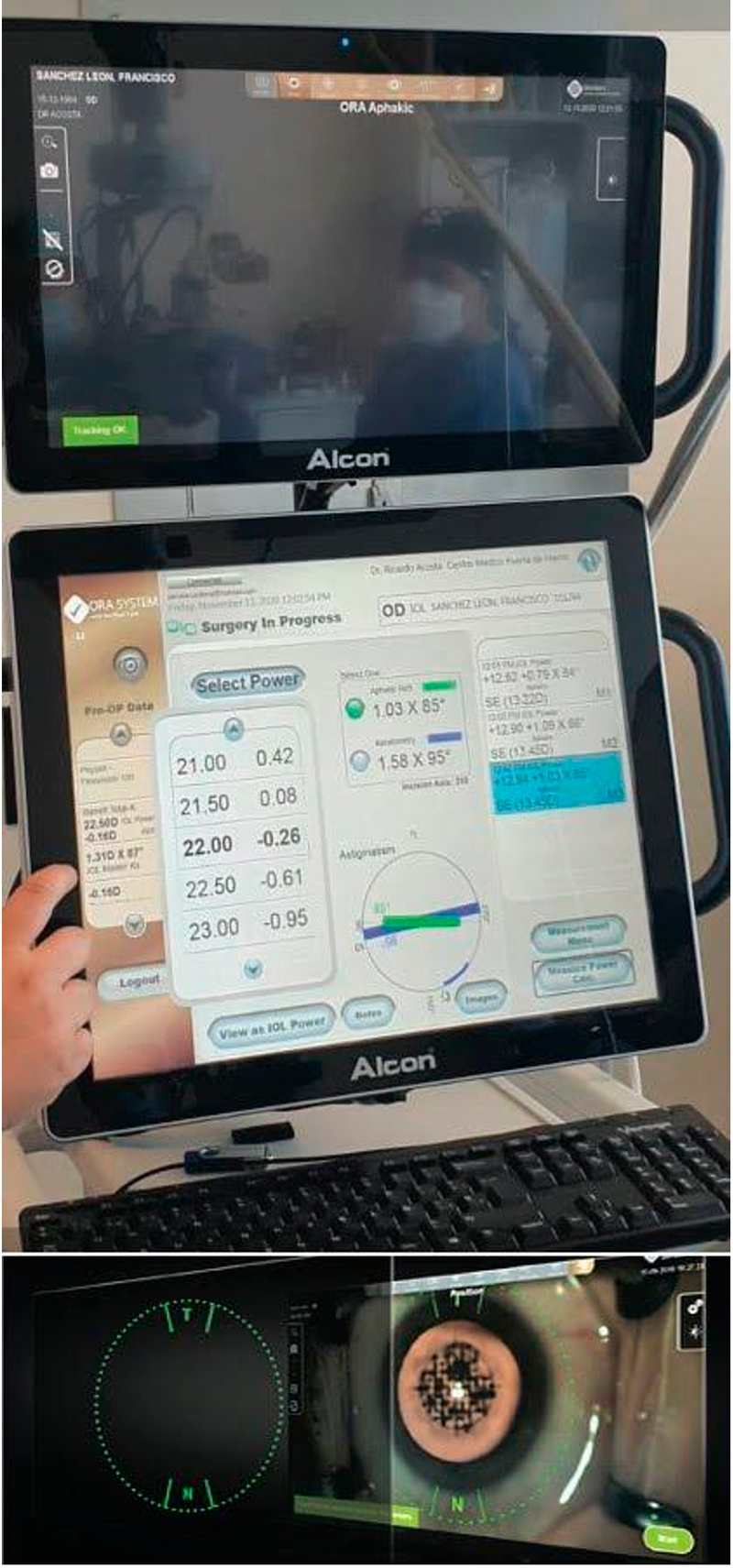
RESULTADOS
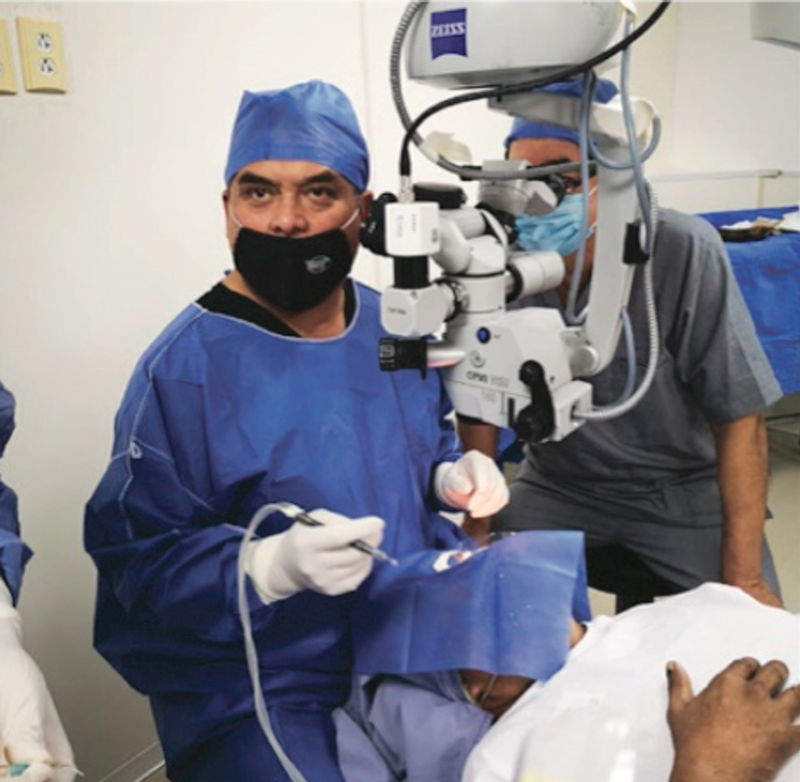
Desde la primera semana postoperatoria obtuve buena agudeza visual de cerca y de lejos, incluso cuando conducía de noche, mi agudeza visual fue nítida desde los primeros días. A los 7 días de mi procedimiento RELEX, realicé 26 cirugías de catarata en nuestra Clínica Novavision Acapulco sin ningún problema (Figura 7), noté un aumento en mi percepción 3D bajo el microscopio, así como aumento en la profundidad de campo (visión nítida a dos distancias distintas, sin la participación de la acomodación). Nueve días después de la cirugía, realicé tres queratoplastias penetrantes, una queratoplastia lamelar anterior profunda y un DSEAK sin molestia alguna. A 15 meses de la cirugía, mi experiencia ha sido positiva ya que he recuperado mi visión de cerca e intermedia, que me permite continuar disfrutando de manera especial nuevamente de la clínica y la cirugía.
Dr. Carlos Restrepo
CC: ¿Cuál es tu LIO preferido?
CR: Al referirse al preferido es el que más implanto, entonces serían trifocales difractivos, aunque cada paciente debería individualizarse al planear su lente.
CC: ¿Desde que edad promedio haces facorefractiva?
CR: Después de los 50 años es lo usual. Aunque un par de casos especiales se han salido de ese parámetro.
CC: Si pudieras solo hacer cirugía, ¿dejarías de hacer consulta oftalmológica?
CR: Antes de oftalmólogo soy médico y disfruto de tratar pacientes. La cirugía y la consulta se complementan, además que disfruto conocer el antes, durante y después de cada caso, conocer cómo se transforma cada paciente con el tratamiento que dirigimos.
CC: ¿Tu lectura preferida por fuera de la oftalmología?
CR: Otras formas de ciencias como la astronomía, también crecimiento y gestión personal.
CC: ¿Cuáles son tus hobbies?
CR: Disfruto de la astronomía, fotografía, el deporte y la música (excepto el reggaeton).
CC: ¿Cuáles son tus alternativas quirúrgicas frente a un paciente con hipermetropía?
CR: Cada vez trato de realizar menos cirugía corneal en estos pacientes. Lo ideal sería una facorefractiva cuando el tiempo lo permita.
CC: ¿Cómo es el abordaje cuando tienes catarata y queratocono al mismo tiempo?
CR: Se los remito al Dr. Cesar Carriazo.
CC: ¿Qué LIO prefieres en pacientes con Glaucoma?
CR: Dependiendo del estadio del glaucoma y si el paciente es adherente al tratamiento. Si no existen alteraciones funcionales y el paciente es adherente al tratamiento no veo contraindicación en lentes trifocales. En caso de lesión funcional los lentes de rango extendido son una excelente opción.
CC: ¿Qué LIO prefieres en pacientes con personalidad tipo A?
CR: En ese tipo de pacientes lo más importante es un adecuado tiempo para explicar de manera realista el alcance de su cirugía, el implante y sobre todo las limitantes que tiene. Para ese tipo de paciente todo, o ningún, lente puede ser un problema. Lo que hago con ellos es solicitarles que me repitan lo que entendieron de cada opción y que el escoja la que más se ajuste a sus necesidades.
CC: ¿Qué LIO prefieres en pacientes post cirugía refractiva?
CR: Para estos pacientes tenemos excelentes opciones con los lentes de rango extendido
CC: Operaras Prelex con EDOF?
CR: La cirugía con lentes EDOF gana cada vez más terreno y es una opción para los pacientes que desean Prelex. Sin embargo hay que hablar claramente de las limitaciones con el paciente y planear el manejo, ya que en muchos sienten que las expectativas no se cumplen al 100%.
CC: ¿Qué lentes te implementarías en tus ojos si tuvieras que operarte?
CR: Hago astronomía visual y fotografía con DSLR. Por esto me implantaría un lente EDOF.
Referencias
Bozukova D, Pagnoulle C, Jérôme C. Biomechanical and optical properties of 2 new hydrophobic platforms for intraocular lenses. J Cataract Refract Surg. 2013;39(9):1404-1414.
Vinas M, Dorronsoro C, Garzón N, Poyales F, Marcos S. In vivo sub- jective and objective longitudinal chromatic aberration after bilat- eral implantation of the same design of hydrophobic and hydrophilic intraocular lenses. J Cataract Refract Surg. 2015;41(10):2115-2124.
Poyales F, Garzón N, Pizarro D, Cobreces S, Hernández A. Stability and visual outcomes yielded by three intraocular trifocal lenses with same optical zone design but differing material or toricity. Eur J Ophthalmol. 2019;29(4):417-425.
Loicq J, Willet N, Gatinel D. Topography and longitudinal chromatic aberration characterizations of refractive–diffractive multifocal intraocular lenses. J Cataract Refract Surg. 2019;45(11):1650-1659.
Orts P, Piñero DP, Aguilar S, Tañá P. Efficacy of astigmatic correction after femtosecond laser-guided cataract surgery using intraoperative aberrometry in eyes with low-to-moderate levels of corneal astigmatism. Int Ophthalmol. 2020;40:1181-1189.
Hatch KM, Woodcock EC, Talamo JH. Intraocular lens power selec- tion and positioning with and without intraoperative aberrometry. J Refract Surg. 2015;31(4):237-242.
 Después de un largo tiempo pudimos reencontrarnos en el congreso de la Sociedad Americana de Catarata y Cirugía refractiva. La pandemia fue una época de renacimiento tecnológico y con ella tuvimos que buscar soluciones para realizar nuestras actividades del día a día de forma remota, con esto empezamos a usar cada vez más la telemedicina. En el Glaucoma day, el Dr. Jacob Brubaker habló de la importancia de la telemedicina y que esta tecnología llegó para quedarse. Sin embargo, esta no fue la única innovación presentada en el congreso que tenía como fin hacer un seguimiento remoto a los pacientes, el Eyetelligence presentado por Bausch+Lomb es una plataforma que funciona por inteligencia artificial, su función es interpretar los resultados de los exámenes de los pacientes y detectar progresión, enviándoles una alerta que indica que es hora de regresar al control. Este año también fue lanzado oficialmente el iCare 2 que es un tonómetro para usar en casa, el paciente puede tomar su presión intraocular de forma fácil y la curva de presiones queda directamente guardada en su historia clínica gracias a la app que viene integrada, llamada Patient2.
Después de un largo tiempo pudimos reencontrarnos en el congreso de la Sociedad Americana de Catarata y Cirugía refractiva. La pandemia fue una época de renacimiento tecnológico y con ella tuvimos que buscar soluciones para realizar nuestras actividades del día a día de forma remota, con esto empezamos a usar cada vez más la telemedicina. En el Glaucoma day, el Dr. Jacob Brubaker habló de la importancia de la telemedicina y que esta tecnología llegó para quedarse. Sin embargo, esta no fue la única innovación presentada en el congreso que tenía como fin hacer un seguimiento remoto a los pacientes, el Eyetelligence presentado por Bausch+Lomb es una plataforma que funciona por inteligencia artificial, su función es interpretar los resultados de los exámenes de los pacientes y detectar progresión, enviándoles una alerta que indica que es hora de regresar al control. Este año también fue lanzado oficialmente el iCare 2 que es un tonómetro para usar en casa, el paciente puede tomar su presión intraocular de forma fácil y la curva de presiones queda directamente guardada en su historia clínica gracias a la app que viene integrada, llamada Patient2.











 Senecio • Paul Klee • 1922 Kunstmuseum, Basilea, Suiza.
Senecio • Paul Klee • 1922 Kunstmuseum, Basilea, Suiza.




 Trifocal: Physiol Micro F
Trifocal: Physiol Micro F







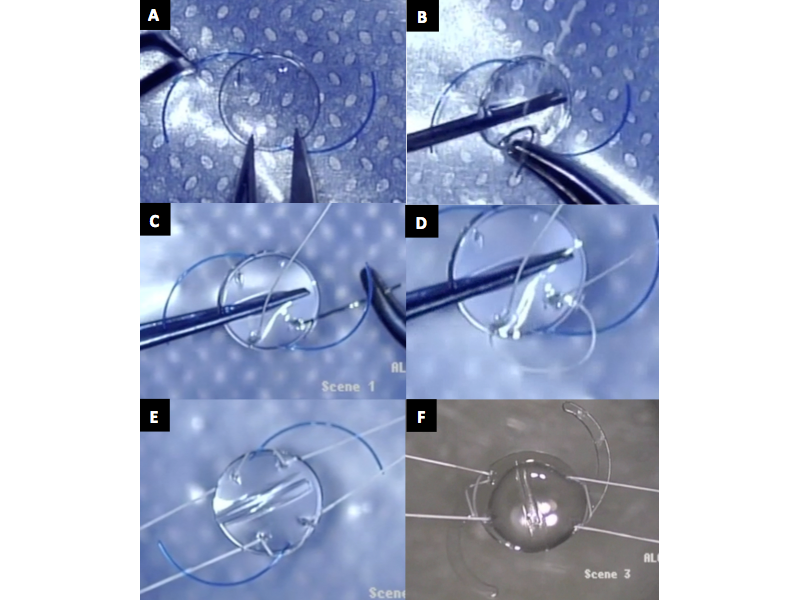
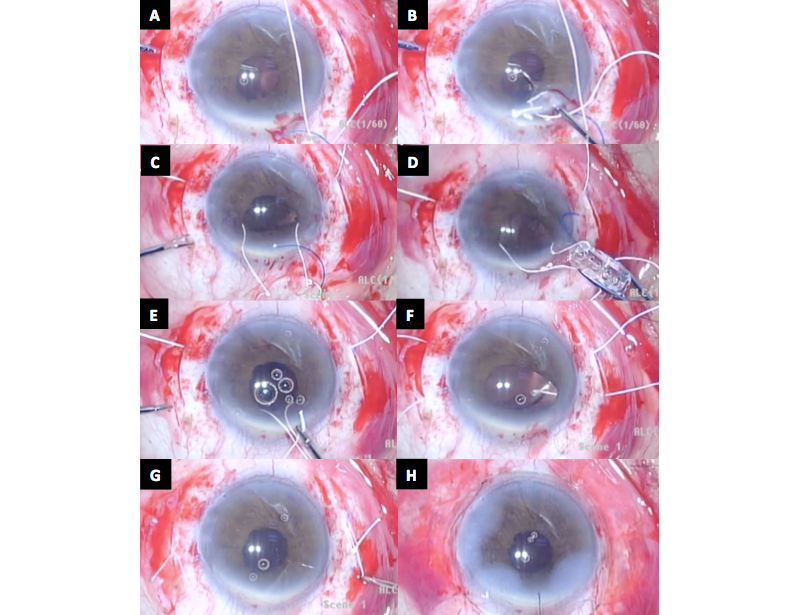
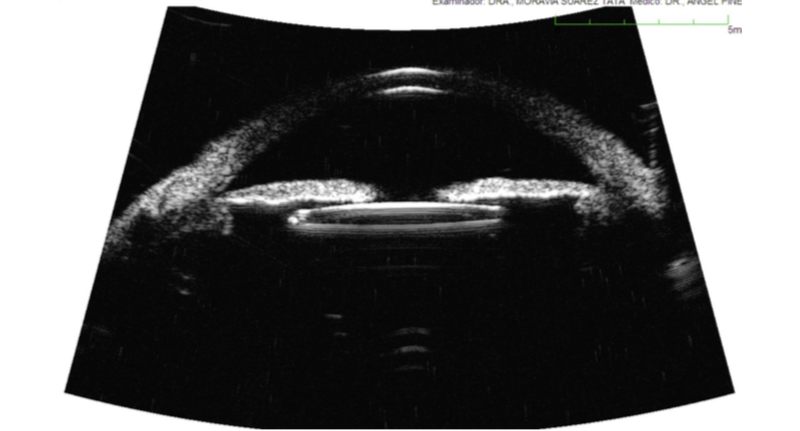 Figura 3. Biomicroscopía Ultrasónica (UBM) muestra Lente Intraocular bien centrado y sin inclinación (tilt) 6 meses después de la cirugía de Transfixión del LIO plegable con Gore-Tex.
Figura 3. Biomicroscopía Ultrasónica (UBM) muestra Lente Intraocular bien centrado y sin inclinación (tilt) 6 meses después de la cirugía de Transfixión del LIO plegable con Gore-Tex.






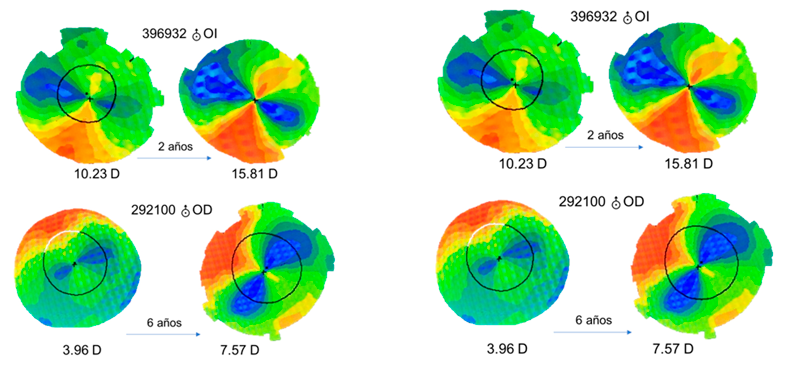 Figura 1 Figura 2
Figura 1 Figura 2
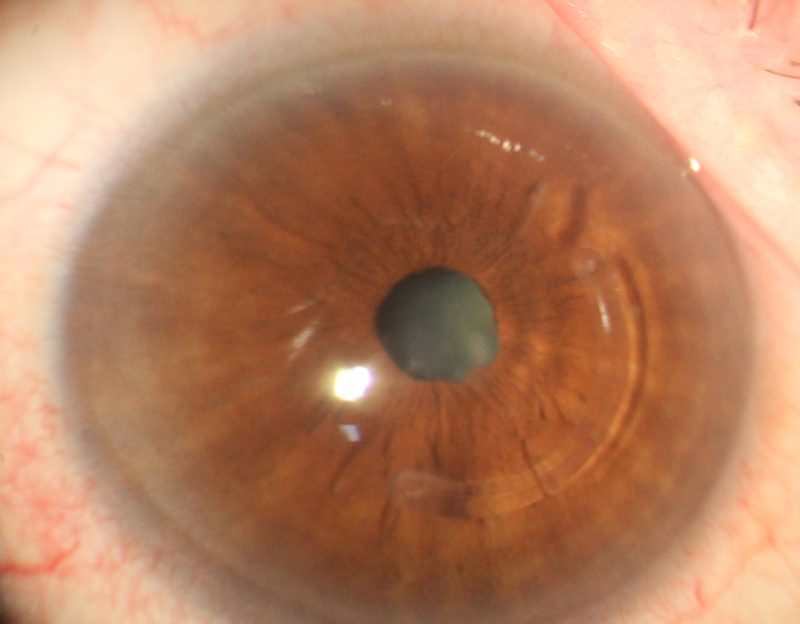
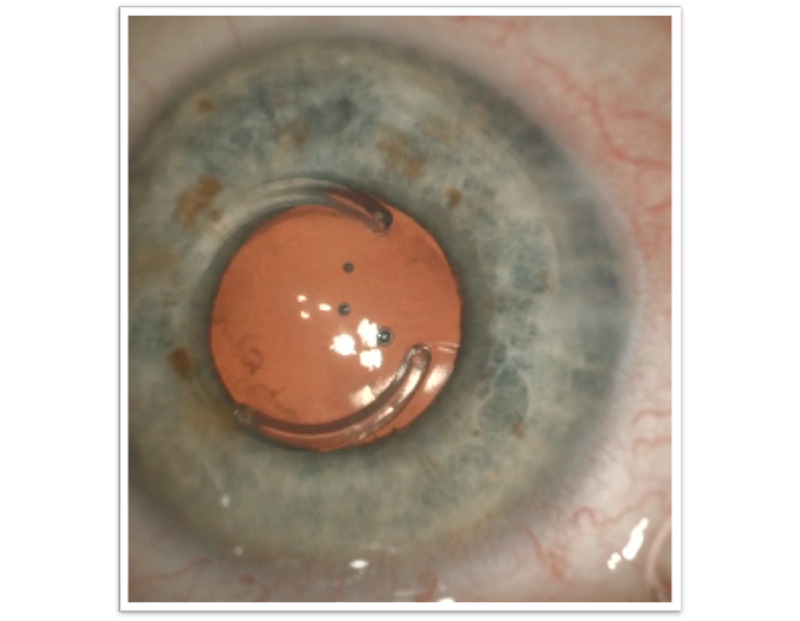


 Dr. Gerardo Valvecchia
Dr. Gerardo Valvecchia Dr. Daniel Badoza
Dr. Daniel Badoza