La medicina siempre ha sido una disciplina científica sujeta a continuas transformaciones a lo largo de toda su historia. Pero no todos los cambios han sido suficientemente profundos como para marcar una impronta que produzca una modificación significativa en su forma de estar presente en la sociedad.
En los últimos tiempos ha habido modificaciones en la concepción de la medicina tal y como la conocíamos durante años y también en la forma de desarrollar la actividad asistencial.
En la era digital, la ciencia, y especialmente la salud, está inmersa en una revolución tecnológica con la incorporación de nuevas herramientas de trabajo como la historia clínica electrónica que, aunque fue una gran aportación al menos hasta este momento, no ha permitido la esperada capacidad de explotación de datos. Algo parecido está sucediendo con la propuesta de la “medicina basada en la evidencia” que a pesar de su evidente interés no deja de ser lenta y costosa, viéndose superada por el propio avance de la medicina en ocasiones.
Dentro de esta revolución tecnológica digital la aplicación de la llamada inteligencia artifificial (IA) está siendo uno de los hitos más importantes.
¿Pero qué se entiende por IA? Aunque fue McCarthy quien acuñó dicho término en la conferencia de Dartmouth de 1956 como “la ciencia e ingeniería de hacer máquinas que se comporten de una forma que llamaríamos inteligente si el humano tuviese ese comportamiento”, ha habido muchos autores después que han propuesto otras defifiniciones. Dichasdefifinicionespueden estar basadas en múltiples criterios, como por ejemplo en el proceso de razonamiento en vez del resultado, de forma que si el proceso de razonamiento se asemeja al humano también se denominaría IA.
Este concepto, en auge en las últimas décadas, no es por tanto novedoso. Ya desde 1950 los científificos, especialmente los programadores de software comenzaron a diseñar sistemas que tuviesen funciones similares a las atribuidas a los humanos y comenzaron a desarrollar esa idea. Muchos de los softwares diseñados en un principio estaban relacionados con sistemas de juegos. Rosenblatt realizó en 1957 un esquema electrónico que se llamó “perceptron” que simulaba el comportamiento de una neurona con conexiones, lo que se considera el primer paso de lo que fifinalmente serían las denominadas redes neuronales.
Y surgen las primeras preguntas: ¿esa inteligencia tal como la entendemos la puede generar una máquina? ¿pueden pensar las máquinas?
En la actualidad, la IA tiene varias áreas de investigación para abordar los diferentes problemas:
• El aprendizaje automático, que permite el análisis y la obtención de conocimiento a partir de los datos que se van incorporando.
• Las redes neuronales que representan modelos computacionales basados en el procesamiento automático inspirado en el funcionamiento del sistema nervioso humano.
• El Big Data, que se resume como el proceso de recogida de una cantidad ingente de datos estructurados, semiestructurados y no estructurados que tienen el potencial de ser analizados y procesados para obtener información, patrones repetitivos o correlaciones no evidentes.
La clave para este aprendizaje automático es el entrenamiento de los sistemas gracias al aumento de la capacidad y rendimiento de los sistemas de procesamiento de la gran cantidad de datos incorporados.
El Big Data, dado el gran número de datos, la complejidad y también su diversidad precisa la utilización de algoritmos y técnicas de análisis que permitan su gestión y procesamiento para poder obtener el conocimiento oculto en ellos.
Estas técnicas de análisis de datos llevan ya tiempo siendo utilizadas en la empresa para reducir costes, mejorar la rapidez de toma de decisiones y la adaptación de los productos a las necesidades de los pacientes de acuerdo a la información analizada.
Existen numerosos ejemplos
que ponen de manifiesto su uso.
En el turismo midiendo el grado
de satisfacción de los clientes,
en la administración de empre-
sas conociendo la capacidad y
calidad de producción, el ajuste
de presupuestos, incluso la pro-
puesta de inversiones. En mer-
cadeo y publicidad usando la
analítica predictiva para saber
la demanda esperable, el con-trol efectivo de stocks, procesos de envío y la satisfacciónexperiencia del cliente.
Algo parecido ocurre en el ámbito de la sanidad. Es posible conocer cuáles son las necesidades de los pacientes y de acuerdo a esta información establecer carteras de servicios, coberturas de seguros e incluso establecer modelos de diagnóstico y propuestas de tratamiento de una manera casi inmediata.
Si nos centramos en la oftalmología, el hecho de que su desarrollo tecnológico en los últimos tiempos la haya convertido en una especialidad tan compleja que resulta imposible ser ejercida en su totalidad por un único especialista capaz de dominar todas las técnicas diagnósticas, terapéuticas, quirúrgicas y además en todas las patologías la ha hecho ser beneficiaria en gran medida de las técnicas de inteligencia artificial (IA).
Los nuevos algoritmos disponibles en oftalmología ofrecen una rentabilidad diagnóstica y terapéutica muy parecida a la de un oftalmólogo experto en el tema y además la dinámica de estos algoritmos posibilitan la mejora y el aprendizaje con los nuevos casos que se van incorporando a la base de datos creando algo similar a lo que llamamos “experiencia”.
este editorial, pero sí se pueden dar unas pinceladas.
En el ámbito de la córnea se ha permitido establecer programas de detección de córneas no patológicas, pero con elevado riesgo de serlo si son sometidas a técnicas de cirugía refractiva. Incluso ha llevado a pronosticar las posibilidades de resultado satisfactorio en cada caso dependiendo de los datos previos recogidos en el sistema.
En la cirugía de catarata, el uso del Big Data se ha incluido en proyectos de registros como EUROQUO (European Registry of Quality Outcomes for Cataract and Refractive Surgery), el IRIS de la Academia Americana de Oftalmología (Intelligent Research in Sight) o ICHOM (International Consortium for Health Outcomes Measurement). La información aportada en estos registros de la ingente base de datos relacionados con la cirugía de catarata ofrece la posibilidad de identifificar las fortalezas y debilidades de los diferentes protocolos quirúrgicos, conocer los resultados reales en concepto de valor salud de la cirugía, y fifinalmente determinar estrategias de política sanitaria en la técnica quirúrgica que presenta el mayor número de intervenciones quirúrgicas en oftalmología en el mundo.
En el glaucoma, se han aplicado básicamente técnicas de “aprendizaje profundo” (Deep Learning DL) para obtener la identifificación automática de las imágenes de fondo de ojo, papila y excavación papilar y con el análisis de la base de datos obtenidas establecer criterios de normalidad y patología.
En las uveítis, se han podido establecer DDSS (Diagnostic Decision Support Systems) o sistemas de soporte a la decisión diagnóstica que permiten hacer el diagnóstico diferencial de forma automática basándose en sistemas computadorizados de forma que faciliten la decisión clínica del médico. Un ejemplo claro de esto es el UVEMASTER (Leading SHT, A Coruña, España) desarrollado para diagnóstico diferencial y apoyo en la decisión terapéutica en uveítis basado en una aplicación móvil para iOS y Android.
En el campo de la retina, la IA ha tenido un papel fundamental en el cribado de retinopatía diabética (RD). En las últimas décadas, el envejecimiento de la población y el aumento de la prevalencia de sobrepeso ha aumentado el número de revisiones anuales de retinopatía diabética, aumentando la carga de los sistemas de salud. Existen softwares que ofrecen la detección automática de RD basándose en sistemas automáticos de análisis de imagen de la retina. Dos ejemplos son RETMARKER Ltd y EyeArt que han demostrado tener una sensibilidad en la detección automática de la RD de un 85% y 93% respectivamente, muy similar a la de un experto en diabetes ocular. Estos programas permiten reducir la necesidad menso potencial para hacer
del personal entrenado y ampliar el acceso al cribado a un mayor número de pacientes.
Para la degeneración macular asociada a la edad (DMAE) existen disponibles en la actualidad tres grandes sistemas de recogida de datos y análisis de Big Data. El registro IRIS (Intelligent Research in Sight) de la AAO, MEDISOFT (United Kingdom) y la plataforma online Fight Retinal Blindness (Australia). Estos tres registros ofrecen la posibilidad en la práctica clínica de analizar los resultados y los recursos destinados con el fin de poder modificar si es necesario el modelo de diagnóstico y tratamiento de la enfermedad.
La IA permite la segmentación automatizada de imágenes, el reconocimiento de patrones basados en árboles de decisión, la predicción de recurrencia y progresión más rápido que un humano y con una mayor base de datos como aprendizaje. Por ello, de la misma forma que se emplea la IA para analizar una imagen del fondo de ojo, se puede aplicar esta tecnología para analizar una tomografía de coherencia óptica macular en el caso de la degeneración macular asociada a la edad, otra patología que ha incrementado su prevalencia en las consultas de oftalmología debido a la mayor esperanza de vida de la pobla-
ción y a la disponibilidad de mejores tratamientos.
Como se puede ver hasta este momento la IA tiene un in una contribución positiva a la medicina y en especial a la oftalmología.
Y ahora surge la pregunta que está sobrevolando nuestras cabezas desde el primer abordaje de este tema: ¿la inteligencia artificial o las máquinas acabarán sustituyéndonos de forma definitiva?
El uso de IA y su aplicación a la salud conlleva una gran responsabilidad, tanto por el manejo de datos de pacientes como por la toma de decisiones sobre su diagnóstico y tratamiento.
Nick Bostrom, filósofo que dirige el Instituto para el Futuro de la Humanidad y el Centro de Investigación de Estrategia de Inteligencia Artificial de la Universidad de Oxford, es una de las voces más críticas con los riesgos de la IA. Afirma que “no es difícil pensar en una inteligencia artificial que sea cada vez más poderosa cuyos objetivos no estén perfectamente alineados con los objetivos humanos”. Por ello, dado su impacto sobre los pacientes debemos establecer unos límites éticos claros y unas pautas morales exquisitas a la hora de diseñar estos modelos matemáticos.
Debemos tener en cuenta que la ética no es inherente a la IA, pero sí es propia de los humanos y nos debe distinguir y hacer responsables de las consecuencias e implicaciones morales que puedan tener los sistemas de IA que empleemos.
El problema fundamental que (EU) 2017/745 sobre equipos plantea el uso de herramientas basadas en IA al médico, es la correcta defifinición de la interacción hombre-máquina. Esta interacción debe defifinir qué procesos se realizarán con algoritmos de IA y cuáles no, y el grado de fifiabilidad que se otorga a los resultados. Para ello, y como sucede con cualquier otra herramienta que utiliza el oftalmólogo, éste debe conocerla en profundidad, siendo perfectamente consciente de sus aplicaciones y de sus limitaciones y adaptar sus decisiones a estas capacidades.
Es un hecho que las herramientas basadas en IA presentan ciertas reticencias en parte de la comunidad médica. Y no sin razón. Por un lado, programas basados en IA, sobre todo aquellos que incluyen procesos con cierto grado de aprendizaje mediante la optimización de diversos parámetros se encuentran con la difificultad de interpretar correctamente las relaciones de causalidad, lo que puede dar lugar a resultados absurdos. Por otro lado, estos programas son vistos como una caja negra de la que se obtienen unos datos de difícil interpretación por alguien no experto en la materia.
Sin embargo, estas reticencias deberían disminuir, ya que el hecho de que este software sea considerado como un equipo médico, implica los mismos estrictos controles antes de su introducción en el mercado que otros equipos médicos similares. En el caso de la Unión Europea, el nuevo Reglamento médicos supone un refuerzo de estos controles incluyendo una mayor trasparencia y trazabilidad de los equipos. En esta misma línea, las revistas de publicaciones médicas están exigiendo revelar los datos usados en la evaluación de software que utilicen herramientas de IA de forma que los resultados puedan ser reproducidos.
Pero en todos los casos, en último término, siempre será la decisión de los oftalmólogos cuándo, cómo y en qué grado se introducirán estas nuevas herramientas en los procesos de diagnóstico y tratamientos oftalmológicos.
No se puede olvidar que la propuesta diagnóstica y la opción terapéutica determinada por la IA al final tiene como receptor no a otra máquina sino al paciente y la demanda de éste sigue siendo cada vez más la de una atención humana de medicina personalizada. Hoy por hoy el objeto de nuestro ejercicio profesional sigue siendo el enfermo y no la enfermedad.
El conocimiento de las posibilidades y los límites de esta tecnología, el entenderla como una herramienta de trabajo capaz de realizar tareas específicas que actualmente requieren la intervención humana aumentará la eficiencia de nuestra práctica clínica, reducirá nuestra participación en tareas rutinarias y facilitará la dedicación y el tiempo que dedicamos a tratar a nuestros pacientes que sigue siendo el fin último de nuestra profesión.

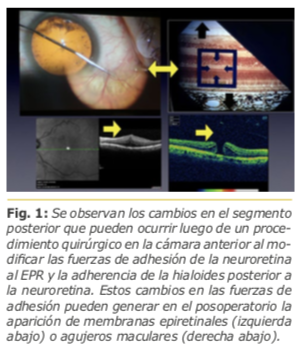
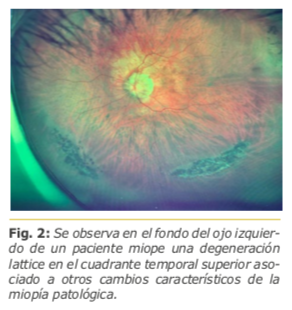
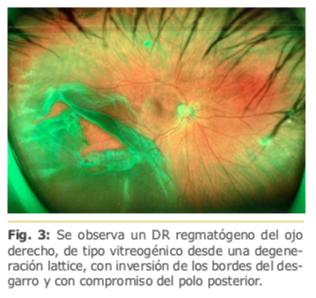





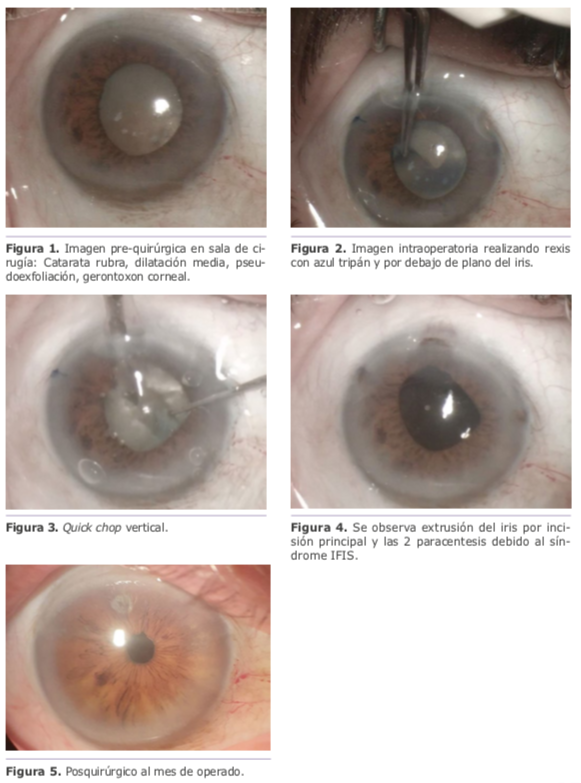

 Dra. Liana O. Ventura – Brasil
Dra. Liana O. Ventura – Brasil Dr. Marcelo C. Ventura – Brasil
Dr. Marcelo C. Ventura – Brasil
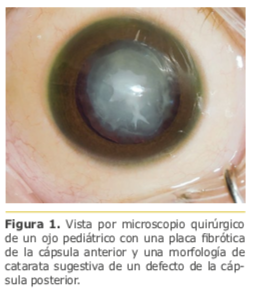
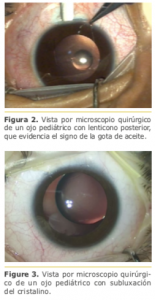





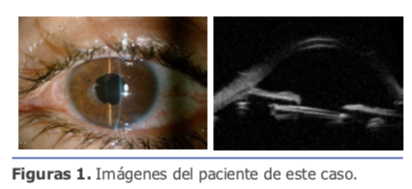
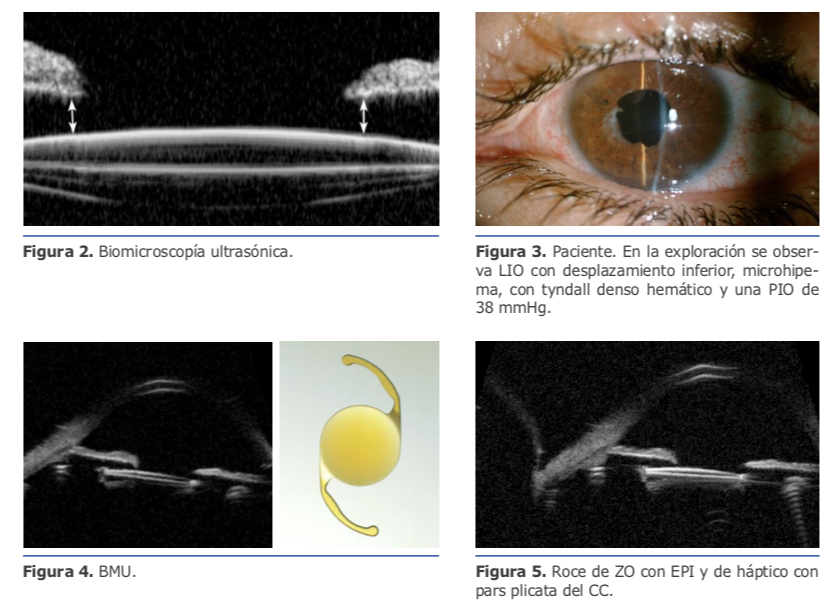
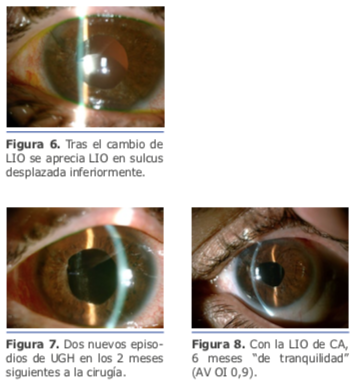 La sustitución de lente monobloque por una de 3 piezas no fue suficiente para una estabilización adecuada de la lente.
La sustitución de lente monobloque por una de 3 piezas no fue suficiente para una estabilización adecuada de la lente.

 Con estos avances tecnológicos los antiguos lentes esféricos fueron transformándose a lentes asféricos, y estos están evolucionando para alcanzar un mayor rango de visión extendida, es así como las plataformas AcrySof IQ Vivity de Alcon y TECNIS Eyhance de Johnson & Johnson han logrado ofrecer nuevas opciones de visión en el tratamiento de catarata y presbicia.
Con estos avances tecnológicos los antiguos lentes esféricos fueron transformándose a lentes asféricos, y estos están evolucionando para alcanzar un mayor rango de visión extendida, es así como las plataformas AcrySof IQ Vivity de Alcon y TECNIS Eyhance de Johnson & Johnson han logrado ofrecer nuevas opciones de visión en el tratamiento de catarata y presbicia.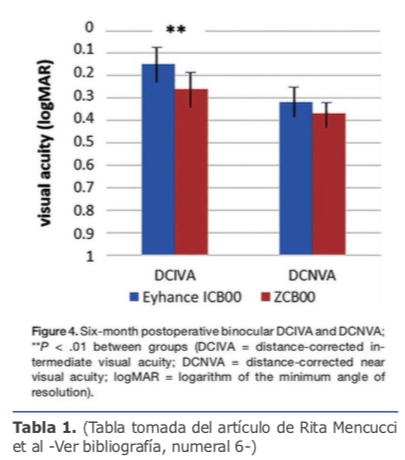 Esta tecnología logra un aumento local y continuo de potencia que va de la periferia hasta el centro de la óptica, el cual tiene una superficie posterior esférica y una superficie anterior asférica modificada, logrando una hiperprolatidad y con eso aumentar la profundidad del foco lo que proporciona una visión intermedia mejorada en comparación con una LIO monofocal asférica estándar.6 Según la compañía, las disfotopsias son comparables a una LIO monofocal asférica estándar pues compensan la aberración corneal asférica.
Esta tecnología logra un aumento local y continuo de potencia que va de la periferia hasta el centro de la óptica, el cual tiene una superficie posterior esférica y una superficie anterior asférica modificada, logrando una hiperprolatidad y con eso aumentar la profundidad del foco lo que proporciona una visión intermedia mejorada en comparación con una LIO monofocal asférica estándar.6 Según la compañía, las disfotopsias son comparables a una LIO monofocal asférica estándar pues compensan la aberración corneal asférica.



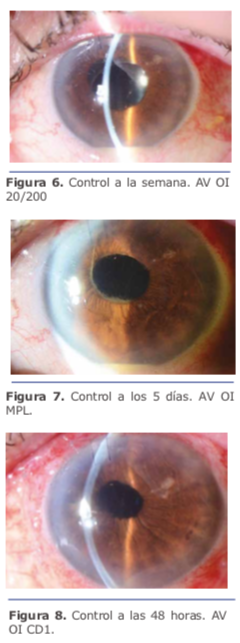

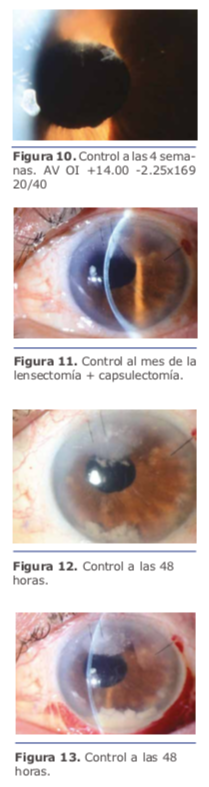
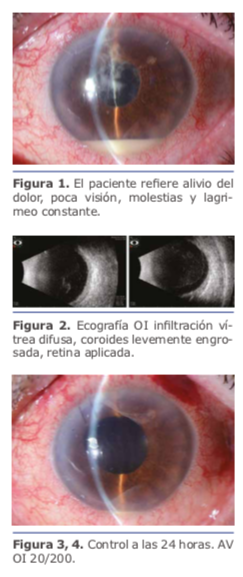
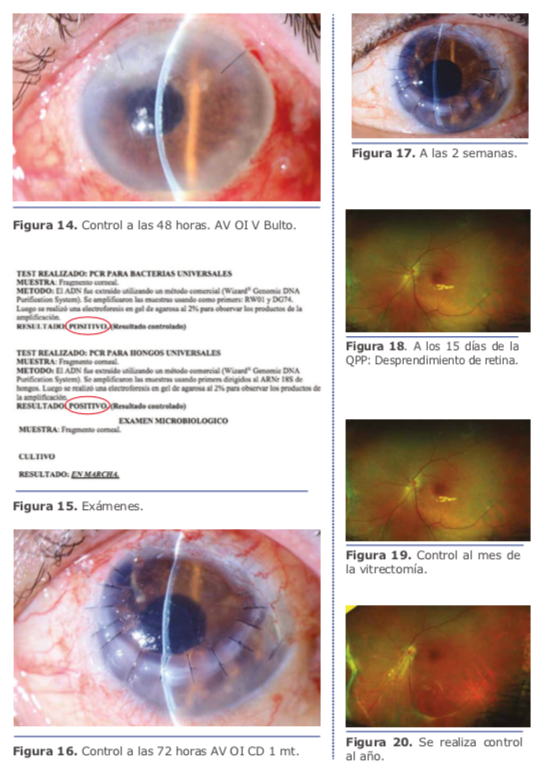 El manejo multidisciplinario del pa- ciente en cuestión por parte del Dr. Charles fue el correcto, lo único que se podría agregar al momento de la primera intervención en la toma de muestra es haber realizado una PCR
El manejo multidisciplinario del pa- ciente en cuestión por parte del Dr. Charles fue el correcto, lo único que se podría agregar al momento de la primera intervención en la toma de muestra es haber realizado una PCR
