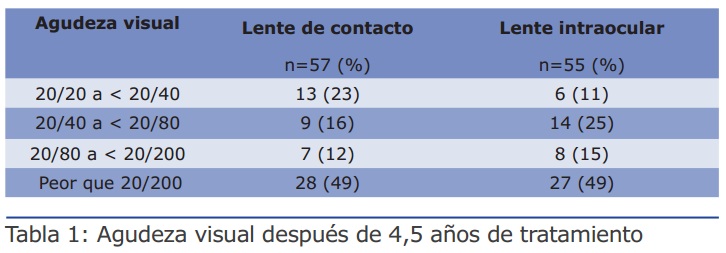
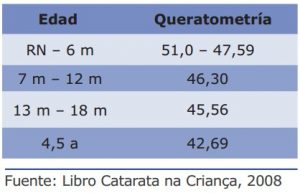
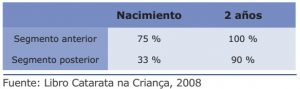
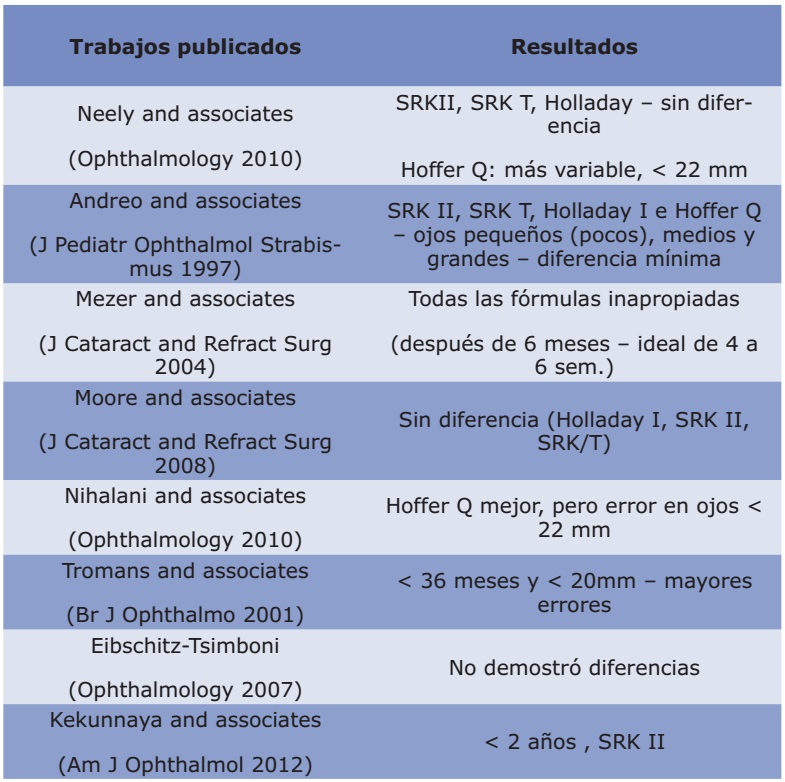
Caso Catarata:
Cirugía de cristalino con láser de femtosegundo en subluxación del cristalino
Coordinadora
Dra. Bruna Ventura – Brasil
Panelistas
Dr. Mauro Campos – Brasil
Dr. Cesar Carriazo – Colombia
Datos de Contacto
Dra. Bruna Ventura – brunaventuramd@gmail.com
Dr. Mauro Campos – mscampos@uol.com.br
Dr. Cesar Carriazo – ccarriazo@carriazo.com
Introducción
Los casos de subluxación del cristalino pueden estar asociados a condiciones sistémicas, como el síndrome de Marfan, la homocistinuria y el síndrome de Weill-Marchesani. La subluxación del cristalino comúnmente resulta en eje visual parcialmente fáquico y error refractivo importante, frecuentemente con altos astigmatismos lenticulares y anisometropia.
La cirugía del cristalino en esos ojos tiene dos grandes desafíos: la confección de la capsulorrexis y la centralización del complejo bolsa capsular/lente intraocular (LIO). La capsulorrexis consiste en un desafío, una vez que generalmente hay una elasticidad aumentada de la cápsula anterior y una disminución de la contra-tracción al hacer la capsulorrexis con pinza de utrata, debido a la fragilidad zonular.
Caso clínico
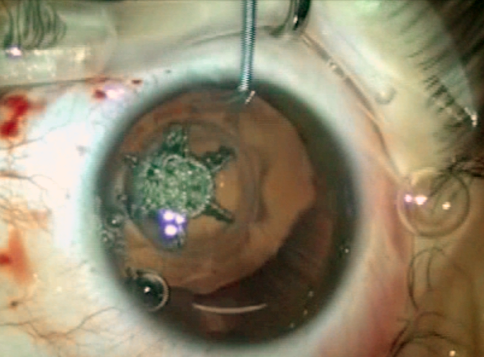
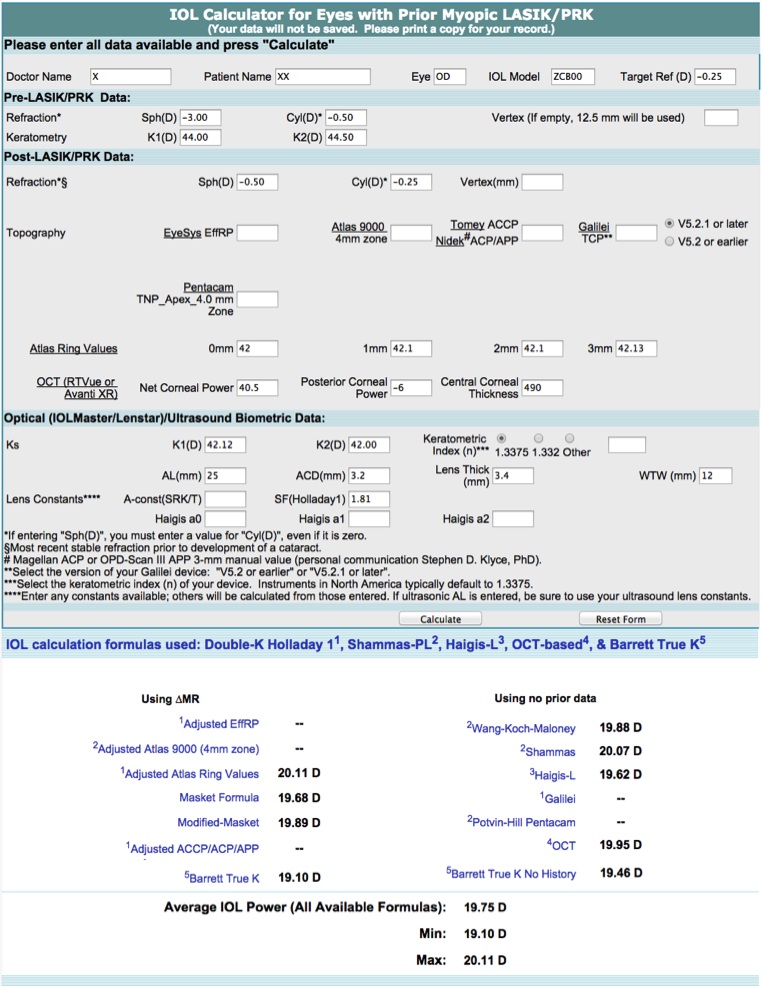
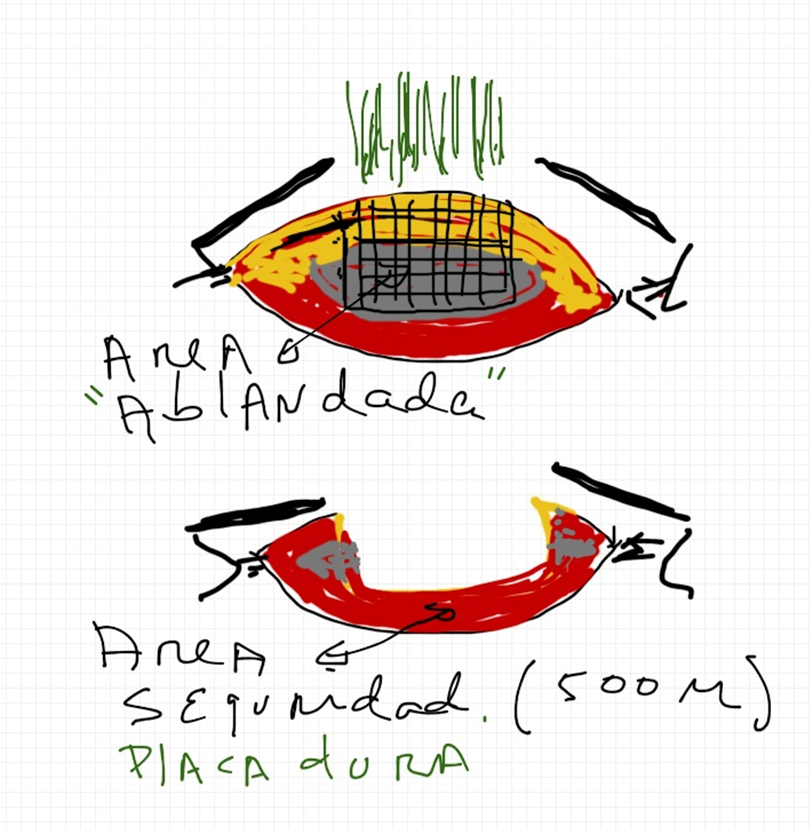
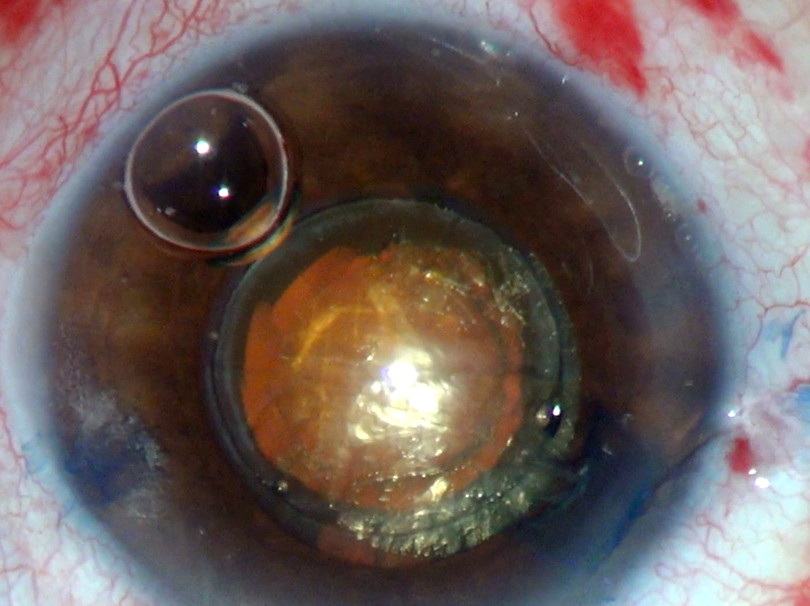
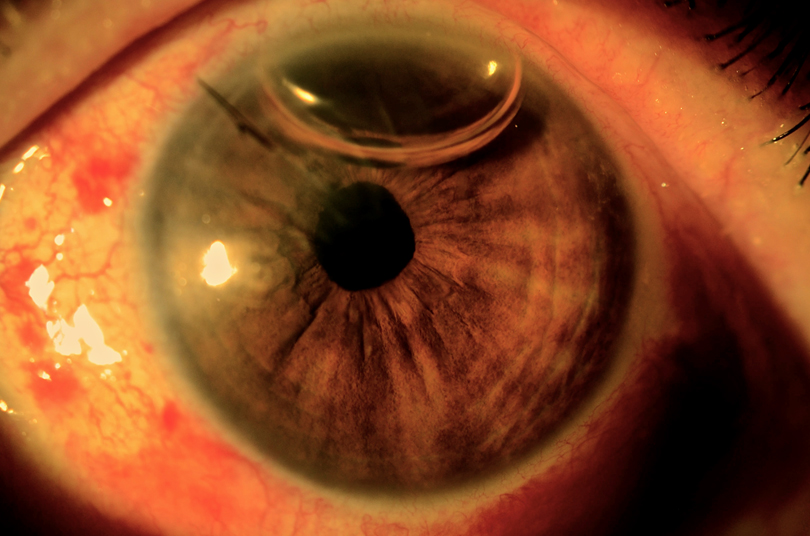
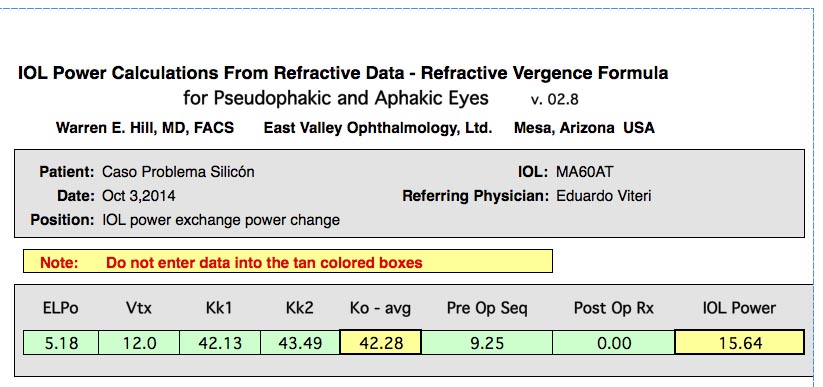
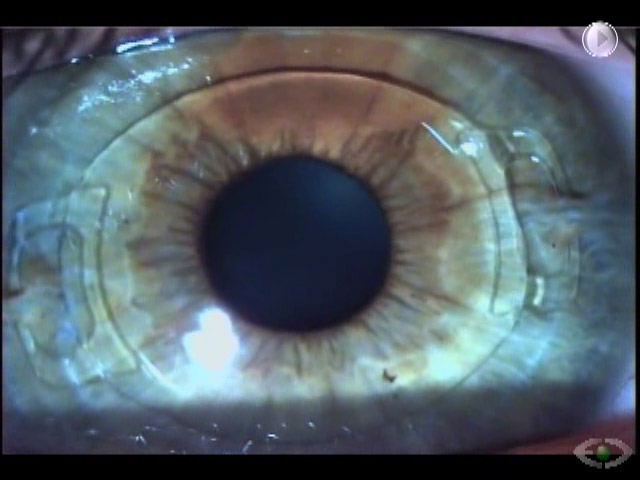
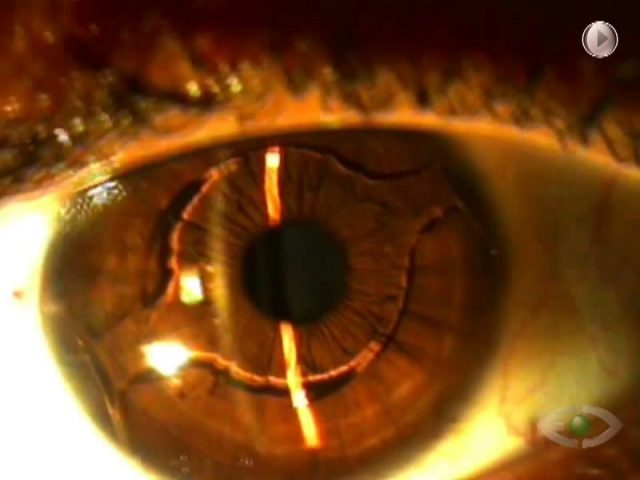
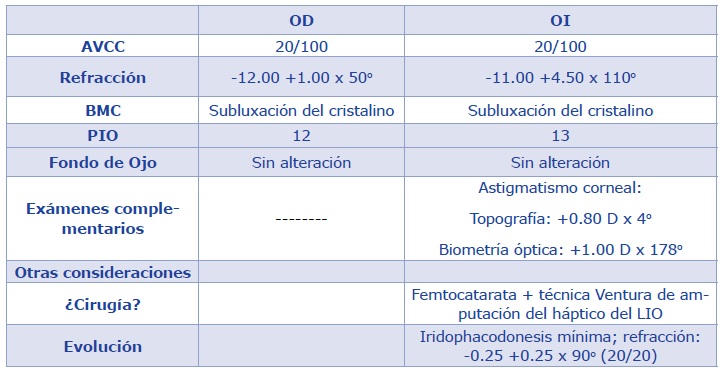
Se presenta un caso de una paciente femenina de 19 años con subluxación del cristalino en ambos los ojos (AO) (Figura 1). Su mejor agudeza visual era de 20/100 en AO con una refracción de -12.00 +1.00 x 50o en ojo derecho (OD) y -11.00 +4.50 x 110o en ojo izquierdo (OI). Decidimos operar primero su OI. En este ojo, tenía un astigmatismo corneal de +0.80 dioptría (D) x 4o medido por el topógrafo y de +1.00 D x 178o medido por el biómetro óptico.
Preguntas para los invitados:
1. En estos casos de subluxación de cristalino, su primera opción de abordaje para ayudar en el desafío de la confección de la capsulorrexis es utilizar el láser de femtosegundo o prefiere seguir con la técnica de facoemulsificación convencional, utilizando pinza de utrata?
2. ¿Cuál(es) es(son) su(s) estrategia(s) preferida(s) para centralizar el complejo bolsa/LIO en esos casos?
3. Cuando el láser de femtosegundo surgió en el mercado, muchos médicos cuestionaron la resistencia de la capsulotomía hecha por el láser y el riesgo de tener una rotura radial al inserir un anillo endocapsular. Yo nunca tuve esa complicación. Hay trabajos en la literatura enseñando que las actualizaciones en los softwares de las distintas plataformas resultaron en una disminución significativa de tags y roturas radiales. Un trabajo recién publicado incluso mostró que el LenSx, después de la inclusión del SoftFit, produce capsulotomías con características muy semejantes a las capsulorrexis manuales. Además, el término de la curva de aprendizaje también es un factor importante. ¿Usted ya tuvo una rotura radial al poner un anillo endocapsular después de hacer una capsulotomía con el láserde femtosegundo?
4. ¿En ese caso, consideraría algún abordaje quirúrgico para disminuir el astigmatismo refraccional final?
Dr. Mauro Campos
Se trata de un paciente con subluxación del cristalino relacionado probablemente al síndrome de Marfan. En este caso el cirujano eligió utilizar el láser de femto, el anillo intracapsular y la amputación del háptico (técnica de Ventura). El paciente presentó en el posoperatorio reciente un excelente resultado anatómico y funcional. No se brindó información sobre el poder dióptrico del LIO.
- En los casos de subluxación en paciente jóvenes es indicado el uso del láser de femto. Con esta tecnología es posible centrar la rexis con mejor control sobre la posición real del lente intraocular en el posoperatorio. Por ser un paciente joven y, probablemente, por tener una cápsula más elástica, la rexis manual es siempre un desafío. Además, la tracción manual puede aumentar el estrés zonular y ampliar la luxación.
- Realizaría la rexis un poco más amplia de lo que normalmente haría en un caso de catarata sin luxación. Dependiendo del implante que será utilizado, posicionaría el centro de la rexis. Si, como en el caso anterior, adopto la amputación del háptico, parece adecuado descentrar la rexis hacia el lado de la amputación. Rutinariamente centraría la rexis lo más cerca posible del área visible del cristalino. La utilización de rexis igual o mayor de 6 mm puede reducir el riesgo de contracción capsular.
- Hacemos la faco hace cerca de 6 meses y hasta ahora no tuvimos accidentes con la rexis. Las plataformas de femto más actuales realizan la rexis de manera más confiable
- No planificaría la reducción del cilindro en este caso, aun con incisiones relajantes.
Observaciones personales: La enfermedad zonular en el caso presentado es progresiva. Eso no significa necesariamente que el paciente tendrá luxación progresiva del saco-LIO, pero es una posibilidad que se debe considerar. Así, en este caso, me parece fundamental conocer la biometría. En caso de que el poder dióptrico da la LIO estuviera próximo de cero, elegiría la afacia.
Reconozco a la técnica Ventura como una solución interesante, pero no dejaría la punta del háptico como aparece en el video. La punta no debería tener una terminación perforante. Sugiero calentar la extremidad del segmento amputado para reducir el riesgo de perforación y posterior descentración del LIO.
Felicito a los autores por la excepcional resolución del problema.

Dr. Cesar Carriazo
- Actualmente todos mis casos de debilidad zonular los hago con la tecnología de femtosegundo, ya que de esta manera el estrés zonular es mínimo y se puede planear mejor la cirugía.
Esta máquina permite descentrar la capsulorrexis si se quisiera recentrar todo el complejo lenticular que está desplazado. - En estos casos descentro la capsulorrexis con el femtofaco ligeramente, realizo una faco con parámetros bajos manteniendo y vigilando el saco capsular con un gancho manipulador, y una vez terminada la faco y habiendo aspirado todos o casi todos los restos corticales introduzco un anillo de tensión capsular. Corto parcialmente el háptico del lente y lo hiperflexiono a tener contacto con la óptica del lente. Esto hace que pierda la mayor parte de la memoria tensil de ese lado. Luego, lo introduzco y lo centro en el saco. Esta es la técnica de Ventura con una ligera modificación que me ha permitido además del recentramiento una buena estabilización.
Por norma siempre busco solucionar los problemas de la forma más fisiológica y con la técnica descrita estamos centrando el lente, pero el complejo bolsa capsular/LIO continúa descentrado e inestable. Por esta razón lo que idealmente y fisiológicamente debe ser la conducta correcta es fijar uno de los hápticos en el sitio de mayor estrés zonular. Esto daría mayor tranquilidad para el futuro de estos pacientes jóvenes. Pero esta técnica implica un mayor reto quirúrgico y aumenta el riesgo de complicación intraoperatoria. - Uso la plataforma Catalys, que es muy estable y predecible. Nunca he tenido rotura radial habiendo hecho la capsulotomía con este femto. Debo anotar que estoy usando el láser hace poco tiempo y son muy pocos los pacientes a los que les he tenido que poner anillos de tensión cápsular.
- Sí. Aunque el astigmatismo es bajo, es contra la regla, por lo que durante el mismo procedimiento programaría la corrección astigmática haciendo una incisión relajante intraestromal.

Resolución del caso por la Dra. Bruna Ventura:
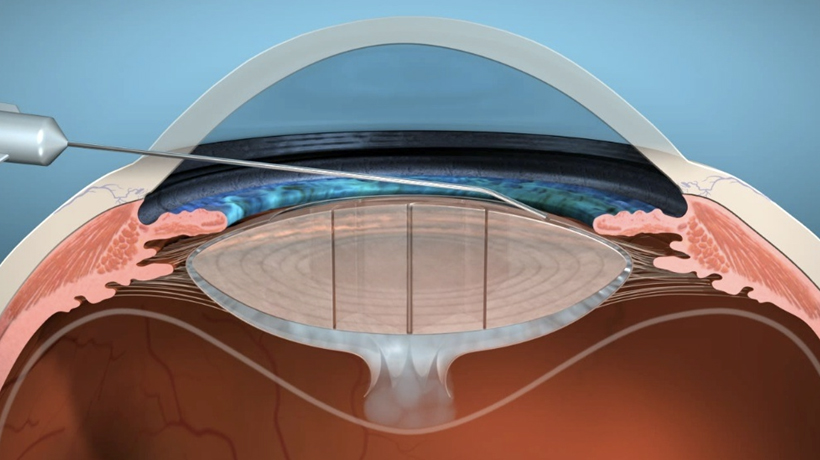
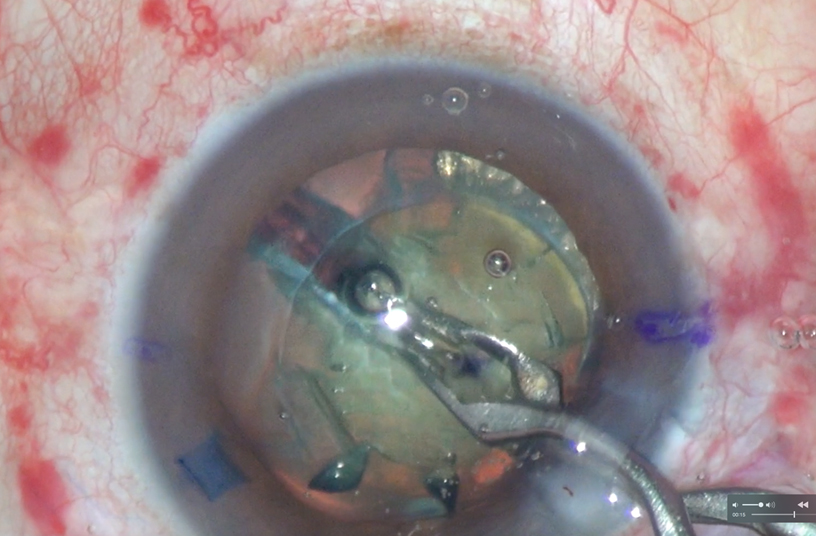
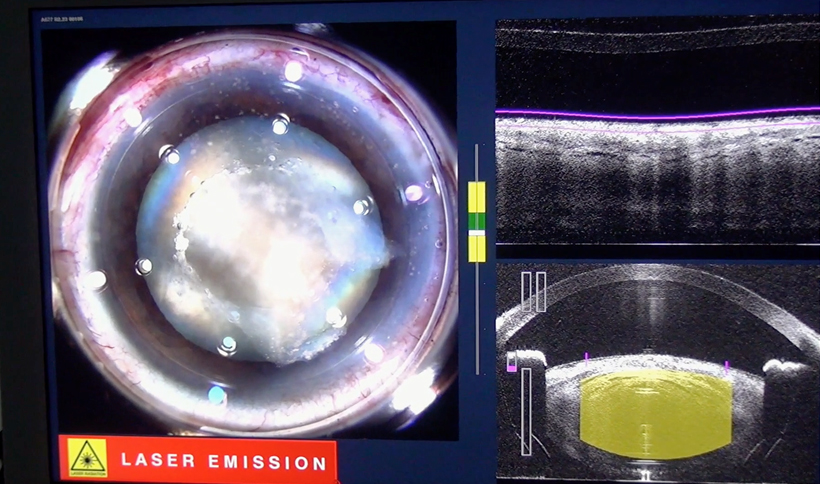
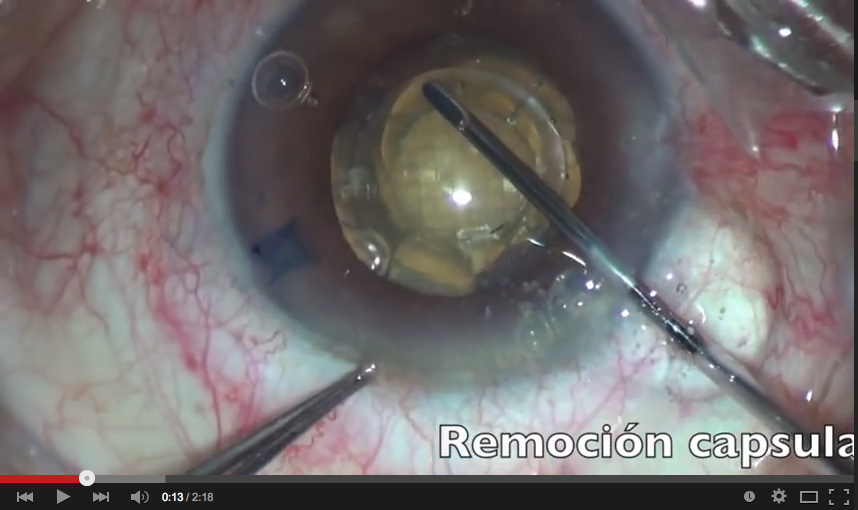
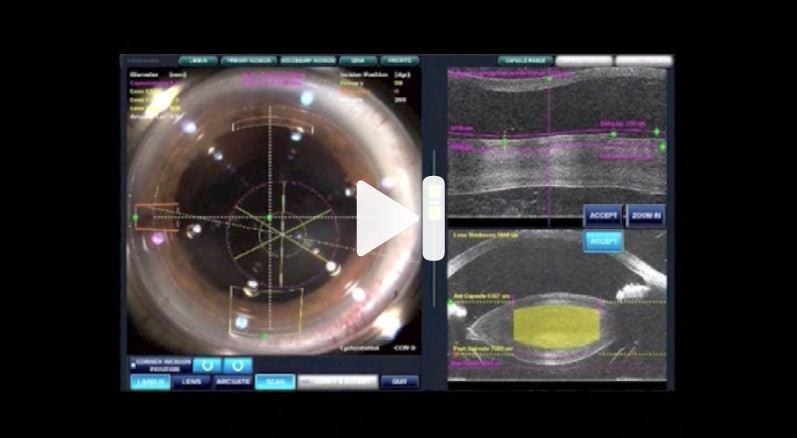
En este caso decidimos utilizar el láser de femtosegundo asociado a la técnica Ventura de amputación del háptico del LIO (Video). El láser de femtosegundo: 1) permite hacer la capsulotomía de forma descentrada en relación al limbo para que se quede más centrada en relación al cristalino subluxado; 2) no tracciona la zónula restante durante la confección de la capsulotomía, y 3) puede hacer incisiones relajantes en la córnea para disminuir el astigmatismo corneal. En el caso presentado, hicimos la incisión principal en el eje más curvo de la córnea y una incisión relajante intraestromal de 45o a 180˚ de la incisión principal. Con este abordaje, el astigmatismo refraccional de la paciente disminuyó de aproximadamente +1.00 D contra la regla para +0.25 D x 90o.
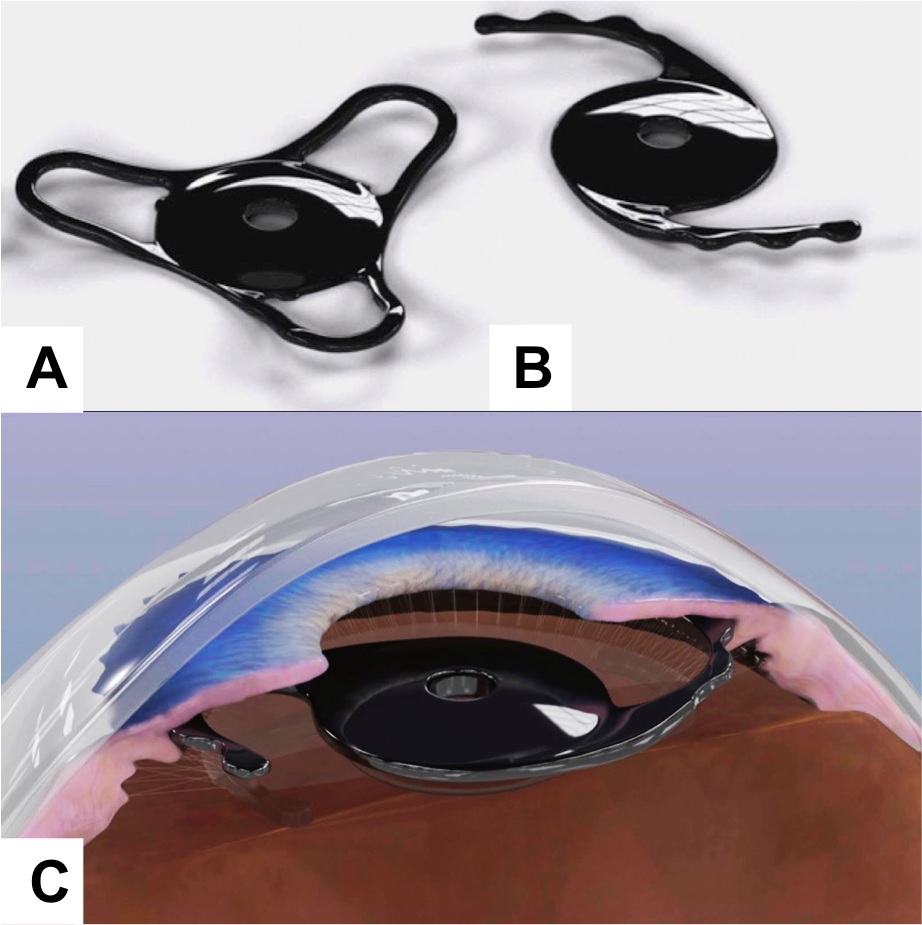
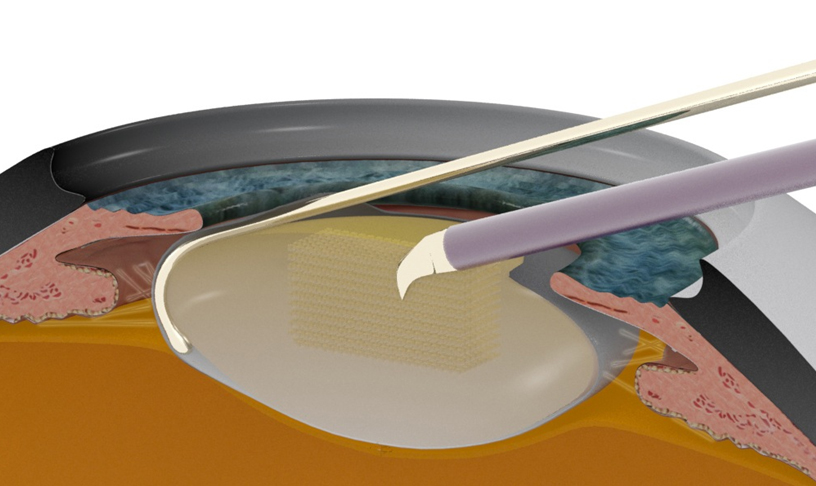
La técnica Ventura de amputación del háptico del LIO está bien descrita en la literatura. En esta técnica insertamos un anillo endocapsular para expandir el saco capsular en sus 360˚ y para relajar la zónula, disminuyendo así el estrés en la zónula restante. Pensamos que este procedimiento estabiliza mejor el saco, evita descentración y progresión de la debilitación zonular. La amputación de uno de los hápticos de un LIO hidrofóbico de tres piezas tiene el objetivo de descentrar el LIO dentro del saco capsular, aproximando uno de los bordes del lente al anillo endocapsular, centrando así el lente en el eje visual, a pesar del saco todavía descentrado anatómicamente.
En el primer día de posoperatorio, la paciente presentó iridofacodonesis mínima y el LIO estaba ocupando todo el eje visual. Tres semanas después, la paciente tenía una agudeza visual de 20/20 con una refracción de -0.25 +0.25 x 90o.