Mi peor caso córnea ref ractiva
Coordinadores:
 Dr. Arturo Ramírez Miranda – México
Dr. Arturo Ramírez Miranda – México
arturorammir@gmail.com
 Dra. Norma Morales Flores –México
Dra. Norma Morales Flores –México
normamoralesf@gmail.com
Panelistas:
 Dr. Julio Hernández Camarena – México
Dr. Julio Hernández Camarena – México
dr.jcesarhc@gmail.com

Dr. José Miguel Varas
Dr. José Miguel Varas – Ecuador
jm@varas.com
 Dr. Antonio Méndez Noble – México
Dr. Antonio Méndez Noble – México
Descripción del caso
Paciente femenino de 27 años, levantadora de pesas, sin otros antecedentes de importancia, acude a cita de revisión por antecedente de SMILE en ambos ojos hace 8 meses. Refiere que la visión del ojo izquierdo ha ido disminuyendo progresivamente. Su visión preoperatoria era de 20/400 en ojo derecho que mejoraba a 20/25 con una refracción de -6.00 =-4.00 x 30 y de 20/400 en ojo izquierdo que mejoraba a 20/25 con una refracción de -5.75=-4.00 x 150.
Se realizó una topografía tipo Scheimpflug sin hallazgos de importancia por lo cual se realizó SMILE con láser femtosegundo VisuMax (VisuMax, Carl Zeiss Meditec, Jena, Germany) a una densidad de energía de 150nJ, grosor de cap de 160μm, zona óptica de 6.00 mm, corte corneal de 2.20mm y estroma residual de 270μm en el ojo derecho, y en el ojo izquierdo grosor de cap 140μm, zona óptica de 6.00mm, corte corneal de 2.20mm y estroma residual de 268μm.
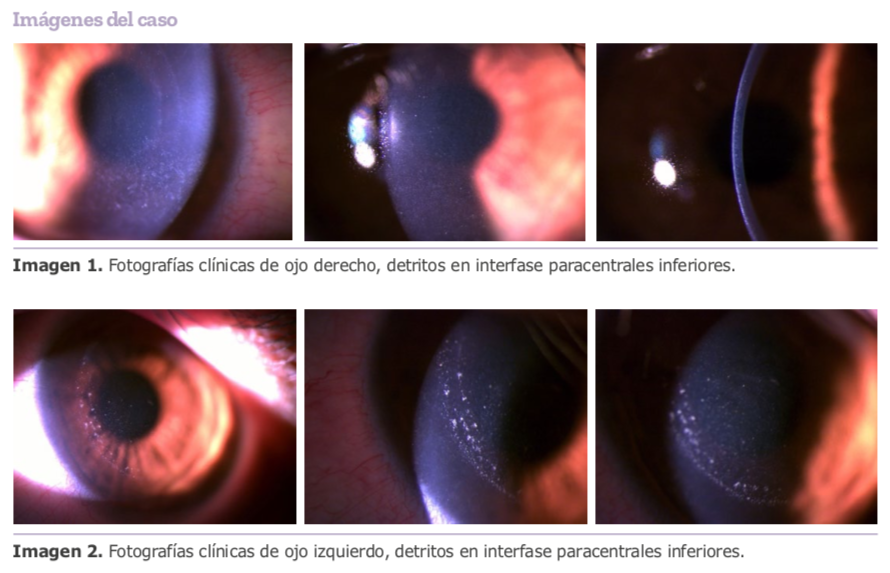
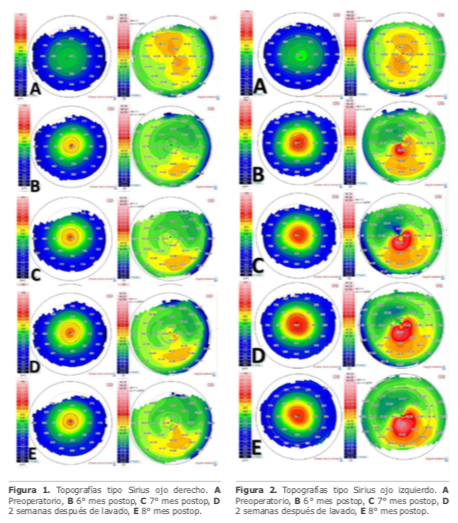
La evolución del paciente fue favorable, sin embargo, desde el sexto mes se encontró una disminución en agudeza visual de ojo izquierdo asociado a un encurvamiento inferior en el mapa queratométrico y a unos detritus a lo largo del borde inferior de la interfase en ambos ojos. Se decidió hacer un lavado de interfase con dexametasona de ojo izquierdo para descartar asociación de detritus en interfase con la disminución de la visión y las alteraciones topográficas. A las dos semanas del lavado hubo una ligera mejoría en la visión y en la refracción, sin embargo, regresó a valores previos al mes del lavado. Actualmente con una agudeza visual de 20/50 en ojo derecho y 20/200 en ojo izquierdo que mejora a 20/20 con una refracción de -1.00 =-1.00 x 90 y 20/50 con -0.50 =-7.25 x110 respectivamente. En la topografía es evidente la progresión del encurvamiento inferior en el ojo izquierdo por lo cual se realiza diagnóstico de ectasia post SMILE.
Presentación del caso
|
OD |
OI |
|
|
AVSC |
20/50 |
20/200 |
|
AVCC |
20/20 |
20/50 |
|
Refracción |
-1.00=-1.00 X 90 |
-0.50=-7.25 X 110 |
|
BMC |
Imagen 1A |
Imagen 2A |
|
PIO |
16 mmHg |
15 mmHg |
|
Fondo de Ojo |
Retina aplicada, papila redonda naranja bordes definidos, excava- ción 35%, anr conservado, macula con brillo. |
Retina aplicada, papila redonda naranja bordes definidos, excava- ción 35%, anr conservado, macula con brillo. |
|
Exámenes comple- mentarios |
Topografía corneal. OCT segmento anterior. |
Topografía corneal. OCT segmento anterior. |
|
Otras consideraciones |
||
|
¿Cirugía? |
SMILE 8 meses antes |
SMILE 8 meses antes |
|
Evolución |
Tabla 1 |
Tabla 1 |
Preguntas.
1. ¿Considera usted que SMILE es una cirugía que previene la ectasia, o una cirugía que puede realizarse si el paciente tiene contraindicado el LASIK o el PRK por parámetros clínicos y/o topográficos?
Dr. Julio Hernández Camarena: No. En la cirugía SMILE, como en toda cirugía corneal refractiva donde se utiliza láser excímer o femtosegundo, existe un porcentaje de tejido corneal “alterado” y no está exenta de complicaciones como la ectasia corneal. Si el paciente ha mostrado alteraciones topográficas o tomográficas (por más leves o discretas que estas sean) en el examen preoperatorio y estas lo hacen un candidato con alto riesgo de complicaciones (ectasia) para LASIK o PRK, también representarán un criterio de riesgo para la cirugía de extracción de lentícula refractiva por incisión pequeña (SMILE).
Habrá que recordar, que los hallazgos topográficos anormales (asimetría inferior en mapa axial, pérdida de la ortogonalidad, alteraciones en el patrón de progresión paquimétrica central-periférico y/o alteraciones de los mapas de elevación corneal) representan un marcador subrogado de patología corneal (alteración biomecánica corneal); por tanto, la intervención con cirugía corneal refractiva con láser excímer o femtosegundo estará potencialmente contraindicada.
Dr. José Miguel Varas: El SMILE no es una variante substractiva que prevenga la ectasia.
En cirugía refractiva corneal hay dos grandes conceptos: el primero es constatar que la córnea guarde un fenotipo libre de características ectásicas. El segundo, habiendo pasado la primera prueba, es conocer el límite de substracción seguro para hacer un tratamiento.
En ambos puntos de análisis: el que descarta o confirma preexistencia de enfermedad y el segundo que calcula la máxima tolerancia que una córnea sana permite ser modificada sin pérdida progresiva de su estabilidad biomecánica. Se conoce que los procesos de decisión cambian según los niveles de sensibilidad a los que la prueba esté diseñada.
Al tratarse de ojos previamente sanos, es preferible aumentar la sensibilidad de los tamizajes y dejar por fuera a algunos candidatos que pecar por lo contrario y operar a casos inadecuados no detectados.
 En candidatos para LASIK o PRK que han pasado las pruebas fenotípicas hay estudios retrospectivos que sugieren límites para establecer riesgos de ectasia. Un ejemplo de ellos es el PTA (Percentage of Tissue Altered) de Santhiago y cols., donde establecen que sobrepasar aquel índice aumenta el riesgo de ectasia. (Más de 100:1, observación de casuística personal).
En candidatos para LASIK o PRK que han pasado las pruebas fenotípicas hay estudios retrospectivos que sugieren límites para establecer riesgos de ectasia. Un ejemplo de ellos es el PTA (Percentage of Tissue Altered) de Santhiago y cols., donde establecen que sobrepasar aquel índice aumenta el riesgo de ectasia. (Más de 100:1, observación de casuística personal).
En el SMILE hemos adoptado el índice de fuerza tensil residual descrito por Reinstein y cols., sin embargo, ese número aún no tiene un límite similar al clínicamente estudiado retrospectivamente como el PTA.
Por otro lado, en las imágenes adjuntas se desconoce si hay enmascaramiento epitelial, el comportamiento de la altura de la cara posterior y la curvatura de los mapas gaussianos de la cara posterior de dichas córneas. Todas ellas en conjunto proveen valiosísima información fenotípica complementaria que ayudan a determinar si existía sospechas pre-existentes.
Dr. Antonio Méndez Noble: De los grupos de técnicas para la corrección de la visión con láser, se ha demostrado que SMILE es el procedimiento que más respeta la biomecánica corneal. Este efecto no nos da ninguna protección para evitar o prevenir una ectasía corneal. Así que de ninguna manera SMILE previene o evita una ectasía corneal.
Debemos de ser igual de estrictos para elegir al paciente para SMILE como lo hacemos para PRK y LASIK. Un caso de SMILE mal indicado puede inducir una ectasia corneal como cualquier otro procedimiento refractivo por ablación.
2. ¿Qué abordaje clínico utilizaría ante este paciente? ¿Cómo abordaría las expectativas del paciente ante esta situación clínica?
Dr. Julio Hernández Camarena: Es como bien lo dice el título, un caso difícil. En primera instancia habría que hablar de las expectativas del paciente, ya que al menos de manera mediata será muy difícil limitar la independencia de su agudeza visual de una corrección óptica (armazón, lentes de contacto escleral) y es importante hacerle entender esta situación. Posteriormente, habrá que incidir sobre la progresión de la patología que estamos actualmente (ectasia corneal), comprender que se necesita de un tratamiento que limite o arreste esta progresión de manera inmediata (crosslinking corneal). Una vez logrado esto, asegurando la estabilidad topográfica en el tiempo (6 meses – 1 año, como mínimo) y dependiendo de la refracción corneal y capacidad visual con corrección, se podría ofrecer una alternativa no corneal para la corrección del error refractivo (lente intraocular fáquico, i.e., ICL).
Dr. José Miguel Varas: Debido a la evidencia de progresión de la ectasia, el primer recurso es la reticulación del colágeno corneal en ambos ojos aprovechando el bosillo estromal existente. Observar durante el primer año antes de plantear una segunda alternativa terapéutica.
Dr. Antonio Méndez Noble: No es raro ocasionalmente ver detritus en la interfase en casos de SMILE, así como se ven después de LASIK, con la experiencia y depuración de la técnica estos van disminuyendo. En casos en los que sospechamos que afectan la visión está indicado lavado de interfase, así como se realizó en este caso. Sin embargo, esto es totalmente independiente a los cambios topográficos que nos indican una ectasia post SMILE.
Es importante, como en todos los casos de ectasia, después de cirugía refractiva verificar nuestra historia clínica y ver cómo lo podríamos evitar otro caso semejante. Dos datos me llaman la atención: el hecho de que la paciente no mejora al 20/20 con su corrección preparatoria y en su topografía corneal observamos un patrón en moño oblicuo con queratometrías altas predominio ojo izquierdo. Esto hoy me hace interrogar más al paciente por estabilidad en su refracción. Inclusive en casos con buenas paquimetrías como en este caso. Si no tenemos los datos, esperar un año, repetir refracción y topografía.
Tenemos que interrogar al paciente si tiene la costumbre de frotarse los ojos o de dormir presionándolos. Esto se ha asociado a progresión de la ectasia corneal.
Otro factor interesante a revisar es, que personas que hacen fisicoculturismo pueden tomar medicamentos controlados que influyen en el metabolismo llegando a afectar la rigidez corneal. Yo interrogaría más a la paciente y la orientaría en caso de ser necesario.
Ahora qué hacer con la ectasia corneal, yo optaría por un entrecruzamiento de collagen corneal (CXL) y uso de lentes de contacto permeables al gas. Verificar estabilidad al año. Aunque la paciente tenía la expectativa de no requerir anteojos, con los lentes de contacto permeables al gas mejoramos la calidad de su visión. Una vez confirmada la estabilidad de su ectasia corneal, posiblemente valoraría implantar un segmento intraestromal.
Conclusión del caso
SMILE ha demostrado tener algunas ventajas teóricas sobre LASIK como mayor estabilidad de la superficie ocular, menos exposición del estroma y una mayor fuerza biomecánica residual. Sin embargo, continúa siendo una técnica sustractiva que no es exenta de tener riesgo de ectasia. En teoría el SMILE preserva el 60% del colágeno del estroma anterior lo cual debería de tener un menor impacto en las propiedades biomecánicas de la córnea. A pesar de esto, ya existen algunos reportes de caso, como el que se presenta, donde hay evidencia de ectasia posterior al procedimiento. Por lo tanto, la evaluación preoperatoria de los pacientes que serán sometidos a SMILE debe de ser al menos igual de estricta como para LASIK.
REFERENCIAS
- Wang Y, Cui C, Li Z, Tao X, Zhang C, Zhang X, et al. Corneal ectasia 6.5 months after sma- ll-incision lenticule extraction. Journal of Ca- taract & Refractive Surgery. 2015;41(5):1100-6.
- Titiyal J, Kaur M, Shaikh F, Gagrani M, Brar A, Rathi A. Small incision lenticule extrac- tion (SMILE) techniques: patient selection and perspectives. Clinical Ophthalmology. 2018;12:1685-99.
- Damgaard IB, Reffat M, Hjortdal J. Review of Corneal Biomechanical Properties Fo- llowing LASIK and SMILE for Myopia and Myopic Astigmatism. Open Ophthalmol J. 2018;12:164-74.
- Agca A, Ozgurhan EB, Demirok A, Bozkurt E, Celik U, Ozkaya A, et al. Comparison of cor- neal hysteresis and corneal resistance factor after small incision lenticule extraction and femtosecond laser-assisted LASIK: a prospec- tive fellow eye study. Cont Lens Anterior Eye. 2014;37(2):77-80.
- Moshirfar M, Albarracin JC, Desautels JD, Birdsong OC, Linn SH, Phillip SCH. Ectasia following small-incision lenticule extraction (SMILE): a review of the literature. Clinical Ophthalmology. 2017;11:1683



 Dr. Juan J. Mura – Chile
Dr. Juan J. Mura – Chile Dr. Alex León – Chile
Dr. Alex León – Chile Dr. Víctor L Pérez – EE.UU.
Dr. Víctor L Pérez – EE.UU. Dr. Matías Soifer – EE. UU.
Dr. Matías Soifer – EE. UU.









