Diagnóstico de ectasia con sistema avanzado de obtención de imágenes de la córnea

Renato Ambrósio Jr, MD, PhD1,2,3,4
Brasil
El diagnóstico de ectasia corneal ha evolucio- nado enormemente en las últimas dos décadas por dos motivos sencillos: (1) la selección de ca- sos con gran susceptibilidad a la progresión de la ectasia tras procedimientos electivos de cor- rección de la visión por láser (LVC, laser vision correction),1 y (2) la llegada de procedimientos alternativos a trasplantes de córnea como con- secuencia de enfermedades ectásicas corneales (ECD, ectatic corneal diseases).2,3 En realidad, el surgimiento de procedimientos quirúrgicos no convencionales, como el crosslinking cor- neal, los segmentos de anillos intracorneales (ICRS, intracorneal ring segments) y las abla- ciones terapéuticas personalizadas por ECD han creado la necesidad no solamente de identi car los casos que se bene ciarían con tales proced- imientos, sino también de plani carlos. De he- cho, a pesar de que hemos roto el paradigma relacionado con la cirugía para ectasia,4 aún enfrentamos las paradojas de cuándo, cómo y por qué decidimos una cirugía en tales casos. Por eso es fundamental disponer de sistemas avanzados de imágenes de la córnea.
Amsler fue quien lideró el trabajo de detec- ción de formas leves de queratocono durante la primera mitad del siglo pasado, época en la que se acuñó el término “forme fruste keratoco- nus” (FFKC), o queratocono forma frustro.5,6 Sin embargo, el trabajo de Amsler con fotoquera- toscopía con disco de Plácido no ha recibido mucha atención debido a la falta de relevan- cia clínica relatada para detectar casos leves de queratocono y ECD. Además, el método era muy complicado, lo que di cultaba su reproducción por otros. Lo curioso es que, cuando la cirugía refractiva surgió como una nueva subespeciali- dad, quedó evidente la necesidad de incluir un análisis completo de la forma de la córnea para
evaluar a los pacientes antes y después de tales procedimientos. Además, las descripciones de ectasia progresiva (queratectasia) como com- plicación grave de procedimientos queratorre- fractivos,7 estableció la necesidad de detectar casos leves de ectasia. La introducción de tec- nologías computarizadas de videoqueratografía a mediados de la década de 1980 permitió el desarrollo de la topografía corneal (Figura 1).8 Varios índices topográ cos, como los que Ra- binowitz y McDonnell describieron en 1989, se crearon para la detección de queratocono.9 Lo interesante es que estos datos hicieron posible que se identi caran cambios ectásicos leves an- tes de la presentación de otros signos clínicos por lámpara de hendidura que, de lo contrario, podría llevar a la pérdida de la agudeza visual lejana sin corrección con gafas (AVLCC).10,11 Di- cha capacidad ha sido el argumento más im- portante para justi car el uso de la topografía corneal como examen obligatorio en la selec- ción de candidatos a cirugía refractiva antes de procedimientos LVC.12
 La búsqueda y la necesidad de ir más allá de la topografía corneal resultaron obvias debido al mayor número de pacientes que padecían ec- tasia pese a una topografía normal y la ausen- cia de otros factores de riesgo aparentes.13,14 Además, los casos de córneas irregulares que habrían sido excluidas de una cirugía en función de las características de la super cie anterior, pero cuyo LASIK no presentó complicaciones y cuyos resultados fueron estables, demuestran la necesidad de una mejor especi cidad.15 De este modo, es indiscutible la necesidad de me- jorar la sensibilidad y la especi cad cuando se considera realizar un diagnóstico de ectasia y una selección para riesgo de ectasia antes de las intervenciones LVC.
La búsqueda y la necesidad de ir más allá de la topografía corneal resultaron obvias debido al mayor número de pacientes que padecían ec- tasia pese a una topografía normal y la ausen- cia de otros factores de riesgo aparentes.13,14 Además, los casos de córneas irregulares que habrían sido excluidas de una cirugía en función de las características de la super cie anterior, pero cuyo LASIK no presentó complicaciones y cuyos resultados fueron estables, demuestran la necesidad de una mejor especi cidad.15 De este modo, es indiscutible la necesidad de me- jorar la sensibilidad y la especi cad cuando se considera realizar un diagnóstico de ectasia y una selección para riesgo de ectasia antes de las intervenciones LVC.
El establecimiento de mejores competencias diagnósticas debe incluir dos elementos distin- tos: (1) el uso consciente o racional de datos ob- jetivos, que es fundamental, puesto que la va- riabilidad del análisis subjetivo de los mapas de curvatura de la super cie anterior es signi cativa entre los diversos especialistas del ramo,16 y (2) la necesidad de producir una información clínica con más detalles mediante técnicas avanzadas de imagen para caracterizar mejor a la córnea,
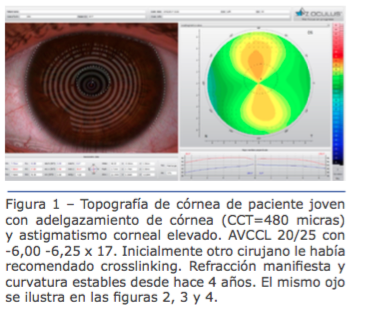
Figura 1 – Topografía de córnea de paciente joven con adelgazamiento de córnea (CCT=480 micras) y astigmatismo corneal elevado. AVCCL 20/25 con -6,00 -6,25 x 17. Inicialmente otro cirujano le había recomendado crosslinking. Refracción mani esta y curvatura estables desde hace 4 años. El mismo ojo se ilustra en las guras 2, 3 y 4.
pero sin excluir los datos de curvatura de la super cie an- terior, incluidas la tomografía y las valoraciones biomecánicas de la córnea.17-20
La tomografía corneal de- scribe las super cies anterior y superior de la córnea y gen- era el mapa paquimétrico de toda la córnea (Figura 2).18 Esto es posible al utilizar dis- tintas tecnologías, incluidas la imagen de Scheimp ug,21,22 la ultrasonografía de muy alta frecuencia (VHF-US)23,24 y la tomografía de coherencia óp- tica (TCO).25,26 Estos métodos cuentan con distintas fun- ciones, pero todos producen un enorme volumen de infor- mación clínica, más allá de la caracterización topográ ca obtenida mediante la curvatu- ra de la super cie anterior. Lo curioso es que ha sido un de- safío demostrar que dichos datos, vastos y complejos, efectivamente permiten me- jorar la exactitud para detec- tar formas leves de ectasia con relación al bien establecido método de topografía de la córnea.1 Aunque el análisis longi- tudinal sería el mejor diseño para este tipo de estudio, el otro ojo con topo- grafía normal de pacientes con ectasia clínica detectada en el ojo ipsilateral ha sido considerado una buena alternativa, ya que, según Klyce, este tipo de ojos es considerado como queratocono de forma frustra.27 Curiosamente, distintos sistemas de Scheimp ug utilizaron ese modelo de casos con ectasia muy asimé- trica para desarrollar y demostrar aún más la mejora en la sensibilidad para detectar formas iniciales de ectasia. Al- gunos de esos estudios emplearon Orb- scan,28 Pentacam,17,29 Sirius30 y Galilei.31 Dichos estudios generan visualizaciones con índices derivados de distintos méto- dos de inteligencia arti cial para generar un análisis objetivo a partir de la infor- mación tomográ ca compleja y facilitar la decisión clínica. Por ejemplo, la visu- alización Belin/Ambrósio Enhanced Ec- tasia Display (BAD), disponible en Pen- tacam, combina los mapas de elevación de super cies anterior y posterior BFS, en sus versiones estándar y mejorada, con la información de distribución del espesor. En él se presentan distintos parámetros de tomografía como la des- viación estándar de la normalidad para la enfermedad (valores d) y se calcu- la un parámetro BAD-D nal según un análisis de regresión con el n de maxi- mizar la exactitud para la detección de enfermedades ectásicas.19,21,22 También están disponibles otras visualizaciones, como el analizador SCORE, desarrollado por Gatinel y Saad, que está integrado al sistema Orbscan.32
 Los sistemas de obtención de imáge- nes corneales han evolucionado también cuanto a su capacidad de analizar indivi- dualmente las capas de la córnea, como el epitelio y la membrana de Bowman.
Los sistemas de obtención de imáge- nes corneales han evolucionado también cuanto a su capacidad de analizar indivi- dualmente las capas de la córnea, como el epitelio y la membrana de Bowman.
A este método lo llamamos tomografía segmental o tomografía corneal en capas (Figura 3).33 Reinstein y colaboradores desarrollaron índices del grosor del epi- telio corneal para la detección de que- ratocono utilizando VHF-US.23,34 Huang y colaboradores elaboraron un abordaje semejante con TCO.25,26 Además, Sinha- Roy y colaboradores analizaron la irre- gularidad de la membrana de Bowman (MB) en córneas ectásicas y normales y crearon el índice de rugosidad BRI (Bowman’s roughness index), el que me- joró, junto con la información del espesor epitelial y de BAD-D, la sensibilidad para la detección de formas leves de ectasia en estudios que involucraron el otro ojo con topografía normal de casos de ecta- sia muy asimétrica (VAE, very asymme- tric ectasia).
No obstante, es importante pensar que algunos de estos casos de VAE pueden ser ejemplos concretos de ectasia unilate- ral.17,35 Curiosamente, hay un consenso de que el verdadero queratocono unilateral no existe, pero también de que una ectasia secundaria o inducida, como consecuencia de un proceso mecánico, como frotarse los ojos continuamente, puede manifestarse unilateralmente.3 Este concepto está de acuerdo con la hipótesis two-hit, la cual considera una predisposición genética subyacente juntamente con factores am- bientales externos.2 Un estudio alternativo para valorar la susceptibilidad a la ectasia involucra el análisis del estado preopera- torio de pacientes con ectasia post-LVC.36 No obstante, la información clínica dispo- nible antes de la cirugía debe ser un factor limitante para la relevancia de tales estu- dios. Distintos grupos han diseñado pun- tuaciones para la valoración del riesgo, como el sistema de puntuación de riesgo de ectasia (ERRS, Ectasia Risk Score Sys- tem) de Randleman y colaboradores37 y la puntuación de la susceptibilidad a la ec- tasia (ESS, Ectasia Susceptibility Score).36
Recientes avances en el ámbito de la biomecánica corneal han contribuido en gran medida para el entendimien- to de la siopatología de la ectasia.38 Los tonómetros de no contacto Ocular Response Analyzer® (Reichert Oph- thalmic Instruments, Depew, NY)39 y Corvis® (OCULUS Optikgeräte GmbH; Wetzlar, Alemania)40 detectan la respuesta de la deformación corneal. Vinciguerra y colaboradores crearon el CBI (Corneal Biomechanical Index), un nuevo índice biomecánico para integrar los valores de la respuesta de la de- formación corneal (DCR) al Corvis ST.41 En última instancia, se ha propuesto integrar las informaciones biomecáni- cas con las de la forma corneal para mejorar aún más la exactitud de la de- tección de ectasias leves o incluso su susceptibilidad.14,17,39 Recientemente se han realizado estudios para desarrollar el índice biomecánico tomográ co, TBI (Tomographic Biomechanical Index), el que combina la información de Cor- vis ST y la información de Pentacam HR mediante un método Random For- est con validación cruzada dejando uno fuera o leave-one-out (RF-LOOCV).17 Este nuevo índice ha demostrado gran exactitud en la detección de ectasias, incluso una gran sensibilidad para de- tectar ectasias subclínicas (fruste) en ojos con topografía normal de pacientes con mucha asimetría, y ha presentado mejor desempeño que todos los demás parámetros probados (Figuras 4, 5 y 6).42 Estudios futuros deben considerar el impacto de los procedimientos LVC y otros factores ambientales, incluidos los valores referentes a la super cie ocular y a la alergia. Ellos serían inte- grados a esos parámetros biomecánic- os y de forma para valorar el riesgo de la progresión de la ectasia. Se estima una continua y acelerada evolución de la revolución en los sistemas de obten- ción de imágenes de la córnea.
Bibliografía
- AmbrosioR,Jr.,RandlemanJB.Screeningforectasia risk: what are we screening for and how should we screen for it? J Refract Surg 2013;29:230-2.
- McGheeCN,KimBZ,WilsonPJ.ContemporaryTreatment Paradigms in Keratoconus. Cornea 2015;34 Suppl 10:S16-23.
- GomesJA,TanD,RapuanoCJ,etal.Globalconsensuson keratoconus and ectatic diseases. Cornea 2015;34:359- 69.
- SeilerT.Theparadigmchangeinkeratoconustherapy. Indian J Ophthalmol 2013;61:381.
- AmslerM.LekératocônefrusteauJaval.Ophthalmologi- ca 1938;96:77-83.
- AmslerM.[The»formefruste»ofkeratoconus].WienKlin Wochenschr 1961;73:842-3.
- SeilerT,QuurkeAW.IatrogenickeratectasiaafterLASIK in a case of forme fruste keratoconus. J Cataract Refract Surg 1998;24:1007-9.
- WilsonSE,AmbrosioR.Computerizedcornealtopogra- phy and its importance to wavefront technology. Cornea 2001;20:441-54.
- RabinowitzYS,McDonnellPJ.Computer-assistedcorneal topography in keratoconus. Refractive & corneal surgery 1989;5:400-8.
-
- Maeda N, Klyce SD, Smolek MK, Thompson HW. Automated kera- toconus screening with corneal topography analysis. Investigative ophthalmology & visual science 1994;35:2749-57.
- Maguire LJ, Bourne WM. Corneal topography of early keratoconus. American journal of ophthalmology 1989;108:107-12.
- Ambrosio R, Jr., Klyce SD, Wilson SE. Corneal topographic and pachymetric screening of keratorefractive patients. J Refract Surg 2003;19:24-9.
- Klein SR, Epstein RJ, Randleman JB, Stulting RD. Corneal ecta- sia after laser in situ keratomileusis in patients without apparent preoperative risk factors. Cornea 2006;25:388-403.
- Ambrosio R, Jr., Dawson DG, Salomao M, Guerra FP, Caiado AL, Be- lin MW. Corneal ectasia after LASIK despite low preoperative risk: tomographic and biomechanical ndings in the unoperated, stable, fellow eye. J Refract Surg 2010;26:906-11.
- Reinstein DZ, Archer TJ, Gobbe M. Stability of LASIK in topographi- cally suspect keratoconus con rmed non-keratoconic by Arte-
mis VHF digital ultrasound epithelial thickness mapping: 1-year follow-up. Journal of refractive surgery (Thorofare, NJ : 1995) 2009;25:569-77. - Ramos IC, Correa R, Guerra FP, et al. Variability of subjective classi cations of corneal topography maps from LASIK candidates. Journal of refractive surgery (Thorofare, NJ : 1995) 2013;29:770-5.
- Ambrosio R, Jr., Lopes BT, Faria-Correia F, et al. Integration of Scheimp ug-Based Corneal Tomography and Biomechanical Assessments for Enhancing Ectasia Detection. J Refract Surg 2017;33:434-43.
- Ambrosio R, Jr., Belin MW. Imaging of the cornea: topography vs tomography. J Refract Surg 2010;26:847-9.
- Ambrosio R, Jr., Nogueira LP, Caldas DL, et al. Evaluation of corneal shape and biomechanics before LASIK. International ophthalmolo- gy clinics 2011;51:11-38.
- Salomao MQ, Esposito A, Dupps WJ, Jr. Advances in anterior seg- ment imaging and analysis. Curr Opin Ophthalmol 2009;20:324-32.
- Ambrosio R, Jr., Valbon BF, Faria-Correia F, Ramos I, Luz A. Sche- imp ug imaging for laser refractive surgery. Curr Opin Ophthalmol 2013;24:310-20.
- Belin MW, Ambrosio R. Scheimp ug imaging for keratoconus and ectatic disease. Indian J Ophthalmol 2013;61:401-6.
- Reinstein DZ, Archer TJ, Urs R, Gobbe M, RoyChoudhury A, Silver- man RH. Detection of Keratoconus in Clinically and Algorithmically Topographically Normal Fellow Eyes Using Epithelial Thickness Analysis. J Refract Surg 2015;31:736-44.
- Reinstein DZ, Silverman RH, Rondeau MJ, Coleman DJ. Epithelial and corneal thickness measurements by high-frequency ultrasound digital signal processing. Ophthalmology 1994;101:140-6.
- Li Y, Chamberlain W, Tan O, Brass R, Weiss JL, Huang D. Subclinical keratoconus detection by pattern analysis of corneal and epithe- lial thickness maps with optical coherence tomography. J Cataract Refract Surg 2016;42:284-95.
- Li Y, Tan O, Brass R, Weiss JL, Huang D. Corneal epithelial thickness mapping by Fourier-domain optical coherence tomography in nor- mal and keratoconic eyes. Ophthalmology 2012;119:2425-33.
- Klyce SD. Chasing the suspect: keratoconus. Br J Ophthalmol 2009;93:845-7.
- Saad A, Gatinel D. Topographic and tomographic properties of forme fruste keratoconus corneas. Investigative ophthalmology & visual science 2010;51:5546-55.
- Ambrosio R, Jr., Caiado AL, Guerra FP, et al. Novel pachymetric parameters based on corneal tomogra- phy for diagnosing keratoconus. Journal of refractive surgery (Thorofare, NJ : 1995) 2011;27:753-8.
- Arbelaez MC, Versaci F, Vestri G, Barboni P, Savini G. Use of a support vector machine for keratoconus and subclinical keratoconus detection by topographic and tomographic data. Ophthalmology 2012;119:2231- 8.
- Smadja D, Touboul D, Cohen A, et al. Detection of subclinical keratoconus using an automated decision tree classi cation. American journal of ophthalmolo- gy 2013;156:237-46.e1.
- Chan C, Ang M, Saad A, et al. Validation of an Ob- jective Scoring System for Forme Fruste Keratoconus Detection and Post-LASIK Ectasia Risk Assessment in Asian Eyes. Cornea 2015;34:996-1004.
- Salomao MQ, Ho ing-Lima AL, Lopes BT, et al. Role of the corneal epithelium measurements in keratorefractive surgery. Curr Opin Ophthalmol 2017;28:326-36.
- Reinstein DZ, Gobbe M, Archer TJ, Silverman RH, Coleman DJ. Epithelial, stromal, and total corneal thickness in keratoconus: three-dimensional display with artemis very-high frequency digital ultrasound. J Refract Surg 2010;26:259-71.
- Isaac C Ramos DZR, Timothy J Archer, Marine Gob- be, Marcella Q Salomão, Bernardo Lopes, Allan Luz, Fernando Faria-Correia, Damien Gatinel, Michael W Belin, Renato Ambrósio Jr. Unilateral Ectasia charac- terized by Advanced Diagnostic Tests. International Journal of Keratoconus and Ectatic Corneal Diseases 2016;5:51.
- Ambrósio Jr R, Ramos I, Lopes B, et al. Assessing ectasia susceptibility prior to LASIK: the role of age and residual stromal bed (RSB) in conjunction to Belin-Ambrósio deviation index (BAD-D). Revista Brasileira de Oftalmologia 2014;73:75-80.
- Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology 2008;115:37-50.
- Roberts CJ, Dupps WJ, Jr. Biomechanics of corneal ectasia and biomechanical treatments. Journal of cataract and refractive surgery 2014;40:991-8.
- Luz A, Lopes B, Hallahan KM, et al. Enhanced Combined Tomography and Biomechanics Data for Distinguishing Forme Fruste Keratoconus. J Refract Surg 2016;32:479-94.
- Ambrósio Jr R, Ramos I, Luz A, et al. Dynamic ultra high speed Scheimp ug imaging for assessing cor- neal biomechanical properties. Revista Brasileira de Oftalmologia 2013;72:99-102.
- Vinciguerra R, Ambrosio R, Jr., Elsheikh A, et al. Detection of Keratoconus With a New Biomechanical Index. J Refract Surg 2016;32:803-10.
- 4Ambrosio R J, Lopes B., Faria-Correia F., Salomao M., Buhren J., Robets C., Elsheikh A., Vinciguerra R., Vinciguerra P. Integration of Scheimp ug based Cor- neal Tomography and Biomechanical Assessments for Enhancing Ectasia Detection. Journal of refractive surgery 2017.
