Innovaciones en Oftalmología
Dr. Julio Fernández Mendy Argentina
La evolución en cada rama del conocimiento humano es el resultado de pequeños eslabones que van encadenando saberes parciales para alcanzar un nuevo descubrimiento.
Estos componentes de la cadena del saber no siempre son logros exitosos. En ocasiones, fracasos estrepitosos también pueden develar otros caminos y nuevos aprendizajes.
Las innovaciones reales se aprecian con el tiempo, y a veces cancelando su destino inicial y permitiendo la aparición de otro desarrollo genial.
Pensemos que muchos dispositivos que nos deslumbraron por la espectacularidad de su lanzamiento en los últimos cuarenta años fueron abandonados al poco tiempo.
Recuerdo que, en mi primer Curso Anual de la Sociedad Argentina de Oftalmología, a principios de los 80, con pocos meses de residente, vi la presentación del primer viscoelástico, el Healon. Si bien en ese momento, quien lo presentaba lo hizo con una gran elocuencia, yo no llegaba a comprender todas las ventajas y la verdadera importancia de su utilización. En ese momento se operaba la catarata con ICCE y recién se comenzaba la curva de aprendizaje de la ECCE, con capsulotomía en abrelatas bajo suero y aire para mantener el espacio de la cámara anterior al implantar el LIO.
El valor de los viscoelásticos quedó demostrado con los años y hoy es una herramienta quirúrgica imprescindible.
Las diferentes subespecialidades que conforman nuestra especialidad en la actualidad son tan dispares y complejas que permiten abarcar infinitas cualidades y destrezas creativas.
Este vasto abanico de oftalmólogos contiene clínicos con una sobresaliente capacidad de observación del paciente en la lámpara de hendidura, cirujanos intraoculares con habilidades manuales sorprendentes que crean constantemente nuevas técnicas quirúrgicas, investigadores en laboratorios que descubren mecanismos químicos con aplicaciones clínicas, y también inventores que desarrollan instrumental quirúrgico o sofisticadas tecnologías novedosas.
Innovaciones pueden ser todas estas, y el impacto es lo que le otorga la entidad de tal.
La oftalmología de los últimos 50 años ha tenido un desarrollo descomunal. Desde 1949, cuando Ridley colocó su primer lente intraocular, las innovaciones en la cirugía refractiva y de la catarata han ocurrido continuamente y seguirán ocurriendo con seguridad.
En el campo de la cirugía de retina ha habido innumerables progresos en los últimos 20 años con el perfeccionamiento de la técnica de vitrectomía mínimamente invasiva y en la clínica de la patología retinal con las inyecciones intravítreas y los dispositivos de liberación prolongada de drogas en la cavidad vítrea.
Toda innovación da lugar a una controversia tácita entre los que están rápidamente a favor y apuestan esperanzados por resultados superiores y futuras aplicaciones y, por el otro los escépticos, que aguardan expectante la confirmación del tiempo, argumentando incrementos de costos y dificultades en la curva de aprendizaje, y sosteniendo que no se ha probado todavía un beneficio real.
Los primeros pueden formar parte de los pioneros, que con su entusiasmo permiten el avance de la ciencia en un camino plagado de dificultades y, por el otro lado los cautos que prefieren transitar el camino ya afirmado.
Los pioneros son indispensables pues sin su participación no existiría progreso en las ciencias, pero sin la mesura aportada por la reflexión crítica de los cautos podríamos generar más daño a los pacientes.
Planteada esta introducción, podemos decir que en la cirugía del segmento anterior: córnea, refractiva, catarata y glaucoma innumerables novedades ocurrieron en los últimos años, se han lanzado al mercado diferentes modelos de lentes intraoculares genéricamente llamados multifocales, se han modificado materiales, dispositivos de implantación, diseño de las ópticas, ideas “futuristas” de los lentes, etc.
Con la aparición hace unos años del Acrysof PanOptix, trifocal refractivo-difractivo, con asfericidad de -0.2 μ, rango de 1 a 3.75 D de astigmatismo, Alcon ha mejorado notablemente los resultados obtenidos con el Restor, primer multifocal difractivo apodizado. ElnuevolanzamientodelClareon, introduce un nuevo biomaterial, con diseño avanzado, que permite una visión más transparente, con baja incidencia de glare, mejor claridad óptica que el anterior material Acrysof y sin glistening. Hoy monofocal, anticipando una nueva generación de trifocales. Además, creó el sistema de inyección AutonoMe, el primero (y único) descartable, precargado y automatizado (motorizado por CO2), con una boquilla con tope para introducirlo por 2.2.mm. (Figura 1)
PhysIOl introdujo una serie de modelos Finevision: EDOF trifocal difractivo hi- drofóbico (Triumf Pod L GF), con doble C loop (que brinda 4 apoyos en bag), una estabilidad de 96% entre 0 y 5° del eje establecido en los tóricos, de un acrílico hidrofóbico G free (sin glistening), 360° borde cuadrado, diámetro 6 mm, bicon- vexo asférico (-0.11μ), número ABBE 42, y foco extendido con +1.75 y 3.50 D de adición. La versión trifocal tórico (Pod FT), con cilindro de 1 a 6 D. Ninguno de estos precargados. (Figura 2)
La firma Rayner, fabricante de los primeros lentes intraoculares implantados por Ridley, produjo un cambio significativo con la plataforma RayOne. El elemento básico común es el sistema de inyección, precargado completamente (sin manipular el lente), con una boquilla de 1.65 mm, para ser implantado manualmente, con émbolo, a través de una incisión sub-2,2 mm. La diversidad de los modelos incluye hasta trifocal difractivo tórico, con asfericidad neutra, de acrílico hidrofílico sin glistening. El diseño de las hápticas es igual a la plataforma tradicional del C Flex, excepto en el nuevo modelo hidrofóbico monofocal en el cual las hápticas son más delgadas. (Figuras 3)
El lente suplementario Sulcoflex trifocal une el diseño del Rayner trifocal en cuanto a la multifocalidad y la experiencia del Sulcoflex en cuanto a facilidad de implante y posibilidad de explantación en caso de ser necesario en el futuro. En efecto, posibilita la realización de un piggy-bag inicialmente, monofocal en bag y trifocal en sulcus, y en los casos donde las condiciones hayan cambiado y la óptica difractiva se transforme en un obstáculo, resultará más simple extraer el sulcoflex trifocal del sulcus, que extraer un lente trifocal del saco. Esta ventaja, la reversibilidad, es una de sus principales ventajas. También es útil en casos clásicos operados años atrás con un monofocal con algún error residual, y que desean no utilizar anteojos de cerca, corrigiendo el error y la presbicia. (Figura 4)
Otra innovación en el mundo de los lentes intraoculares es el Tecnis Eyhance IOL de Johnson & Johnson, otro lente de la familia Tecnis, última generación de lente monofocal con visión intermedia, en la misma plataforma ya probada desde el Tecnis 1.
La compañía OPHTEC, ha incorporado el Precizion Presbyopic, que es un lente de acrílico híbrido, monómeros hidrofóbico e hidrofílico, con segmentos y no anillos, sino un nuevo concepto de CTF (Continuous Transitional Focus), con aberración neutra (modelo 570 A0) y negativa (modelo 570A1). El número ABBE es 47. (Figura 5)
Intensity Hanita introdujo una tecnología de multifocalidad, con un algoritmo DLU (Dynamic Light Utilization), tiene la superficie anterior esférica y la posterior asférica difractiva, es de acrílico hidrofílico, y cuenta con optimización de la utilización de la luz con distribución simétrica de los focos, lo que otorga una visión continua.
Otra tecnología innovadora en su momento, publicada en 2003 y no muy utilizada, la de los lentes foto ajustables (Light Adjustable Lens, LAL RxSight), que están hechos de un material en el que puede modificarse su poder, por efecto de una luz ultravioleta con un preciso patrón, una vez implantado. La corrección del cilindro como el esférico residual, realizada dentro del mes posoperatorio mantiene una estabilidad con los años. Esta tecnología, ha sido aprobada por la FDA y obtiene en el 92% un residual de ±0.50 D. Algunos expertos opinan que podría provocar un cambio disruptivo en el futuro. (Figura 6)
Swiss Advanced Vision, que lanzó en 2017 el Lucidis, un EDOF que tiene buenos resultados, está trabajando en una nueva generación de lentes intraoculares el R-TASC Project, que es un lente electrónico y que enfoca automáticamente, funcionando con energía solar.
Como podemos ver estamos ante desarrollos ópticos con muy diversas orientaciones, biomateriales alternativos que buscan minimizar las disfotopsias, positivas y negativas, el glistening, las opacidades que pueden aparecer cada tanto y nos La compañía OPHTEC, ha incorporado el Precizion Presbyopic, que es un lente de acrílico híbrido, monómeros hidrofóbico e hidrofílico, con segmentos y no anillos, sino un nuevo concepto de CTF (Continuous Transitional Focus), con aberración neutra (modelo 570 A0) y negativa (modelo 570A1). El número ABBE es 47. (Figura 5)
Intensity Hanita introdujo una tecnología de multifocalidad, con un algoritmo DLU (Dynamic Light Utilization), tiene la superficie anterior esférica y la posterior asférica difractiva, es de acrílico hidrofílico, y cuenta con optimización de la utilización de la luz con distribución simétrica de los focos, lo que otorga una visión continua.
Otra tecnología innovadora en su momento, publicada en 2003 y no muy utilizada, la de los lentes foto ajustables (Light Adjustable Lens, LAL RxSight), que están hechos de un material en el que puede modificarse su poder, por efecto de una luz ultravioleta con un preciso patrón, una vez implantado. La corrección del cilindro como el esférico residual, realizada dentro del mes posoperatorio mantiene una estabilidad con los años. Esta tecnología, ha sido aprobada por la FDA y obtiene en el 92% un residual de ±0.50 D. Algunos expertos opinan que podría provocar un cambio disruptivo en el futuro. (Figura 6)
Swiss Advanced Vision, que lanzó en 2017 el Lucidis, un EDOF que tiene buenos resultados, está trabajando en una nueva generación de lentes intraoculares el R-TASC Project, que es un lente electrónico y que enfoca automáticamente, funcionando con energía solar.
Como podemos ver estamos ante desarrollos ópticos con muy diversas orientaciones, biomateriales alternativos que buscan minimizar las disfotopsias, positivas y negativas, el glistening, las opacidades que pueden aparecer cada tanto y nos enfrentan a una complicación no deseada como es explantar un lente que fue implantado perfectamente.
Otra vía en el sentido de crear inyectores precargados descartables, para minimizar la manipulación de las lentes, evitando la contaminación y el daño de ópticas y hápticas.
La aparición de lentes suplementarios, especialmente diseñados para el surco, puede transformar la indicación de la cirugía como “Duet” inicial, como están promoviendo algunos cirujanos.
Otra incógnita es si las lentes foto ajustables, que están siendo utilizadas hace tiempo limitadamente, son capaces de comenzar a utilizarse más masivamente como algunos expertos sugieren o si se irán desvaneciendo.
Finalmente, las lentes intraoculares electrónicas que parecen algo más lejano.
El tiempo, como siempre, nos demostrará cuáles terminan imponiéndose y cuáles abandonadas.








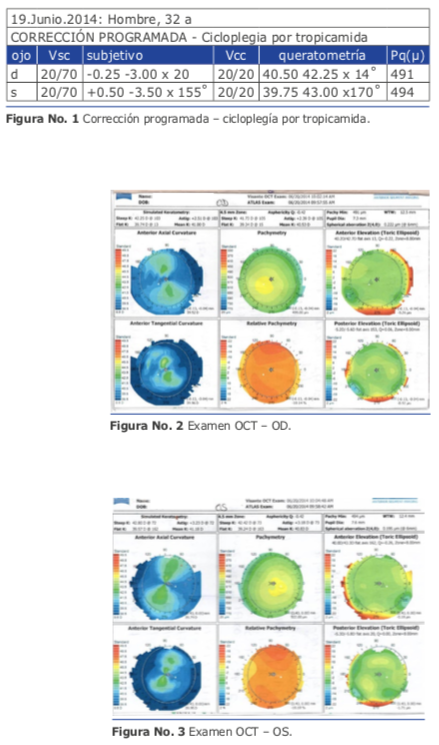 Mi peor caso de cirugía refractiva lo padecí con un hombre de 32 años que en el año 2014 me consultó para la corrección de un astigmatismo miópico elevado que habitualmente debe corregirse con Femto Láser y zona óptica grande, pero en este caso, presentaba córneas de menos de 500 micras. Usé el Excimer AMARIS 750 de Schwind. Tenía buena experiencia con la técnica de TransPRK con Mitomicina C y en las ventajas de la nueva tecnología de “smart pulse”. Realicé una ablación corneal de ambos ojos siguiendo los pasos habituales que dictaba mi experiencia:
Mi peor caso de cirugía refractiva lo padecí con un hombre de 32 años que en el año 2014 me consultó para la corrección de un astigmatismo miópico elevado que habitualmente debe corregirse con Femto Láser y zona óptica grande, pero en este caso, presentaba córneas de menos de 500 micras. Usé el Excimer AMARIS 750 de Schwind. Tenía buena experiencia con la técnica de TransPRK con Mitomicina C y en las ventajas de la nueva tecnología de “smart pulse”. Realicé una ablación corneal de ambos ojos siguiendo los pasos habituales que dictaba mi experiencia: El resultado al cabo de 1 mes fue muy bueno (Ver figura 10). La visión sin corrección mejoró 4 líneas (de 20/80 a 20/30). Pero lamentablemente el efecto logrado se perdió totalmen- te en 3 meses.
El resultado al cabo de 1 mes fue muy bueno (Ver figura 10). La visión sin corrección mejoró 4 líneas (de 20/80 a 20/30). Pero lamentablemente el efecto logrado se perdió totalmen- te en 3 meses.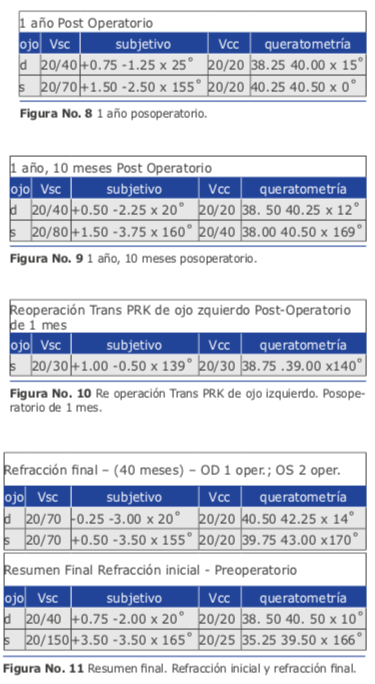
 Durante la cirugía la paciente resultó muy aprensiva. El ojo derecho logró operarse sin inconvenientes, pero en la cirugía del ojo izquier do colapsó emocionalmente (Ver vídeo).
Durante la cirugía la paciente resultó muy aprensiva. El ojo derecho logró operarse sin inconvenientes, pero en la cirugía del ojo izquier do colapsó emocionalmente (Ver vídeo).

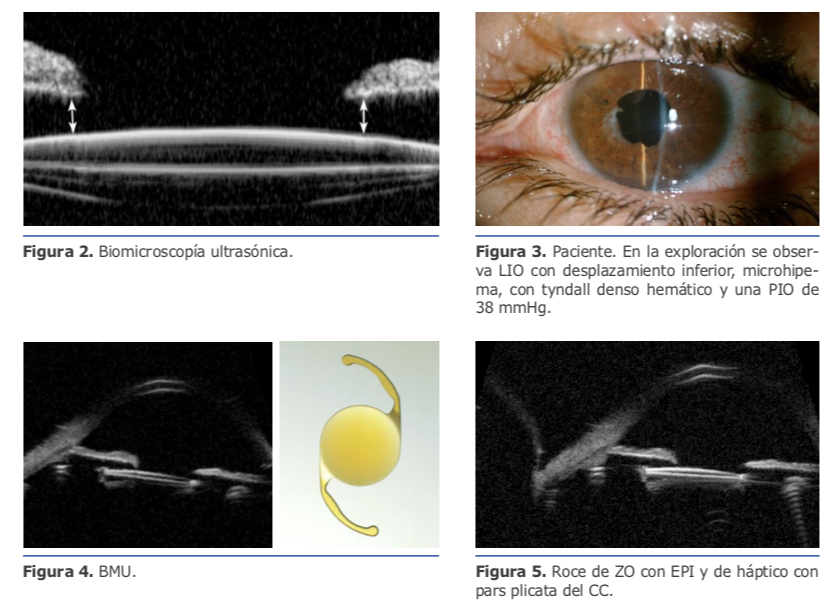
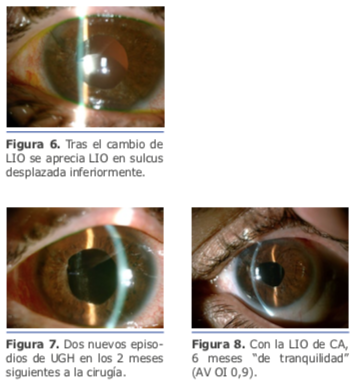 La sustitución de lente monobloque por una de 3 piezas no fue suficiente para una estabilización adecuada de la lente.
La sustitución de lente monobloque por una de 3 piezas no fue suficiente para una estabilización adecuada de la lente.


 Con estos avances tecnológicos los antiguos lentes esféricos fueron transformándose a lentes asféricos, y estos están evolucionando para alcanzar un mayor rango de visión extendida, es así como las plataformas AcrySof IQ Vivity de Alcon y TECNIS Eyhance de Johnson & Johnson han logrado ofrecer nuevas opciones de visión en el tratamiento de catarata y presbicia.
Con estos avances tecnológicos los antiguos lentes esféricos fueron transformándose a lentes asféricos, y estos están evolucionando para alcanzar un mayor rango de visión extendida, es así como las plataformas AcrySof IQ Vivity de Alcon y TECNIS Eyhance de Johnson & Johnson han logrado ofrecer nuevas opciones de visión en el tratamiento de catarata y presbicia.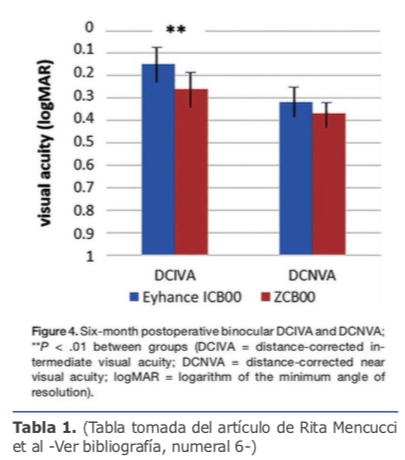 Esta tecnología logra un aumento local y continuo de potencia que va de la periferia hasta el centro de la óptica, el cual tiene una superficie posterior esférica y una superficie anterior asférica modificada, logrando una hiperprolatidad y con eso aumentar la profundidad del foco lo que proporciona una visión intermedia mejorada en comparación con una LIO monofocal asférica estándar.6 Según la compañía, las disfotopsias son comparables a una LIO monofocal asférica estándar pues compensan la aberración corneal asférica.
Esta tecnología logra un aumento local y continuo de potencia que va de la periferia hasta el centro de la óptica, el cual tiene una superficie posterior esférica y una superficie anterior asférica modificada, logrando una hiperprolatidad y con eso aumentar la profundidad del foco lo que proporciona una visión intermedia mejorada en comparación con una LIO monofocal asférica estándar.6 Según la compañía, las disfotopsias son comparables a una LIO monofocal asférica estándar pues compensan la aberración corneal asférica.
