¿Cómo y quién debe financiar el desarrollo de las nuevas tecnologías?
Dr. Daniel Badoza
Argentina
Contacto
Dr. Daniel Badoza – dabadoza@gmail.com
El autor no presenta interés financiero en este artículo. Las opiniones vertidas en el mismo no son vinculables a la ALACSSA-R.
En los últimos años nuestra subespecialidad se ha visto favorecida por la aparición y el desarrollo de nuevas tecnologías en todos sus campos.
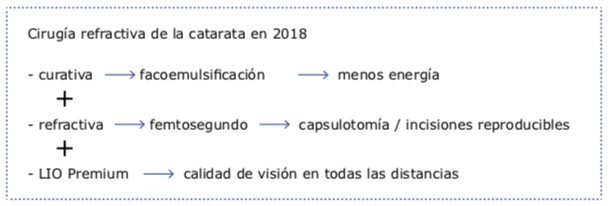
En catarata hemos visto el paulatino mejoramiento de las plataformas de las LIO, el desarrollo de las ópticas tóricas y multifocales, así como el progreso en el cálculo del poder de las lentes. Todo esto ha confirmado la aseveración de que la cirugía de catarata se ha transformado en una herramienta más de la cirugía refractiva.
Los facoemulsificadores han evolucionado mejorando la eficiencia en la entrega de la energía ultrasónica, permitiendo que la incidencia de edema y quemaduras corneales se reduzca significativamente. Lo mismo ha ocurrido con respecto a la fluídica, la estabilidad de la cámara y las medidas preventivas del surge han logrado que los temores a romper la cápsula sean infinitamente menores que una década atrás.
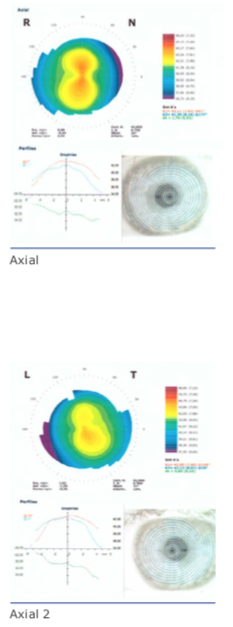
En cirugía refractiva el desarrollo ha sido notable. La evolución de los métodos diagnósticos, las ablaciones personalizadas para córneas aberrantes o con asimetrías, la mejora en el rendimiento de los láseres ha hecho que el uso del excimer láser haya pasado casi todas las fronteras en la cirugía de los diversos defectos refractivos. Las lentes fáquicas, en especial las de cámara posterior, evolucionaron con la aparición de materiales flexibles y ópticas tóricas. El desarrollo de un amplio rango de corrección dióptrica, desde combinaciones esfero-cilíndricas bajas hasta altas ametropías, hacen que en mi criterio, todo paciente que consulte por cirugía refractiva y tenga refracción estable, expectativas adecuadas y requisitos anatómicos para el implante de una lente intraocular, pueda ver cumplido su deseo de una significativa reducción de la dependencia a los anteojos o lentes de contacto. En un futuro cercano, las LIO fáquicas multifocales nos permitirán corregir la presbicia en nuestros pacientes miopes y en algunos hipermétropes, haciendo innecesario correr los riesgos de operar un cristalino transparente.
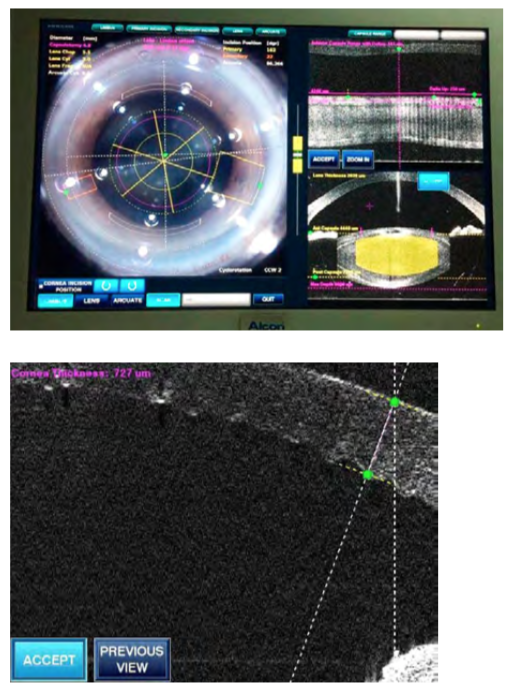
Los avances más significativos posiblemente lleguen de la mano de la tecnología láser femtosegundo. Sin embargo, el uso de la misma, en especial en el campo de la cirugía del cristalino, no está demostrando un gran crecimiento en su uso y aún no tiene la aceptación global de la comunidad oftalmológica. ¿Por qué ocurre esto, habiendo sido esta tecnología aprobada por la FDA en el 2010?
Considero que esto se debe a la relación de tres variables que influyen en la difusión entre los colegas de toda nueva terapia, técnica quirúrgica o tecnología: a) las ventajas con respecto a la tecnología actual; b) la curva de aprendizaje; c) el costo de adquisición, de uso y de mantenimiento.
Tomemos dos ejemplos exitosos: el de los agentes anti-VEGF y el LASIK. En cuanto a los primeros, fueron una revolución en el tratamiento de la maculopatía por membrana neovascular. Para una patología en la que prácticamente no podíamos dar respuestas, a finales de 2005 aparece una terapia farmacológica que con sólo hacer una serie de inyecciones podía conservar, y aun mejor, recuperar parte de la visión perdida por maculopatía. El perfil de seguridad de estas drogas, como en la totalidad de los productos de la industria farmacéutica, es ampliamente investigado en las fases 1 a 3, en estudios randomizados controlados por las agencias nacionales de salud pública, lo que hace que sea excepcional la aparición de efectos adversos no conocidos al momento de ser introducidos en el mercado. Tratamiento con efectos sin precedentes, técnica fácil de incorporar y sin costo de inversión, efectos adversos conocidos y baja incidencia de complicaciones: la terapia fue un éxito inmediato en su difusión.
Con el LASIK ocurrió algo semejante: si bien requería una alta inversión para iniciarse en la técnica, la precisión para corregir miopías, hipermetropía y astigmatismos de gran diversidad dióptrica, con un resultado estable casi inmediato y poca necesidad de controles posoperatorios, hizo que en escaso tiempo su predecesora, la inestable y limitada queratotomía radial, pasara al olvido.
Las complicaciones de la creación de los flaps con el microqueratomo, así como su incidencia, fueron conocidas al momento de la introducción de la tecnología en el mercado, sin mayores sorpresas. Button-holes, colgajos incompletos o free caps, todas complicaciones relativamente manejables y de baja incidencia. Con el tiempo la aparición de ectasias nos hizo aprender los criterios de exclusión del LASIK. Luego la tecnología fue experimentando mejoras en sus resultados finales con los sistemas de ablación personalizada, los eye-trackers, el iris-recognition. Pero desde su nacimiento, el LASIK desplazó a la queratotomía radial como método refractivo, demostrando que, cuando una nueva tecnología genera mejoras significativas en los resultados visuales de nuestros pacientes, los oftalmólogos no dudamos en incorporarla rápidamente invirtiendo lo necesario, aunque sea oneroso y capacitándonos en su curva de aprendizaje.
Con la tecnología femtosegundo ocurrió algo absolutamente distinto. La industria lanzó estos equipos afirmando que era la tecnologíamás precisa para la cirugía facorrefractiva y las lentes premium. Desde el mismo lanzamiento de la tecnología, allá por el 2011, he escuchado a colegas expresar que el láser realizaba las incisiones con una precisión absoluta que con sus manos no podían repetir, rexis que no fallaban nunca y lentes que siempre quedaban perfectamente centradas. Salvo excepciones como la de los doctores Arnaldo Espaillat o Ángel Pineda, no hemos visto comparaciones de resultados refractivos y visuales, tanto en corto como mediano plazo, que identificaran diferencias significativas con respecto a la faco manual. Llama la atención también que dentro de ciertos estudios comparativos se reporten incidencia de desgarros de la rexis mayores del 1 % en la técnica manual, lo cual es muy alto para cirujanos expertos.
También el argumento de que el femtosegundo ayudaría en los casos difíciles, en especial en córneas con defectos endoteliales, ha demostrado una floja y hasta nula evidencia de superioridad con respecto a la faco manual.
Al poco tiempo del lanzamiento de estas «mágicas» herramientas de tecnología robótica infalible, se reportaron complicaciones de gravedad mediana (como los desgarros en el margen de la rexis o desprendimientos de Descemet) o extrema (como los bloqueos capsulares intraoperatorios al realizar la hidrodisección). Eso llevó al desarrollo, en poco tiempo, de nuevos dockings, mejores sistemas de OCT intraoperatorios, y de técnicas para evitar el efecto de la hidrodisección sobre las burbujas acumuladas entre la cara posterior del cristalino y la cápsula posterior.
El alto costo de adquisición, mantenimiento y uso de estos equipos, y la rápida necesidad de mejorarlos desde su introducción en el mercado, me llevan a hacer una consideración económica y ética sobre quién y de qué manera se debe financiar el desarrollo de las nuevas tecnologías con las que a diario somos bombardeados en nuestra especialidad.
Los pasos habituales mediante los cuales la industria farmacéutica introduce sus productos en el mercado son: el desarrollo de la droga y la prueba de la misma en los ensayos clínicos, estableciendo relación dosisefecto e incidencia de efectos adversos. Esa información científica desarrollada les permite introducir la droga en el mercado, y recién ahí, recuperar la inversión. Todo el proceso muchas veces lleva varios años. En cierta forma, el modelo de negocio es similar al de las empresas de construcción vial: desarrollan una nueva autopista, y con la obra terminada instalan las cabinas del peaje para recuperar la inversión y obtener ganancias.
El modelo que siguieron las empresas que desarrollaron las máquinas de femtofaco fue inverso: han introducido en el mercado productos (casi afirmaría que eran prototipos) no desarrollados ni evaluados en su performance completamente, los han introducido al mercado con costos elevadísimos en todos los aspectos (adquisición, mantenimiento y uso), acompañado de una estrategia de mercado tendiente a generar en nosotros la expectativa de que esta tecnología es el nuevo gold standard y de que con ella tendremos resultados perfectos. Luego se han nutrido de la experiencia de los oftalmólogos (y de sus coronarias) como fuente de información gratuita de lo que se requiere para mejorar la tecnología. En cierta forma, homologando el negocio con el de las constructoras viales, luego de pagar el peaje (y en última instancia, de abonarlo los pacientes) a valores de transbordador espacial, nos ponen el chaleco naranja y nos dan las palas para que junto con nuestros pacientes empecemos a hacer el trazado de la futura autopista.
Creo que con esta tecnología la industria debería haberse manejado como con los fármacos. Al principio financiar las cirugías en estudios multicéntricos con cirujanos expertos que, con el consentimiento de sus pacientes, hubieran detectado
las complicaciones, determinado adecuadamente los parámetros de energía más convenientes, genera- do la información para el perfeccio- namiento de los dockings, y hubie- ran desarrollado las modificaciones en la técnica de faco para evitar las complicaciones del femto. Eso hu- biera prevenido, por ejemplo, los reportes de bloqueo capsular in- traoperatorio con caída de núcleo al vítreo, que deben haber traído un dolor de cabeza a los cirujanos que prometieron a sus ilusionados pa- cientes los resultados perfectos de una cirugía premium. La tecnología se debería haber introducido en el mercado luego de haber obtenido toda esa información, al precio ne- cesario para recuperar la inversión y obtener sus merecidas ganancias. Pero por supuesto que eso conlle- va un elevado riesgo: si tanta in- versión en desarrollo termina en no obtener mejores resultados que la faco convencional, la inversión fue una mala apuesta.
Es tentador asociar el futuro de las máquinas de femtosegundo con el desarrollo que tuvieron las máqui- nas de faco en sus comienzos. Sin embargo, la idea de la faco tenía un fin, establecía un nuevo paradigma a alcanzar en la cirugía de la catara- ta, que la diferenciaba de la técnica extracapsular y estimulaba a iniciar la curva de aprendizaje de la misma: una cirugía de incisión pequeña mu- cho más segura porque mantenía la cámara cerrada. La aparición de las lentes plegables, permitiendo reducir el astigmatismo inducido, catapul- tó la facoemulsificación a ser el gold standard de la cirugía de catarata.
Por el contrario, al día de hoy el femtosegundo es una nueva manera de realizar la facoemulsifica- ción, pero no cambia la esencia de la misma, no agrega ventajas que
la superen ni soluciona o ha mostrado reducir la incidencia de sus problemas «clásicos»: la endoftalmitis, la ruptura capsular, el edema macular, el edema corneal y el error en el cálculo de la lente intraocular. Por eso todos los estudios comparativos demuestran que es una forma más cara pero no más precisa ni segura de realizar la facoemulsificación.
Como entusiasta de la incorporación de la tecnología, tuve mucha expectativa con la llegada del femtofaco en 2014 a mi clínica. Tras una serie de casos en los que tuve desgarros de la cápsula anterior (habiendo tenido menos de 10 casos en más de 20 años realizando faco) y en los que mis pacientes donde usé ambas técnicas siempre prefirieron el ojo operado con téc- nica manual, decidí suspender el uso del equipo en las cirugías de catarata. Teniendo presente el principio que nos guía al recomendar tecno- logías a nuestros pacientes (underpromise and overdeliver) me parece inapropiado que mis pacientes paguen esos valores para obtener tan poco beneficio. No dudo en que volveré a re- comendárselos cuando la evidencia demuestre que esta tecnología es significativamente mejor que la faco convencional, aparezcan nuevas aplicaciones de la misma con real utilidad, o cuando la edad reduzca mi destreza manual y compruebe que por ese motivo mis resultados ya no son los mismos.
Así como la investigación clínica ha evolucionado con el tiempo desde el Código de Núremberg y la Declaración de Helsinki dando lugar a las reglas del GCP, creo que deberíamos establecer, junto con la industria y las autoridades sanitarias, las condiciones en las que debe desarrollarse y la evidencia mínima de ventajas y desventajas con respecto al gold standard actual que debe presentar la tecnología médi- ca antes de ser introducida en el mercado. De esta manera, la salud en general y la visión de nuestros pacientes en particular podrán recibir los mejores resultados posibles con la mayor eficiencia en el manejo de los recursos, y noso- tros podremos confiar plenamente en las ideas y argumentos expresados por las empresas y por los colegas que disertan sobre las nuevas tecnologías que sean ofrecidas para que incor- poremos en nuestra práctica diaria.
Infecciones
Coordinador:
Dr. Luis Fernando Mejía – Colombia
Panelistas
Dr. Germán Giraldo – Colombia
Dra. Ángela María Gutiérrez – Colombia Dr. Eduardo Viteri – Ecuador
1. ¿Usa profilaxis antibiótica en el preoperatorio? ¿Cuál?
Dr. Germán Giraldo: Uso, de rutina, moxifloxacino desde el día previo a la cirugía, 1 gota cada 6 horas, hasta el momento de entrar al quirófano.
Dra. Ángela María Gutiérrez: No uso profilaxis antibiótica de rutina. A todos mis pacientes se le aplica yodo-povidona al 5 % por 3 minutos antes de la cirugía. Con esta intervención, buscamos reducir la flora de la conjuntiva y de los párpados para evitar la contaminación de la herida quirúrgica y, por ende, el acceso de microorganismos al ojo, tanto en el momento intraoperatorio como en el posoperatorio. Su eficacia tiene un nivel de evidencia II, con una recomendación clínica de uso B. De haber alergia al compuesto yodado, se utiliza clorhexidina al 0.02 % como alternativa.
Cuando veo pacientes con patología de párpados como blefaritis (anterior y/o posterior) o que tengan rosácea, atopia y compromiso palpebral, les formulo champú de bebé o alguna de las soluciones para lavado y limpieza de párpados con compuestos como aceite del árbol del té (antimicrobiano, astringente), caléndula, avena, etc., que remueven partículas, células y escamas del borde palpebral, reduciendo la carga infecciosa de microorganismos que están en el párpado y, a la vez, desinflamando. Aunque esta medida no tiene un nivel de evidencia significativo (III – C), considero que es importante en el manejo integral de un paciente que va a ser llevado a una cirugía intraocular.
Ocasionalmente, a pacientes diabéticos o con inmunosupresión o en estado de franco deterioro, con blefaritis o antecedente de infecciones sistémicas les formulo profilácticamente moxifloxacina 0.5 % o Zymaxid 0.5 % en gotas a razón de 5 gotas al día 1 un día antes y hasta que ingresen a cirugía. Además, a esta medida la acompaño con un AINE tópico.
Según publicaciones como las de Vasavada, el antibiótico tópico administrado desde el día anterior es tan eficaz como el antibiótico tópico administrado 2 horas antes de la cirugía, y su efecto de disminuir la flora conjuntival ha sido efectivo en ambas modalidades. En términos generales, la evidencia (III – C) no es tan sustantiva como para afirmar que esta acción es realmente efectiva como profilaxis preoperatoria para evitar la endoftalmitis.
En la valoración prequirúrgica de cirugía de catarata, descarto pacientes con infecciones en vías lagrimales o en el ojo congénere, y no los opero hasta que no se haya tratado y resuelto la patología.
Aislamos los bordes palpebrales y las pestañas con plástico que se adhiere al borde palpebral. Igualmente tenemos un control muy estricto de asepsia en salas de cirugía, así como todo lo referente al instrumental y equipo que se utiliza en el procedimiento.
Dr. Eduardo Viteri: Como profilaxis para infecciones, prescribo rutinariamente moxifloxacina TID durante los tres días previos a la cirugía. Adicionalmente se indica a los pacientes realizar lavado de borde palpebral con alguna de las soluciones jabonosas comercialmente disponibles. Si hubiera evidencia de demodicosis palpebral prescribo ivermectina oral adicional a las medidas de higiene. No prescribo antibióticos sistémicos.
Previo al inicio de la intervención se instila povidona yodada al 5 % en fondos de saco conjuntivales e irrigación profusa.
2.Cuál de estos tres métodos prefiere usar en cirugía: ¿antibióticos intracamerales, en la infusión de la FACO, o subconjuntivales? ¿Por qué? ¿Cuál antibiótico usa?
Dr. Germán Giraldo: No utilizo antibiótico intraoperatorio. Considero que la moxifloxacina desde el día antes me asegura niveles adecuados en cámara anterior al momento de la cirugía. Sin embargo, al finalizar la cirugía administro una gota de moxifloxacina.
Dra. Ángela María Gutiérrez: No utilizo antibióticos intracamerales ni endilución en el líquido de irrigación, a pesar de existir evidencia de alta efectividad del uso de antibiótico intracameral (nivel de evidencia 1b, grado de recomendación A) en la prevención de la endoftalmitis. La explicación es que en mi país (Colombia), no disponemos de antibióticos en monodosis para uso intracameral. Otra de las razones es el temor a que se presente un error en la dilución con la cefuroxima, la moxifloxacina, la vancomicina u otros, o que se contaminen los medicamentos y no queden totalmente estériles, dando lugar a toxicidad intraocular o infección. Entre las complicaciones que pueden presentarse con los antibióticos intracamerales están: las reacciones alérgicas, edema macular, síndrome tóxico del segmento anterior, oclusión arterial en vasos retinianos, etc.
Tenemos una tasa bajísima de incidencia de endoftalmitis en el sitio donde realizo mis cirugías (alrededor de 0.04 %) y ninguno de los cirujanos de catarata utiliza antibióticos intracamerales. Nuestra tasa es prácticamente comparable con la de centros en los que se coloca el bolo intracameral de antibiótico y que reportan tasas tan bajas de endoftalmitis como en nuestro centro (Clínica Barraquer, Bogotá Colombia).
Al finalizar la cirugía, aplicamos una gota de moxifloxacina 0.5% y otra de prednisolona 1% sobre la superficie ocular.
Utilizo inyección subconjuntival de ceftazidima con dexametasona al finalizar el procedimiento en personas de alto riesgo de infección e inflamación, como lo son los diabéticos. También, coloco inyección subconjuntival de ceftazidima y dexametasona si hay ruptura de cápsula posterior con pérdida de vítreo. La explicación es que el antibiótico inhibe el crecimiento bacteriano que puede entrar en el ojo durante la cirugía.
Consideraría la aplicación de antibióticos intracamerales en mis pacientes de cirugía de catarata si se dispusiera de medicamentos que reúnan los criterios de manufactura respecto a la concentración y esterilidad por parte de los laboratorios.
Durante la cirugía trato de mantener el campo quirúrgico seco, evitando tener exceso de líquido acumulado en la superficie ocular. Trato de mantener siempre la incisión cerrada o estanca al introducir o sacar los instrumentos del ojo, evitando la salida de fluido intraocular o entrada de líquido que esté por fuera del sistema de irrigación. Esto es importante en casos de cirugías complejas o reoperaciones por un riesgo mayor a infección.
Para recordar, los gérmenes que más frecuentemente producen endoftalmitis son las bacterias grampositivas, tales como los estafilococos coagulasa negativa, Staphylococcus epidermidis, aureus y Streptococcus viridans, y las gramnegativas. Menos frecuentes son la Pseudomonas aeruginosa, el Hemophilus influenzae, el P. acnes y hongos, tal como se ha encontrado en los diferentes estudios y publicaciones.
Dr. Eduardo Viteri: Hasta recientemente inyectaba en cámara anterior 0.1 ml de solución de moxifloxacina y dexametasona que se consigue comercialmente preparada para colirio (sin conservantes), sin haber observado efectos secundarios ni registrado casos de endoftalmitis posoperatorias.
Luego de revisar un reciente artículo de Miyake (*) y colaboradores sobre la toxicidad de moxifloxacina, vancomicina y cefuroxima en células vasculares de retina, he suspendido la administración de antibióticos intracamerales en casos rutinarios no complicados.
Considero que este es un aspecto del manejo de posoperatorio que todavía se encuentra sujeto a investigación y es motivo de activa controversia. Debemos mantener nuestra mente abierta a la evidencia que va apareciendo para ajustar nuestra conducta de acuerdo con los protocolos establecidos y la evolución del conocimiento.
3.¿Cuál antibiótico utiliza en su profilaxis? ¿Antibiótico en el posoperatorio, en qué dosis y por cuánto tiempo?
Dr. Germán Giraldo: Utilizo de rutina moxifloxacino desde el día antes de la cirugía, 1 gota, cada 6 horas. Al finalizar la cirugía administro una gota y retiro el paciente del quirófano con protector ocular, sin apósito, con instrucciones de iniciar nuevamente el moxifloxacino al llegar a su casa. El antibiótico lo ordeno por 2 semanas.
Dra. Ángela María Gutiérrez: En el posoperatorio utilizo moxifloxacina 0.5 % y fosfato de dexametasona 0.1 % o gatifloxacina 0.3 % y acetato de prednisolona 1 % (quinolonas de 4.a generación), combinación de antibiótico-corticoide en una presentación en el mismo frasco de colirio, a razón de 4 gotas al día, por 2 semanas o 14 días, esperando que para este tiempo de transcurrida la cirugía, haya cicatrizado la incisión y no haya inflamación en segmento anterior. No las prescribo por más tiempo por las resistencias que se han generado con los antibióticos y que también ya se están reportando con las quinolonas de cuarta generación. Está descrito que tienen una mayor penetración en cámara anterior, alcanzando concentraciones terapéuticas. Son antibióticos que tienen un amplio espectro. Estos motivos son suficientes para pensar en formularlos en el posoperatorio, a pesar de que no hay suficiente evidencia científica que demuestre que los antibióticos en el posoperatorio sean eficaces para prevenir la endoftalmitis.
Dr. Eduardo Viteri: En el posoperatorio de casos rutinarios se indica al paciente continuar aplicando colirio de moxifloxacina TID durante 10 días.
Referencia Dr. Viteri respuesta # 2:
• (*) Miyake, Hitomi & Miyazaki, Dai & Shimizu, Yumiko & Sasaki, Shin-ichi & Baba, Takashi & Inoue, Yoshitsugu & Matsuura, Kazuki. (2019). Toxicities of and inflammatory responses to moxifloxacin, cefuroxime, and vancomycin on retinal vascular cells. Scientific Reports. 9. 10.1038/ s41598-019-46236-2.
Bibliografía sugerida por la Dra. Ángela María Gutiérrez:
- Ciulla TA, Starr MB, Masket S. Bacterial endophthalmitis prophylaxis for cataract surgery: an evidence – based up- date. Ophthaalmology. 2002; 109:13-24
- Behndig A, Cochener B, Guell JL, Kodjikian L, Mencucci R, Nuijts RM, et al. Endophthalmitis prophilaxis in Cataract Surgery: Overview of current practice patterns in 9 Euro- pean countries. J Cataract Refract Surg 2013; 39:1.421- 1.431
- Friling E, Lundstrom M, Stenevi U, Montan P. Six-year inci- dence endophthalmitis after cataract surgery: Swedish na- tional study. J Cataract Refract Surg 2013;39: 15-21
- Vasavada A, Gajjar D, Raj S, Vasavada V, Vasavada V.. Comparison of 2 moxifloxacin regímenes for preoperative prophylaxis: Prospective randomized triple-masked trial. Part 2: Residual conjuntival flora. J Cataract Refract Surg 2008;34: 1383-1388
- Verma L, Chakravarti. Prevention and management of postoperative endophthalmitis: A case-based approach. (Downloaded free from http://www.ijo.in Sunday, Decem- ber 15, 2019, IP: 186.29.150.)
- Merayo-Lloves J, Riestra AC, Galarreta D, Cordovés L, Al- fonso JF. Manejo de la endoftalmitis en cirugía de cataratas. Barcelona: Ediciones Mayo, 2014
- Wycoff CC, Parrott MB, FlynnHW Jr, Shi W Miller D, Alfonso EC. Nosocomial acute-onset postoperative endophthalmi- tis at auniversity teaching hospital (2002 – 2009). Am J Opthalmol. 2010 150:392-398