Introducción
El queratocono es la ectasia corneal más frecuente y se caracteriza por un adelgazamiento y deformación progresiva de la córnea, que puede generar una pérdida visual significativa. En las últimas dos décadas se ha producido un cambio de paradigma en su manejo. El tratamiento, previamente limitado al uso de anteojos, lentes de contacto y, en casos avanzados, a la queratoplastia penetrante, se ha expandido hacia múltiples alternativas terapéuticas y refractivas 1 y 2. Estas incluyen el cross-linking corneal con distintos protocolos, cirugías combinadas con procedimientos querato-refractivos, segmentos de anillos intracorneales, lentes intraoculares fáquicos, queratoplastia lamelar anterior y, más recientemente, el trasplante de la capa de Bowman, los implantes estromales autólogos (CAIRS)³ y los implantes de colágeno porcino (Xenia). La amplia disponibilidad de opciones y combinaciones posibles ha llevado a abordajes individualizados, en los que no siempre existe una única estrategia terapéutica correcta, particularmente en el uso de anillos intracorneales, donde la elección del nomograma depende tanto de la evidencia disponible como de la experiencia del cirujano.
CASO 1:
Paciente de 22 años de edad que consulta por primera vez a control, sin antecedentes oftalmológicos previos registrados. A la evaluación inicial, la agudeza visual resultó:
Ojo derecho 20/20 sin corrección
Ojo izquierdo 20/60 sin corrección y 20/25 con corrección
La refracción manifiesta fue neutra en el OD y de −1.00 −1.00 × 125° en el OI. Presenta la siguiente topografía (figura 1 y 2). ¿Cuál es su conducta inicial?
Receta para anteojos o lentes de contacto y control en 6 meses
Crosslinking bilateral
Crosslinking en ojo izquierdo
Colocación de segmentos intracorneales y crosslinking en ojo izquierdo
Colocación de segmentos intracorneales en ojo izquierdo
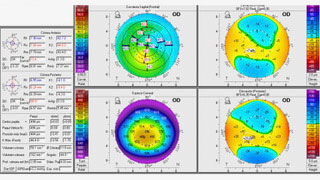
Figura 1: Pentacam ojo derecho Caso 1
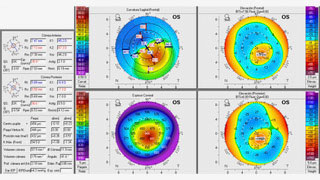
Figura 2: Pentacam ojo izquierdo Caso 1

Dr. Olivier Prisant (Francia)
Respuesta D. Colocación de segmentos intracorneales y crosslinking en ojo izquierdo Comentarios: Este paciente joven requiere cross-linking corneal (CXL) para detener la progresión. Debido a la baja paquimetría, el tratamiento con láser guiado por topografía debe abordarse con cautela. Inicialmente, implantaría un segmento intracorneal (ICRS) de 160° / 150 µm para regularizar la córnea, actuando como un factor de preservación tisular. Luego de algunos meses (> 3), se realizaría CXL, asociado a PRK guiada por topografía (TG-PRK) si se requiere una regularización adicional.
Dra. Jordana Sandes (Brasil)
Respuesta E. Colocación de segmentos intracorneales en ojo izquierdo
Comentarios: Dado que se trata de una primera consulta y no existe documentación previa que confirme progresión de la enfermedad, no indicaría cross-linking corneal en este momento. No parece prudente recomendar un procedimiento que no está exento de riesgos en un paciente sin evidencia de progresión, particularmente cuando un adecuado control de la alergia ocular por sí solo puede contribuir a la estabilidad de la enfermedad.
Por lo tanto, indicaría el uso de anteojos y mantendría un seguimiento estrecho cada cuatro meses, incluyendo evaluaciones seriadas con Pentacam para monitorizar una posible progresión.
Dado que la agudeza visual corregida es buena, el manejo debe individualizarse de acuerdo con los síntomas del paciente; debemos tratar al paciente y no únicamente los hallazgos en las imágenes. Si el uso de anteojos no representa una molestia y el paciente permanece asintomático con corrección, mantendría este enfoque conservador.
Por otro lado, considerando que la agudeza visual no corregida es de 20/60, si el paciente no logra adaptarse al uso de anteojos o desea una mayor independencia visual, lo consideraría funcionalmente monocular. En este escenario, indicaría la implantación de segmentos de anillos intracorneales en el ojo izquierdo, con el objetivo de mejorar la calidad visual y reducir la dependencia de los anteojos.
Justificación y referencias:
El Consenso Internacional de 2025 establece que el cross-linking corneal (CXL) está indicado principalmente en el queratocono progresivo, apoyando un enfoque conservador cuando no se ha demostrado progresión ⁴. Esta estrategia se ve reforzada por estudios de seguimiento a largo plazo y meta-análisis que confirman los beneficios sostenidos del CXL en ectasia progresiva y destacan la importancia de un seguimiento cuidadoso antes de intervenir⁵.
Si bien se reconoce que los pacientes jóvenes presentan un mayor riesgo de progresión, esto no implica la indicación automática de CXL en ausencia de criterios objetivos, sino más bien la necesidad de controles más estrechos y una evaluación individualizada⁶.
Los segmentos intracorneales han demostrado beneficios visuales y topográficos así como también una mejoría de la visión funcional gracias a su rol refractivo ⁷,⁸.
Dra. Cristina Peris – Martínez (España)
Respuesta C. Crosslinking en ojo izquierdo
Comentarios: Aunque no esté documentada la progresión en la historia clínica (aumento de 1D en un espacio de visitas separadas 6 meses), al tratarse de un paciente joven (22 años) tiene muchas posibilidades de progresión y existe una diferencia de astigmatismo topográfico del OD (1,3D) al OI (2,1D) 9. Es por ello, que primero realizaría crosslinking (CXL) en el ojo izquierdo (OI)(respuesta c) para asegurarme la detención de la progresión del queratocono (QC) del OI. Tras el tratamiento posiblemente también mejorará el astigmatismo del OI en 1-2 dioptrías (D) 9,10 y no sea necesario el implante de anillos intracorneales para la rehabilitación visual y el tratamiento refractivo. Además, es importante hacer hincapié en las medidas higiénicas: evitar encarecidamente el frotamiento ocular, colirios antihistamínicos, control de la inflamación y la alergia ocultar si la hubiera. Monitorizaría la evolución del ojo derecho en 6 meses para valorar también el CXL en el OD si progresara.
También se podría optar por una actitud más conservadora, (respuesta a); recetar la gafa o las lentes de contacto y tras documentar la progresión a los 6 meses valorar el CXL. Si se tratara de un paciente pediátrico, no esperaría a documentar la progresión para tratar, ya que la edad joven es uno de los principales factores de riesgo para la progresión 11.
CASO 2:
En un paciente con queratocono progresivo documentado y disminución de la agudeza visual, en quien se ha indicado la implantación de anillos intracorneales, cuál es su estrategia terapéutica?:
Cross linking corneal, y luego de 6 meses colocación de segmentos
Colocación de segmentos y Crosslinking simultáneamente
Implantación de anillos intracorneales como primer paso, con seguimiento evolutivo posterior para definir la necesidad de realizar cross-linking corneal
Implantación de anillos intracorneales seguida de cross-linking corneal diferido, generalmente a los 6 meses.
Dr. Olivier Prisant (Francia)
Respuesta D: Implantación de anillos intracorneales seguida de cross-linking corneal diferido, generalmente a los 6 meses.
Comentarios: La implantación primaria de segmentos intracorneales proporcionaría la mayor parte de la regularización corneal. El cross-linking corneal (CXL) se realizaría al menos 3 meses después, asociado a PRK guiada por topografía (TG-PRK) si se requiere una regularización adicional.
Dra. Jordana Sandes (Brasil)
Respuesta C: Implantación de anillos intracorneales como primer paso, con seguimiento evolutivo posterior para definir la necesidad de realizar cross-linking corneal
Comentarios: En un paciente con queratocono progresivo documentado y disminución de la agudeza visual, en quien se ha indicado la implantación de segmentos de anillos intracorneales, favorecería la implantación de anillos intracorneales como primer paso terapéutico.
Cuando la agudeza visual ya se encuentra comprometida, la implantación inicial de anillos permite la regularización corneal y la rehabilitación visual, lo que a menudo se traduce en una mejora significativa tanto de la agudeza visual no corregida como de la corregida. Este enfoque también facilita una evaluación posterior más precisa del comportamiento de la enfermedad.
El cross-linking corneal quedaría reservado para aquellos casos en los que se documente progresión adicional durante el seguimiento. Si bien el cross-linking es eficaz para detener la progresión de la enfermedad, su objetivo principal no es mejorar la calidad visual, y su realización rutinaria en todos los casos podría exponer innecesariamente a los pacientes a riesgos relacionados con el procedimiento.
Por lo tanto, prefiero una estrategia escalonada e individualizada: rehabilitación visual inicial mediante segmentos de anillos intracorneales, seguida de un monitoreo tomográfico estrecho y la indicación selectiva de cross-linking corneal únicamente si la progresión persiste.
Justificación y referencias:
El estudio aleatorizado de Hersh et al. comparó la realización secuencial versus simultánea de corneal cross-linking (CXL) e intracorneal ring segments (ICRS), y demostró que los resultados topográficos y de agudeza visual fueron comparables entre ambos enfoques13. Estos hallazgos permiten concluir que los ICRS pueden implantarse tanto antes como después del CXL con resultados similares, lo que respalda la estrategia de implantar primero los ICRS y reservar el CXL para una etapa posterior únicamente si resulta necesario.
En la misma línea, Kanellopoulos y Asimellis compararon combinaciones simultáneas versus secuenciales de ICRS y CXL en el manejo del queratocono, observando diferencias relevantes en términos de recuperación corneal y seguridad14. En su serie, los ojos sometidos a CXL e ICRS de manera simultánea en una misma sesión quirúrgica presentaron un mayor riesgo de formación de haze y una recuperación visual más lenta en comparación con aquellos tratados de forma escalonada. Por el contrario, el tratamiento secuencial (ICRS primero, seguido de CXL) se asoció a mejor claridad corneal y a una menor incidencia de complicaciones epiteliales y haze.
Estos resultados coinciden con observaciones reportadas en otras series clínicas, incluyendo las de Alió et al., que describen mayores tasas de haze corneal o cicatrización irregular cuando el CXL y los ICRS se realizan en la misma sesión, particularmente en ausencia de estrategias profilácticas adecuadas15.
Dra. Cristina Peris – Martínez (España)
Respuesta B. Colocación de segmentos y Crosslinking simultáneamente
Comentarios: Si ya se ha documentado la progresión del QC, la indicación del CXL es clara para detener la progresión. Si además es necesario la rehabilitación visual (ya indicación de implante de anillos intracorneales), indicaría el CXL y la colocación de segmentos, a la mayor brevedad posible y de manera simultánea (respuesta b) 16,17.
CASO 3:
Paciente de 26 años, que presenta una agudeza visual en el ojo derecho de 20/60 que no mejora con corrección (Figura 3). Se decide colocar segmentos intracorneales, qué segmentos colocaría y por qué?
1 segmento de 5 mm de 160°
1 segmento de 5 mm 160° asimétrico
2 segmentos de 5 mm: asimétrico de 160° y simétrico de 120°
1 segmento de 5 mm de 210°
1 segmento de 5 mm de 320°
Otra
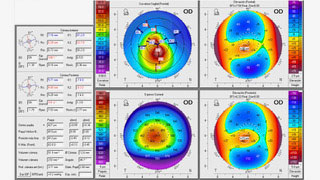
Figura 3: Pentacam ojo derecho Caso 3
CASO 3:
Dr. Olivier Prisant (Francia)
Respuesta F. Otra
Comentarios: Se trata de un queratocono con fenotipo tipo snowman y alto astigmatismo topográfico (6,5 D). Implantaría dos Kerarings asimétricos opuestos (1 Keraring AS 160° / 200–300 µm en sentido horario + 1 Keraring AS 160° / 200–300 µm en sentido antihorario)18.. La miopía preoperatoria debe confirmarse para evitar un desplazamiento hipermetrópico. El protocolo de Atenas se realizaría algunos meses después.
Dra. Jordana Sandes (Brasil)
Respuesta B: 1 segmento de 5 mm 160° asimétrico
Comentarios: La elección de un único segmento asimétrico de 160° estuvo guiada por nomogramas topográficos y paramétricos que consideran la asfericidad, el astigmatismo y el eje de coma, los cuales sugieren una mejor regularización corneal en conos paracentrales u ovales con marcada asimetría (Fernández et al.; Iqbal; Utine).
La documentación técnica de Ferrara / KeraRing (SSCP / manuales) describe las diferentes opciones de arco (incluyendo 160°) y sus indicaciones según el patrón del cono y el espesor corneal. Esto constituye una referencia práctica y de la industria que respalda la elección del arco utilizado.
En los fenotipos de queratocono asimétrico, un ensayo clínico aleatorizado que comparó segmentos de anillos intracorneales simétricos versus asimétricos demostró resultados topográficos, tomográficos y visuales superiores con el uso de ICRS asimétricos, lo que respalda la elección de un único segmento asimétrico largo en casos con conos irregulares u ovales19.
Dra. Cristina Peris – Martínez (España)
Respuesta E. 1 segmento de 5 mm de 320°
Comentarios: La alteración visual de los pacientes con QC viene fundamentalmente por el astigmatismo y la aberración cromática. En este caso no tenemos datos de la aberración cromática. El paciente tiene en su OD un astigmatismo irregular topográfico de 6,5 D, con una Kmax de 53,7 y una K min de 47,2D. Asfericidad Q -1,30 (alta). Si queremos reducir el gran astigmatismo, los anillos más próximos al eje visual (5 mm) son los más indicados. El espesor de la córnea en la zona de implante de los anillos a 5 mm oscila en torno a 467-500 micras. Profundidad de implante del anillo si es con láser de femtosegundo al 70% del espesor corneal mínimo Basándonos en estos parámetros la opción c: 2 segmentos de 5 mm: asimétrico de160º y simétrico de 120º reduciría de manera significativa el astigmatismo, pero recientes estudios están demostrando que el implante de 1 segmento único de gran longitud de arco puede reducir aún más el astigmatismo topográfico, aunque quirúrgicamente tenga una mayor dificultad su inserción 20, 21. Por ello implantaría la respuesta e: 1 segmento de 5 mm de 320°.
REFERENCIAS
D’Oria F, Bagaglia SA, Alio Del Barrio JL, Alessio G, Alio JL, Mazzotta C. Refractive surgical correction and treatment of keratoconus. Surv Ophthalmol. 2024 Jan-Feb;69(1):122-139. doi: 10.1016/j.survophthal.2023.09.005. Epub 2023 Sep 27. PMID: 37774800.
Deshmukh R, Ong ZZ, Rampat R, Alió Del Barrio JL, Barua A, Ang M, Mehta JS, Said DG, Dua HS, Ambrósio R Jr, Ting DSJ. Management of keratoconus: an updated review. Front Med (Lausanne). 2023 Jun 20;10:1212314. doi: 10.3389/fmed.2023.1212314. PMID: 37409272; PMCID: PMC10318194.
Jacob S, Agarwal A, Awwad ST, Mazzotta C, Parashar P, Jambulingam S. Customized corneal allogenic intrastromal ring segments (CAIRS) for keratoconus with decentered asymmetric cone. Indian J Ophthalmol. 2023 Dec 1;71(12):3723-3729. doi: 10.4103/IJO.IJO_1988_23. Epub 2023 Nov 20. PMID: 37991313; PMCID: PMC10788746.
Gomes JAP, Tan D, Rapuano CJ, et al. *Global consensus on keratoconus and ectatic diseases*. Cornea. 2015;34(4):359-369.
Larkin DFP, Leung V, Pooley J, et al. *Long-term outcomes of corneal collagen cross-linking for progressive keratoconus and ectasia: a systematic review and meta-analysis*. Ophthalmol Ther. 2021;10(2):231-245.
Chatzis N, Hafezi F. *Progression of keratoconus and efficacy of corneal collagen cross-linking in children and adolescents*. J Refract Surg. 2012;28(5):271-276.
DS, Kymionis GD, Ginis HS, et al. *Ferrara intrastromal corneal rings for the correction of keratoconus*. J Cataract Refract Surg. 2002;28(8):1480-1487.
Carrasquillo KM, Marrone M, Tan J, et al. *Efficacy of small-incision intrastromal corneal ring segments for keratoconus: a systematic review and meta-analysis*. J Cataract Refract Surg. 2018;44(6):747-754.
Wollensak G., Spoerl E., Seiler T. Riboflavin/ultraviolet-a–induced collagen crosslinking for the treatment of keratoconus. American Journal of Ophthalmology. 2003;135(5):620–627. doi: 10.1016/S0002-9394(02)02220-1
Gomes JA, Tan D, Rapuano CJ, Belin MW, Ambrósio R Jr, Guell JL, Malecaze F, Nishida K, Sangwan VS; Group of Panelists for the Global Delphi Panel of Keratoconus and Ectatic Diseases. Global consensus on keratoconus and ectatic diseases. Cornea. 2015 Apr;34(4):359-69. doi: 10.1097/ICO.0000000000000408. PMID: 2573823
Hafezi F, Kling S, Hafezi NL, Aydemir ME, Lu NJ, Hillen M, Knyazer B, Awwad S, Mazzotta C, Kollros L, Torres-Netto EA. Corneal cross-linking. Prog Retin Eye Res. 2025 Jan; 104:101322. doi: 10.1016/j.preteyeres.2024.101322. Epub 2024 Dec 15. PMID: 39681212.
Einan-Lifshitz A, Achiron A, Hed S, Hecht I, Dubinsky-Pertzov B, Knyazer B. Three-year follow- up of accelerated versus standard corneal cross-linking in paediatric Keratoconus. Eye (Lond). 2023 Apr;37(6):1219-1224. doi: 10.1038/s41433-022-02093-4. Epub 2022 May 19. PMID:35590103; PMCID: PMC10102302.
Hersh PS, Issa R, Greenstein SA. Corneal crosslinking and intracorneal ring segments for keratoconus: A randomized study of concurrent versus sequential surgery. J Cataract Refract Surg. 2019 Jun;45(6):830-839. doi: 10.1016/j.jcrs.2019.01.020. Epub 2019 Mar 27. PMID: 30928252.
Kanellopoulos AJ, Asimellis G. Comparison of simultaneous vs sequential corneal cross-linking and intrastromal ring segments in keratoconus: effects on corneal clarity. Clinical Ophthalmology. 2014;8:2249–2258.
Alió JL, et al. Combined ICRS and CXL in keratoconus: corneal haze and its effect on visual outcomes. Journal of Refractive Surgery. 2017;33(9):619–627.
Fernández-Vega-Cueto L, Romano V, Zaldivar R, Gordillo CH, Aiello F, Madrid-Costa D, Alfonso JF. Surgical Options for the Refractive Correction of Keratoconus: Myth or Reality. J Ophthalmol. 2017; 2017:7589816. doi: 10.1155/2017/7589816. Epub 2017 Dec 18. PMID: 29403662; PMCID: PMC5748308.
Nasrat MM, Abdelsalam AM, Goily MB, Eldib AA, Hegazy GA. Keratometric Outcomes after Simultaneous versus Sequential Intracorneal Ring Segment Implantation with Femtosecond Laser and Corneal Collagen Crosslinking in Egyptian Patients with Keratoconus and Ectasia. J Microsc Ultrastruct. 2022 Sep 6;12(1):35-42. doi: 10.4103/jmau.jmau_80_21. PMID: 38633569; PMCID: PMC11019591.
Clinical Outcomes of an Asymmetric Model of Intrastromal Corneal Ring Segments for the Correction of Keratoconus. O. Prisant. Cornea 39(2):155–160, febrero de 2020.
Nassaralla BA, Sandes J, et al. *A randomized controlled trial of symmetric versus asymmetric intrastromal corneal ring segments for asymmetric keratoconus*. [EJO]. 2025
Guilherme MP, Frederico MP, Alessandra MCC, Carolina SB, Anna FRP, Caroline AC, Frederico BDS. Surprising astigmatism hypercorrection after corneal ring segments implantation in keratoconus treatment after 8 years of follow up. Rom J Ophthalmol. 2021 Jan-Mar;65(1):80-84. doi: 10.22336/rjo.2021.16. PMID: 33817440; PMCID: PMC7995498.
Torquetti, Leonardo MD, PhD*; Cunha, Priscila MD†; Luz, Allan MD, PhD‡; Kwitko, Sérgio MD§; Carrion, Márcio MD¶; Rocha, Guilherme MDII; Signorelli, Armando MD**; Coscarelli, Sandro MD††; Ferrara, Guilherme MD‡‡; Bicalho, Frederico MD†; Neves, Renato MD§§; Ferrara, Paulo MD, PHD‡‡. Clinical Outcomes After Implantation of 320°-Arc Length Intrastromal Corneal Ring
Segments in Keratoconus. Córnea 37(10):p 1299-1305, October 2018. | DOI: 10.1097/ ICO.0000000000001709

 28º Curso Regional Panamericano de Oftalmología (PAAO 2026) + 30º Congreso Chileno de Oftalmología (COCHIOF)
28º Curso Regional Panamericano de Oftalmología (PAAO 2026) + 30º Congreso Chileno de Oftalmología (COCHIOF) ASCR 2026
ASCR 2026 BRASCRS 2026
BRASCRS 2026 XLII Congreso Internacional de Oftalmología
XLII Congreso Internacional de Oftalmología XXVI Congreso Internacional ALACCSA – R
XXVI Congreso Internacional ALACCSA – R

 Dr. Sofía Ambrosetto
Dr. Sofía Ambrosetto
 Dra. Malena Parmeggiani
Dra. Malena Parmeggiani




 Dr. Ricardo Stevenson
Dr. Ricardo Stevenson











